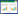文章信息
- 贾山, 张紫薇, 谭佳威, 杨冰, 白洁, 李鹏跃, 杜守颖, 陆洋
- JIA Shan, ZHANG Ziwei, TAN Jiawei, YANG Bing, DU Shouying,
- 通窍散瘀方微乳的制备及评价
- Preparation and evaluation of Tongqiao Sanyu microemulsion
- 天津中医药大学学报, 2018, 37(5): 393-398
- Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(5): 393-398
- http://dx.doi.org/10.11656/j.issn.1673-9043.2018.05.12
-
文章历史
收稿日期: 2018-03-25
通窍散瘀方原方为王永炎院士临床经验方,由葛根、白芍、薄荷脑等药味组成,用于治疗急性脑中风,疗效确切。方中主要成分有葛根素、芍药苷和薄荷脑。主要药效成分为葛根素、芍药苷。葛根素具有扩张冠状动脉、抗心肌缺血,抑制血小板凝集、改善脑循环[1]、对脑缺血及缺血再灌注引起的神经细胞损伤具有保护作用[2-3]。芍药苷对脑神经元有保护作用[4],薄荷脑在一定浓度范围内能够促进葛根素的渗透,当浓度达到5 mg/mL时具有显著促渗作用[5]。通窍散瘀方在临床上主要以水煎液给患者。而方中主要药效成分葛根素在水和油中的溶解度都很低[6],提高葛根素的生物利用度非常必要。为了发挥该方速效急救的临床疗效,研制一种安全稳定并使有效成分能够直达脑部的剂型非常必要。微乳作为一种新型的纳米制剂,具有脑靶向、低刺激性和高稳定性的特点。
本研究首先通过伪三元相图制备通窍散瘀方微乳,并对其理化性质、含量、刺激性进行评价。
1 材料仪器LC-20AD高效液相色谱仪(日本岛津公司,SPD-M20A,PDA检测器;LC Solution色谱工作站);磁力搅拌器(金坛区华城润华实验仪器厂);激光粒径测定仪(Zetasizer Nano ZS,英国马尔文仪器有限公司);TK-20B型透皮扩散试验仪(上海皆凯科技贸易有限公司);葛根素提取物(北京普博欣生物科技有限责任公司,批号PB10624-1);芍药苷提取物(北京普博欣生物科技有限责任公司);薄荷脑提取物(北京普博欣生物科技有限责任公司,批号PB31210);葛根素对照品(110752-201615);芍药苷对照品(110736-201441);肉豆蔻酸异丙酯IPM(麦克林);油酸乙酯(北京化工厂);油酸(北京化工厂);蓖麻油聚氧乙烯35(阿达玛斯试剂公司);辛酸葵酸聚乙二醇甘油酯(labrasol)(嘉法狮(上海)贸易有限公司)等;SD大鼠,雄性,体质量(180~220)g[北京维通利华实验动物技术有限公司许可证编号:SCXK(京)2006-2009]。
2 方法与结果 2.1 葛根素在各油相、乳化剂、助乳化剂中的溶解度考察 2.1.1 色谱条件十八烷基键合硅胶柱;甲醇-水(37:63)(1%醋酸);流速1.0 mL/min;检测波长:250 nm,柱温:25 ℃,进样量:20 μL。
2.1.2 标准曲线的绘制精密称取葛根素对照品适量,用甲醇溶解并稀释成浓度为613.000、367.800、122.600、61.300、24.520、2.452 μg/mL的葛根素标准供试液。按照上述色谱条件,进样20 μL,记录峰面积。以样品色谱峰面积A对浓度C进行线性回归,结果表明,葛根素在2.452~613 μg/mL线性关系良好,回归方程为Y=51 121 441.36X-34 622.21,r2=0.999 9。
2.1.3 精密度实验取高、中、低质量浓度(613、367.8、2.452 μg/mL),连续进样3次,记录峰面积,计算RSD值0.33%、0.17%、0.000 80%。表明仪器精密度良好。
2.1.4 稳定性实验分别在2、4、6、8、10、12 h测样品含量。计算RSD值,RSD值为1.79%,表明12 h内样品稳定性良好。
2.1.5 溶解度实验测定葛根素在不同油相(IPM、油酸、油酸乙酯中)、不同乳化剂(EL-35、吐温80、辛酸葵酸聚乙二醇甘油酯(Labrasol)、不同助乳化剂(1,2-丙二醇、无水乙醇、丙三醇、PEG400、Transpol p(二乙二醇单乙基醚))中的溶解度。室温下,在足量的葛根素中,分别加入5 mL的各溶媒,搅拌48 h,使药物充分溶解。在3、9、12、24、48 h取点,每次取300 μL。然后于5 000 r/min下离心15 min,精密量取上清液100 μL,甲醇定容到10 mL,HPLC测定葛根素含量。结果见1~2。
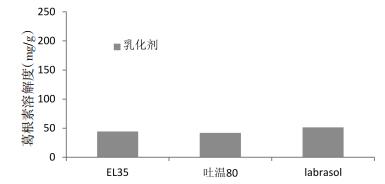
|
| 图 1 葛根素在不同乳化剂中的溶解度 |
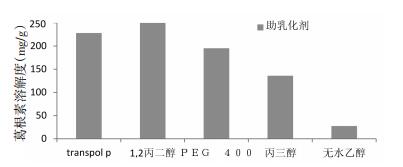
|
| 图 2 葛根素在不同助乳化剂中的溶解度 |
结果显示,对于油相,IPM、油酸、油酸乙酯,葛根素在其中的溶解度均小于0.1 mg/g,说明葛根素在油中的溶解度很低,因此选择这3种油相作进一步的研究。葛根素在3种表面活性剂中的溶解度都大于40 mg/g,且大小差不多,因此选择这3种乳化剂进行进一步的实验。对于助乳化剂,葛根素在1,2-丙二醇的溶解度为254.83 mg/g,明显高于在其他助乳化剂的溶解度。因此选择这1,2丙二醇作为助乳化剂。
2.2 微乳油相的筛选精密称取EL35作为乳化剂,1,2-丙二醇作为助乳化剂,乳化剂和助乳化剂按质量比(Km)为1:1混合均匀,制成混合乳化剂。将混合乳化剂分别与IPM、油酸乙酯、油酸,按质量比9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9的比例精确称量,置于西林瓶中,25 ℃恒温,350 r/min磁力搅拌混合均匀,以去离子水滴定,每滴一次待其充分混合均匀,观察液体的形态变化,同时以入射光照射,观察是否有丁达尔现象,记录体系的临界变化点。计算临界点时每个组分在微乳体系中的质量百分含量,借助O-riginPro8.0软件绘制微乳的伪三元相图,确定O/W型微乳区。结果见图 3。
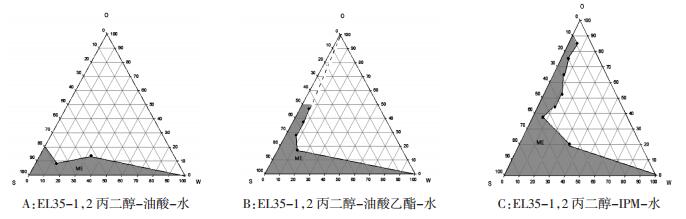
|
| 图 3 微乳的伪三元相图 |
结果显示,EL35-1,2丙二醇-IPM-水微乳区面积最大。微乳区面积大者,微乳的稳定性较好。所以选择IPM作为油相。
2.3 微乳乳化剂的筛选精密称取IPM作为油相,1,2-丙二醇作为助乳化剂、EL-35、吐温80、(Labrasol)为乳化剂,将各乳化剂和助乳化剂按质量比(Km)1:1,混合均匀,制成混合乳化剂。将不同的混合乳化剂与IPM,按质量比9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9的比例精确称量,置于西林瓶中,后面的实验操作同2.2。结果见图 4。
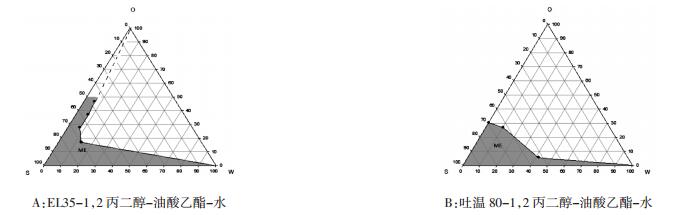
|
| 图 4 不同微乳乳化剂的伪三元相图 |
结果显示,以Labrasol作乳化剂的处方,在任何比例下都不可形成微乳。而以EL35,吐温80为乳化剂的微乳面积比较,EL35的微乳区面积大者,选择乳化剂EL-35。
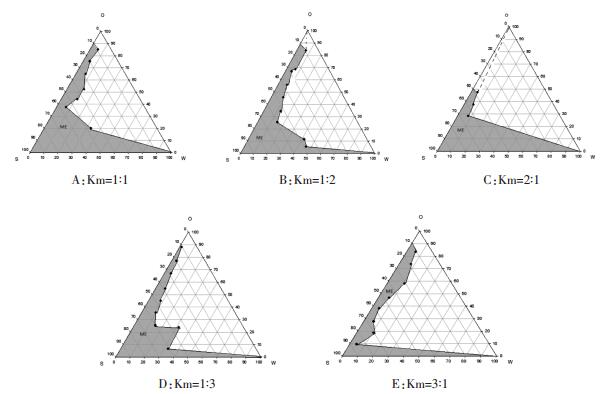
2.4 微乳Km值的筛选精密称取EL35作为乳化剂和1,2-丙二醇作为助乳化剂按质量比(Km)为3:1、2:1、1:1、1:2、1:3分别混合均匀,制成混合乳化剂。将混合乳化剂与IPM,按质量比9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8和1:9的比例精确称量,置于西林瓶中,后面的实验操作同2.2。结果见图 5。
|
| 图 5 不同km值的伪三元相同 |
结果显示,当Km=1:1时,微乳区面积最大,选择Km=1:1。
2.5 最佳空白微乳处方的筛选在筛选出的以IPM为油相、EL-35为乳化剂、1,2丙二醇为助乳化剂,Km值为1:1的伪三元相图中,筛选13个点作进一步研究。乳化剂的用量一般为处方的40%~60%,油相为5%左右。
采用马尔文激光粒径测定仪,对已经选择的微乳区域内的13个处方进行粒径和多分散指数(PDI)测定。以形成微乳的外观、粒径、PDI作为衡量指标综合考虑,选择最佳处方配比,作为最优处方。结果见表 1。
结果显示,处方2、处方5和处方13,外观澄清透明,PDI小,比较稳定。将这3个处方进行进一步实验。
2.6 最佳载药微乳处方的筛选考察葛根素载药量500、600、700、800、900、1 000 mg葛根素。芍药苷和薄荷脑按照处方比例添加到空白微乳处方中。处方比例为葛根素:芍药苷:薄荷脑=2:1:0.8。将空白处方2,处方5和处方13加入各药物之后,制得载药微乳,在常温下放置,处方13载药500 mg在第2天析出,处方5载药500 mg在第10天析出,处方2载药500、600、700 mg,放置不析出,根据最大载药量原则,最终选择载药量700 mg。
2.7 通窍散瘀微乳处方设计设计空白处方总量为10 g,IPM 0.519 g,1,2-丙二醇2.923 g,EL35 2.923 g,水3.635 g,其中载药葛根素700 mg,芍药苷280 mg,薄荷脑350 mg。
2.7.1 通窍散瘀微乳制法取10 mL西林瓶,按照处方比例依次加入1,2丙二醇、EL35、葛根素,25 ℃恒温水浴,以350 r/min搅拌,使其充分溶解。加入薄荷脑、IPM。搅拌,使其充分溶解, 作为A相。另取芍药苷提取物加入相应量的纯净水中搅拌使其充分溶解,作为B相。将B相逐滴加入A相中,不断搅拌使混合均匀,即得。
2.8 通窍散瘀方微乳pH值测定取3个批号的通窍散瘀方微乳各10 g,置于西林瓶中,将pH酸度计校正平衡后,测定3个样品的pH值。
结果显示,醒脑静鼻用微乳的平均pH值为5.31,而正常生理状态下,鼻腔内pH值为4.5~6.5,在此PH值下,生物适应性良好[7]。
2.9 微乳中葛根素和芍药苷含量测定 2.9.1 色谱条件Agilent C18(4.6 mm×250 mm,5 μm)色谱柱,柱温30 ℃;流动相乙腈-甲醇-水(15:10:75);流速1.0 mL/min;葛根素检测波长250 nm;芍药苷检测波长230 nm;进样量10 μL。
2.9.2 标准曲线的建立分别精密称取葛根素、芍药苷对照品6.64、5.2 mg,加甲醇配制成葛根素浓度为0.066 4 mg/mL,芍药苷浓度为0.013 mg/mL的对照品储备液。配置成一系列葛根素浓度为66.40、33.20、16.60、8.30、6.64、3.32 μg/mL的对照品溶液。芍药苷浓度为26.00、13.00、6.50、3.25、2.60、1.30 μg/mL,摇匀,得到标准溶液系列。按上述色谱条件依次进样。以测得峰面积A与其浓度C线性回归,得葛根素标准曲线方程Y=37 784 682.811 1X+22 121.591 5,r=0.999 4,线性范围3.32~66.40 μg/mL,芍药苷标准曲线方程Y=12 863 791.653 0X+4 071.561 6,r=0.999 4,线性范围1.300~26.00 μg/mL。
2.9.3 专属性考察 2.9.3.1 空白体系微乳的配制精密称取微乳1.064 4 g,15 000 r/min离心10 min,取上清液,于10 mL容量瓶中,加甲醇定容。取1 mL加到25 mL,加甲醇定容。取1mL加到10 mL容量瓶中,加甲醇定容。
2.9.3.2 样品溶液的配制精密称取微乳1.005 0 g,15 000 r/min离心10 min,取上清液,于10 mL容量瓶中,加甲醇定容。取1 mL加到25 mL,加甲醇定容。取1 mL加到10 mL容量瓶中,加甲醇定容。
2.9.4 精密度实验取同一对照品溶液,重复进样6次。葛根素峰面积RSD =0.13%,芍药苷RSD =0.40%,表明本实验的方法精密度良好。
2.9.5 重现性实验取同一批样品6份,分别制成供试品溶液,按含量测定法测定,结果葛根素,RSD=0.19,芍药苷RSD=0.61,表明本实验的方法重现性良好。
2.9.6 稳定性考察取载药微乳溶液,按照供试品的处理方法制成待测液后,于0、2、4、6、8、10、12、24 h进行测定,记录峰面积值,葛根素RSD=0.17,芍药苷RSD=0.74,表明供试品在处理后24 h保持稳定。
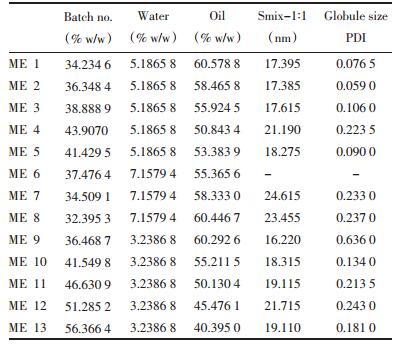
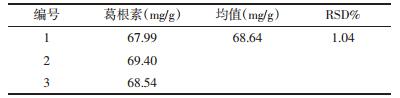
2.9.7 载药微乳的含量测定取3批样品,依供试品溶液的处理办法制成供试品溶液,按照2.9.3项下进行测定,结果如下表 2~3。
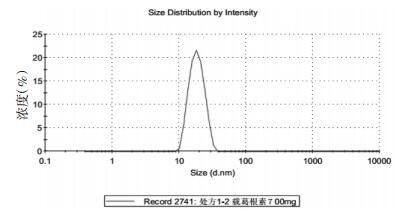
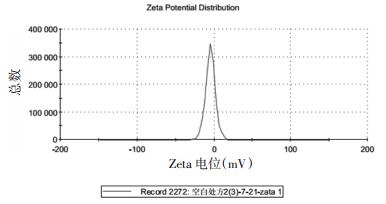
采用激光散射法测定了空白微乳和载药微乳的,取稀释10倍的载药微乳适量,用马尔文粒径仪测定自微乳的粒径和Zeta电位,记录粒径及电位。载药微乳的平均粒径(直径)为17.86 nm,PDI为0.031,Zeta电位为-4.90 mV。空白微乳的粒径和电位与载药微乳差异不大,结果见图 6~7。
|
| 图 6 载药微乳的粒径 |
|
| 图 7 载药微乳的电位 |
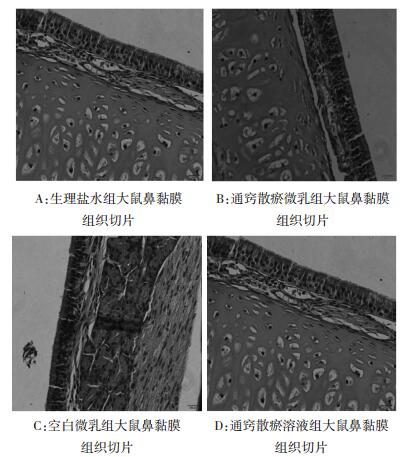
大鼠共21只,随机分为4组,其中载药微乳组、空白微乳组、药物混悬液组各6只,生理盐水组3只。第1天给药3次,每次给药50 μL,在给药后的第2天和第8天分别处死3只大鼠(生理盐水组第2天处死)。取鼻中隔软骨(带黏膜),苏木精-伊红(HE)染色,石蜡切片,做光镜观察,结果见图 8~9。
|
| 图 8 给药第2天倒置显微镜下观察图(40×) |
|
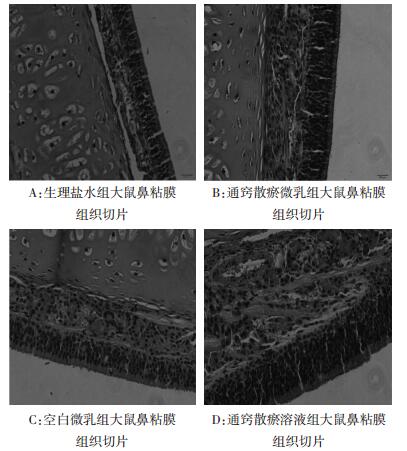
| 图 9 给药8天后倒置显微镜下观察图(40×) |
结果显示,HE染色下生理盐水组大鼠鼻粘膜病理切片中可见无上皮细胞无增生,排列整齐,杯状细胞少,固有层无水肿。通窍散瘀微乳组病理切片可见上皮细胞的纤毛脱落,固有层水肿,腺体增生,血管不同程度扩张并略微充血。通窍散瘀微乳恢复1周组的大鼠病理切片大鼠鼻黏膜恢复正常。通窍散瘀药液组大鼠鼻黏膜切片可见杯状细胞增多,腺体增生,血管不同程度扩张并有充血现象。通窍散瘀药液恢复1周组大鼠鼻黏膜未恢复正常,仍可见杯状细胞增多,腺体增生,血管不同程度扩张并有充血现象。
4 讨论方中的葛根素是难溶性成分,提高葛根素溶解度很重要。首先采用溶解度实验初步选出乳化剂、助乳化剂、油相,再以滴水法绘制伪三元相图,单因素考察乳化剂、助乳化剂、油相,进一步筛选出合适的乳化剂、助乳化剂、油相。以粒径、PDI为指标,确定乳化剂、助乳化剂、油相的比例。再以载药量为指标,确定处方中各药物的量,最终制备载药微乳。
通窍散瘀微乳能显著提高难溶性药物葛根素的载药量,并且形成均一稳定的体系。可为通窍散瘀方给药提供新的剂型。
通过大鼠鼻中隔切片实验研究结果可以发现,以生理盐水作为对照组,通窍散瘀微乳给药后有一定毒性,然而在给药1周后切片观察,发现其纤毛再生,细胞在恢复,表明通窍散瘀微乳虽对大鼠鼻黏膜和纤毛产生刺激性,但其可以恢复。说明微乳对鼻腔的刺激性具有可逆性,可为通窍散瘀方给药提供新的剂型。
| [1] |
伟唯, 江培. 葛根素药理作用研究进展[J]. 黑龙江医药, 2014, 27(1): 51-55. |
| [2] |
潘洪平. 葛根总黄酮和葛根素的药理作用和临床应用研究进展[J]. 广西医学, 2003, 25(10): 1941-1944. DOI:10.3969/j.issn.0253-4304.2003.10.044 |
| [3] |
徐晓虹, 陈瑜, 郑筱祥. 葛根素对脑缺血诱导神经细胞凋亡的保护作用[J]. 中国药学杂志, 2006, 41(21): 1628-1631. DOI:10.3321/j.issn:1001-2494.2006.21.009 |
| [4] |
李冬梅, 徐丽, 张淑珍, 等. 芍药苷对沙土鼠脑缺血再灌注损伤的保护作用[J]. 医学研究生学报, 2014, 11: 1139-1142. DOI:10.3969/j.issn.1008-8199.2014.11.005 |
| [5] |
李鹏跃, 陆洋, 杜守颖, 等. 薄荷脑对葛根素体外黏膜的促渗作用研究[J]. 中国药房, 2012, 47: 4425-4427. DOI:10.6039/j.issn.1001-0408.2012.47.04 |
| [6] |
王展.制剂新技术提高葛根素溶解性能的研究[D].北京: 北京中医药大学, 2007. http://cdmd.cnki.com.cn/Article/CDMD-10026-2007077960.htm
|
| [7] |
刘永革.鼻腔pH值的测定(摘要)[A].中国中西医结合耳鼻咽喉科专业委员会.第三届第二次全国中西医结合耳鼻咽喉科学术大会论文汇编[C].中国中西医结合耳鼻咽喉科专业委员会, 2000.
|
 2018, Vol. 37
2018, Vol. 37