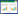文章信息
- 张兵, 张丽娜, 韩鹏军, 黄瑞, 祁东利, 刘志东
- ZHANG Bing, ZHANG Lina, HAN Pengjun, HUANG Rui, QI Dongli, LIU Zhidong
- 白术中3种内酯成分的含量测定及指纹图谱研究
- Determination of 3 atractylenolides in Atractylodes macrocephala Koidz. and the study of the fingerprint
- 天津中医药大学学报, 2018, 37(5): 411-415
- Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(5): 411-415
- http://dx.doi.org/10.11656/j.issn.1673-9043.2018.05.15
-
文章历史
收稿日期: 2018-05-22
2. 天津中医药大学, 天津市现代中药重点实验室-省部共建国家重点实验室培育基地, 天津 300193
2. Tianjin State Key Laboratory of Modern Chinese Medicine, Tianjin 300193, China
中药白术为菊科植物白术(Atractylodes macrocephala Koidz.)的干燥根茎。中医认为白术味苦、甘,性温。归脾、胃经。具有健脾益气,燥湿利水,止汗,安胎功效。用于脾虚食少,腹胀泄泻,痰饮眩悸,水肿,自汗,胎动不安等症[1]。近年来的研究表明白术具有抗炎、利尿、抗衰老、抑制肿瘤、促进胃肠运动、提高机体免疫力等作用[2-7],同时对神经系统与子宫平滑肌也有一定调节作用[8-9]。2015年版中国药典中仅收录了白术饮片,并未指明其药材、饮片的含量测定项。本文研究建立了白术内酯Ⅰ、Ⅱ、Ⅲ含量测定方法,对来自4个产地的12批次白术饮片进行了上述成分的含量测定,测定了白术饮片的指纹图谱,并对结果进行聚类分析,以期为白术的质量标准研究提供依据和参考。
1 仪器与试药岛津LC-20A液相色谱仪(日本岛津公司),安捷伦1200LC-DAD液相色谱仪(美国安捷伦公司),XP205型十万分之一天平(METTLER TOLEDO),F124型万分之一天平(天津亿诺科学仪器有限公司),Q-300B型超声波清洗仪(昆山市超声仪器有限公司),Mill-QⅡ型超纯水系统(Millipore公司),中草药粉碎机(天津市泰斯特仪器有限公司)。
白术内酯Ⅰ(天津中新药业,Lot. No.: W10-3-1,纯度≥98.0%);白术内酯Ⅱ(天津中新药业,Lot. No.: W13-4-9,纯度≥98.0%);白术内酯Ⅲ(天津中新药业,Lot. No.: W09-9-8,纯度≥98.0%);乙腈为色谱级(天津康科德试剂有限公司);水为超纯水;白术饮片来源见表 1。
分别精密称取白术内酯Ⅰ、Ⅱ、Ⅲ对照品适量,加甲醇制成每1 mL含76.83、77.61、156.40 μg的标准对照品储备液。
2.1.2 供试品溶液制备精密称取样品粉末(过5号筛)2 g,置具塞锥形瓶中,精密加入甲醇25 mL,称定质量,超声处理(功率300 W,频率45 kHz)30 min,取出,再称质量,用甲醇补足减失质量,摇匀,滤过,取续滤液,即得。
2.1.3 色谱条件色谱柱Agilent ZORBAX Eclipse Plus C18(5 μm, 250 mm×4.6 mm),流动相为乙腈-水=50:50(v/v),流速1.0 mL/min,柱温30 ℃,进样量10 μL,检测波长222 nm(白术内酯Ⅰ、Ⅲ)[10-11]与278 nm(白术内酯Ⅱ)[10-14]。
2.1.4 线性关系考察取各对照品溶液,用甲醇稀释成系列浓度,按2.1.3中条件测定色谱峰面积,以标准品浓度(μg/mL)为横坐标(X),色谱峰面积为纵坐标(Y),绘制标准曲线,白术内酯Ⅰ、Ⅱ、Ⅲ回归方程分别为:Y=44 219X-1 399.9(r2=0.998 5),Y=57 339X-1 035.3(r2=0.999 2),Y=27 654X-3 278.8(r2=0.996 9);线性范围分别为0.015~0.768 μg,0.016~0.776 μg和0.031~1.594 μg。
2.1.5 精密度实验精密吸取安徽20150603批次白术饮片供试品溶液10 μL,连续进样6次,测定色谱峰面积,结果白术内酯Ⅰ、Ⅱ、Ⅲ的RSD(n=6)分别为1.58%、2.28%和1.03%。数据表明本实验精密度良好。
2.1.6 稳定性实验精密吸取安徽20150603批次白术饮片供试品溶液10 μL,于0、2、4、8、12、24 h分别进样分析,测定色谱峰面积,结果白术内酯Ⅰ、Ⅱ、Ⅲ的RSD(n=6)分别为1.46%、3.81%和0.96%。表明供试品溶液在制备后24 h内稳定。
2.1.7 重复性实验精密称取安徽20150603批次白术饮片粉末6份,每份2 g,按2.1.2项下方法制备供试品溶液,精密吸取10 μL进样测定。结果白术内酯Ⅰ、Ⅱ、Ⅲ的RSD分别为2.61%、2.35%和3.50%。结果表明方法重复性良好。
2.1.8 加样回收实验取已知白术内酯含量的样品粉末6份,每份1 g,精密称定,置锥形瓶中,加入浓度为76.83 μg/mL的白术内酯Ⅰ对照品溶液10 mL,浓度为77.61 μg/mL的白术内酯Ⅱ对照品溶液3 mL,加入浓度为78.20 μg/mL的白术内酯Ⅲ对照品溶液各6 mL,按2.1.2项下方法制备供试溶液,精密吸取10 μL进样测定,计算回收率。结果白术内酯Ⅰ、Ⅱ、Ⅲ的平均回收率分别为100.98%,95.35%和95.23%,RSD分别为0.78%,2.40%和4.46%。结果表明方法加样回收率结果良好。
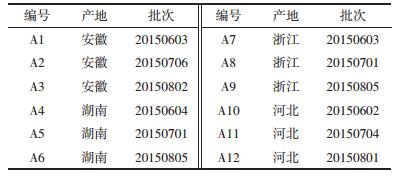
2.1.9 样品测定结果分别取4个产地12批次白术样品粉末,每个样品取2份,按2.1.2项下方法制备供试品溶液,精密吸取10 μL进样测定,样品中白术内酯Ⅰ、Ⅱ、Ⅲ的含量结果见表 2。
2.2 白术饮片指纹图谱的建立与测定 2.2.1 标准对照品溶液和供试品溶液制备见2.1项下内容。
2.2.2 色谱条件色谱柱Agilent ZORBAX Eclipse Plus C18(5 μm, 250 mm×4.6 mm),流动相为乙腈(A)-水(B),梯度洗脱程序为:0~15 min,45%~55%A;15~20 min,55%A;20~40 min,55%~61%A;40~51 min,61%~69%A;51~80 min,69%~100%A;80~87 min,100%A;流速1.0 mL/min,进样量10 μL,柱温25 ℃,检测波长220 nm。
2.2.3 精密度实验取供试品溶液,连续进样6次,按2.2.2项下的色谱条件测定,以参比峰的保留时间和峰面积为参照,计算得供试品溶液中各共有峰相对保留时间的RSD为0.04%~2.61%,相对峰面积的RSD为0.59%~6.91%,表明仪器稳定,仪器精密度良好。
2.2.4 稳定性实验取供试品溶液,在0、2、4、8、12、24、48 h按2.2.2项下的色谱条件测定6次。以参比峰的保留时间和峰面积为参照,计算得供试品溶液中各共有峰相对保留时间RSD在0.003%~1.82%,相对峰面积的RSD在1.09%~7.58%,表明供试品溶液在48 h内稳定。
取6份供试品溶液,按2.2.2项下的色谱条件测定。以参比峰的保留时间和峰面积为参照,计算得供试品溶液中各共有峰相对保留时间的RSD为0.00%~0.08%,相对峰面积的RSD为1.46%~6.28%,表明方法重复性好。
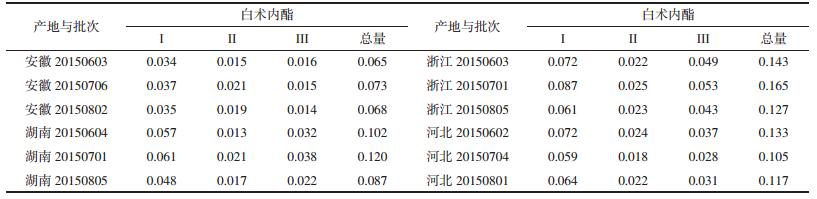
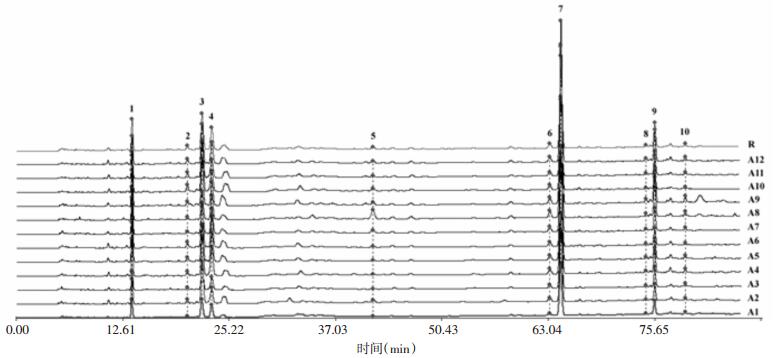
2.2.6 样品的测定和指纹图谱的建立取标准对照品溶液和12批白术供试品溶液,分别进样10 μL,液相测定。将色谱数据导入“中药色谱指纹图谱相似度评价系统(2004A版)”,7号峰峰面积最大且稳定,故选择作为参比峰(S),以A1图谱为校正参照,时间窗宽度设为1.0 min,建立12批次白术饮片指纹图谱叠加图,见图 1,确定10个共有峰,得到白术饮片共有峰指纹图谱(R),每批样品与R比较,计算12批样品的指纹图谱相似度,其相似度在0.972~0.998之间,见表 3。
|
| 1号峰为白术内酯Ⅲ,3号峰为白术内酯Ⅰ 图 1 白术饮片的指纹图谱叠加图和共有峰图谱(R) |
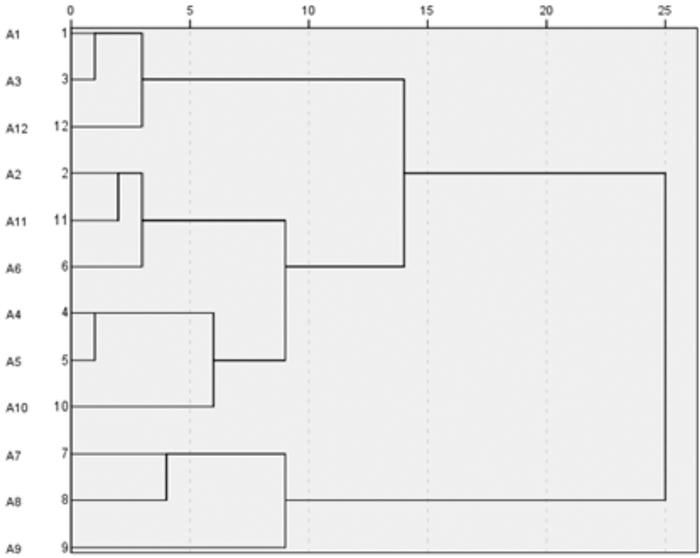
以12批白术饮片中的3种成分含量、10种共有成分的相对峰面积为变量,采用SPSS 22.0统计软件对样品进行聚类分析。采用利差平方和法(Ward法),以欧氏距离平方作为样品测度,聚类树状图见图 2。
|
| 图 2 白术饮片聚类分析 |
由系统聚类树状图可以看出,12批白术饮片样品被分为4类,与白术饮片产地具有较好的一致性,根据聚类分析的结果可大致判断白术饮片的产地。
3 讨论分析4个产地12批次白术饮片中白术内酯Ⅰ、Ⅱ、Ⅲ的含量结果,发现白术内酯的单一成分含量和3个成分总含量的高低顺序具有一致性,各产地饮片中白术内酯含量由高至低依次为浙江、河北、湖南、安徽,而这可能与其产地、生长年限、环境、采收加工等因素有关。
在指纹图谱相似度评价中,4个产地12批次白术饮片指纹图谱与共有峰R图谱的相似度在0.972~0.998之间。其中A8样品(浙江20150701)的相似度最低(0.972),这可能是该样品中白术内酯总量最高所造成的。
在系统聚类分析中,A7~A9样品被分为一类,表明该产地(浙江)白术饮片不同批次之间质量均一性良好,这与其内酯类含量在4个产地中最高的含量测定结果和最低的指纹图谱相似度结果相一致。而A4与A5、A1与A3各被分至一类,表明这两个产地(安徽、湖南)的白术饮片质量较为均一。
高效液相色谱法含量测定结合指纹图谱分析与系统聚类分析的评价方法,适用于中药质量控制与评价。在本实验中,通过三者结合的方法,在一定程度上表征了不同产地不同批次白术饮片在化学成分方面的共性与差异,并大致区别出了白术饮片的产地,基于三者的综合信息,可以为白术饮片质量控制与评价提供参考。
| [1] |
中华人民共和国药典委员会. 中华人民共和国药典(一部)[M]. 北京: 中国医药科技出版社, 2015: 103-104.
|
| [2] |
Wang C, Duan H, He L. Inhibitory effect of Atractylenolide Ⅰ on angiogenesis in chronic inflammation in vivo and in vitro[J]. Eur J Pharmcaol, 2009, 612(1-3): 143-152. DOI:10.1016/j.ejphar.2009.04.001 |
| [3] |
Dong H, He L, Huang M, et al. Anti-inflammatory components isolated from Atractylodes macrocephala Koidz[J]. Nat Prod Res, 2008, 22(16): 1418-1427. DOI:10.1080/14786410801931629 |
| [4] |
Li N, Xu ZC, Zhang H, et al. New triterpene prosaponin and sapogenin with unsaturated lactone skeleton from gynostemma pentaphfllum and the antitumor activities assay[C]. Proceeding of 2008 international conference on ginseng, 2008.
|
| [5] |
Wang CC, Lin SY, Cheng HC, et al. Pro-oxidant and cytotoxic activities of AtractylenolideⅠin human promyeloleukemic HL-60 cells[J]. Food Chem Toxicol, 2006, 44(8): 1308-1315. DOI:10.1016/j.fct.2006.02.008 |
| [6] |
李培训, 贾英杰, 贾彦焘, 等. 参苓白术汤加减改善胃癌大肠癌术后脾虚证的观察[J]. 天津中医药大学, 2005, 24(3): 151-152. DOI:10.3969/j.issn.1673-9043.2005.03.017 |
| [7] |
孙文平, 李发胜, 侯殿东, 等. 当归、白术、制白附子多糖对小鼠免疫调节作用的影响[J]. 中国中医药信息杂志, 2008, 15(7): 37-38. DOI:10.3969/j.issn.1005-5304.2008.07.017 |
| [8] |
王光伟, 丰昀, 刘永乐, 等. 白术多糖对局灶性脑缺血再灌注大鼠的神经保护作用[J]. 食品科学, 2009, 30(15): 220-222. DOI:10.3321/j.issn:1002-6630.2009.15.052 |
| [9] |
章小莉, 汪林, 徐龙, 等. 白术对人妊娠子宫平滑肌细胞膜钙依赖钾通道电流的影响[J]. 中国妇幼保健, 2009, 24(3): 365-366. |
| [10] |
刘玉强, 才谦. 50批不同来源白术饮片及饮片中白术内酯Ⅰ和白术内酯Ⅲ含量的HPLC法测定[J]. 药物分析杂志, 2012, 32(7): 1249-1250. |
| [11] |
张英丰, 朱黎霞, 梁东辉, 等. HPLC同时测定黄芪白术药对提取物毛蕊异黄酮苷、白术内酯Ⅰ、白术内酯Ⅲ含量[J]. 中国实验方剂学杂志, 2012, 18(9): 86-87. DOI:10.3969/j.issn.1005-9903.2012.09.026 |
| [12] |
陈鸿平, 张杰红, 王晓宇, 等. 土炒对白术中白术内酯Ⅰ、Ⅱ、Ⅲ含量的影响[J]. 中药材, 2011, 34(3): 354-357. |
| [13] |
李羾, 何丹, 杨常成. 高效液相色谱法测定白术中白术内酯Ⅰ、Ⅱ、Ⅲ的含量[J]. 中南药学, 2014, 12(1): 70-71. |
| [14] |
尹华, 王知青, 王玲, 等. HPLC-DAD波长切换法同时测定白术中白术内酯Ⅰ、Ⅱ、Ⅲ和苍术酮的含量[J]. 中华中医药杂志, 2013, 28(1): 233-234. |
 2018, Vol. 37
2018, Vol. 37