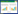文章信息
- 张文杰, 李梦荣, 韩立峰, 郝佳, 刘二伟
- ZHANG Wenjie, LI Mengrong, HAN Lifeng, HAO Jia, LIU Erwei
- “Cocktail”体外探针法评价补骨脂素对人肝微粒体P450酶亚型活性的影响
- Evaluation of the effect of psoralen on human cytochrome P450 subunit activities by Cocktail invitro probe method
- 天津中医药大学学报, 2018, 37(6): 494-499
- Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(6): 494-499
- http://dx.doi.org/10.11656/j.issn.1673-9043.2018.06.13
-
文章历史
收稿日期: 2018-09-05
2. 天津市中药化学与分析重点实验室, 天津 300193
2. Key Laboratory of Pharmacology of Traditional Chinese Medical Formulae, Ministry of Education, Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
补骨脂,蔷薇目豆科植物补骨脂(Psoralea corylifolia L.)的干燥成熟果实,主要含香豆素类、黄酮类、单萜酚类、苯并呋喃类和少量其他成分,其主要成分补骨脂素(PSO)属于呋喃香豆素类化合物,具有治疗白癜风病、拟雌激素效果、抗白血病及抗肿瘤等多种药理作用[1-3],其作为多种中药复方和制剂的主要成分而广泛应用于临床治疗当中。实验证明,PSO能明显抑制肝癌细胞等癌细胞的生长[4],并且对去甲肾上腺素和多巴胺的转运具有抑制作用,可用于注意力缺陷多动障碍、抑郁症、帕金森病等多种疾病的临床治疗[5]。相关实验研究已表明,大鼠在给予补骨脂水煎剂后,检测其血清中的主要活性成分即为PSO[6]。前期药代动力学实验研究发现,雄性大鼠长期服用PSO后能使联合使用的降压药硝苯地平的血药浓度升高,存在联合用药产生的不良反应安全隐患。另有报道称,在雄性小鼠连续28 d服用PSO后,其CYP3A11的活性显著增高,而肝脏中CYP2E1的活性则降低[7]。但PSO对人肝微粒体CYP450酶代谢的抑制和诱导作用的相关研究尚未见报道。
探针药物法,指某些经CYP450代谢的药物,以其代谢物和原型药的比例或速率来衡量酶代谢能力变化的方法[8]。将两种及两种以上经不同酶代谢的药物同时给予的方法被称为“Cocktail ”探针药物法[9],此实验方法因具有经济、快速、简便、有效的特点而备受推崇。作为最重要的药物代谢酶,CYP酶约参与75 %的临床药物的体内代谢,其中介导临床药物代谢的5个主要的CYP同工酶分别为CYP2C9,CYP1A2,CYP2D6,CYP2E1和CYP3A4,而药物在临床上产生代谢性相互作用的主要原因即为其对于CYP酶的诱导和抑制[10-11]。所以,通过加深对中药有效成分对CYP酶的诱导或抑制潜能的研究与了解,可有利于降低临床因药-药相互作用而引起的风险,从而有效提高临床用药的安全性。
呋喃香豆素类化合物与CYP450酶之间具有非常复杂的相互作用,它们通常由CYP酶介导代谢,同时也可反过来对CYP酶的活性进行抑制[12]。
1 仪器与试药 1.1 仪器Waters Acquity H-Class高效液相系统(美国沃特世公司);WatersXevo TQ-S质谱仪(美国沃特世公司);WatersACQUITY UPLC HSS T 3分析柱(2.1 mm×100 mm,1.8 μm)(美国沃特世公司);恒温水浴锅(埃朗科技国际贸易有限公司);超纯水制造机(Millipore公司,Mill-QⅡ型);万分之一天平(德国Sartorius公司,BP121S);十万分之一天平(瑞士Mettler Toledo公司,AX-205);涡旋混合仪(美国LABNET公司,VX-200);超低温冰箱(美国Thermo Heto公司,-70 ℃);低温高速离心机(德国Sigma公司);移液枪(德国Eppendorf公司)。
1.2 试药色谱乙腈、色谱甲醇,德国默克公司;去离子水,美国Millipore公司;PBS溶液(北京索莱宝科技有限公司,PH7.2~7.4);甲酸,美国ACS恩科化学公司;PSO(中国药品生物制品检定所);非那西丁(Phe,CYP1A2的探针),甲苯磺丁脲(Tol,CYP2C9的探针),右美沙芬(Dex,CYP2D6的探针),咪达唑仑(Mdzl,CYP3A4的探针),氯唑沙宗(Chlo,CYP2E1的探针),Sigma-Aldrich;香豆素(Xds,CYP2A6的探针),紫杉醇(Zsc,CYP2C8的探针),中国国家标准物质研究中心;对乙酰氨基酚(Apap,非那西丁代谢产物),4-羟基甲苯磺丁脲(4-OH Tol,甲苯磺丁脲代谢产物),去甲基右美沙芬(Dexde, 右美沙芬代谢产物),α-羟基咪达唑仑(α-OH Mdzl, 咪达唑仑代谢产物),6-羟基氯唑沙宗(6-OH Chlo,氯唑沙宗代谢产物),7-羟基香豆素(7-OH Xds, 香豆素代谢产物),6α-羟基紫杉醇(6α-OH Zsc, 紫杉醇代谢产物),中国药品生物制品检定所;安替比林(ATBL,内标),缬沙坦(XST, 内标),中国国家标准物质研究中心。蒙古人种混合肝微粒体(20 mg/mL),瑞德肝脏有限公司。
2 实验方法与结果 2.1 色谱条件程序洗脱:流动相为乙腈(A),0.1%甲酸水(B);0~10 min,A相3%~100%,10~15 min,A相100%。柱温40 ℃,流速0.4 mL/min;进样量3 μL。
2.2 质谱条件质谱参数为:毛细管电压,3.0 kV(正离子模式),2.5 kV(负离子模式);锥孔电压,30 V;去溶剂化温度,450 ℃;去溶剂气流量,900 L/h(N2,纯度99.9 %);检测模式,多反应检测(MRM)模式; 锥孔电压(CV)和碰撞能量(CE)如表所示,数据采集和数据分析使用Masslynx 4.1和TargetLynx软件完成。
精密称取的各探针代谢产物标准品以甲醇溶液溶解后,用PBS溶液稀释至浓度分别为1、2、5、10、20、50、100、200 ng/mL制成系列混合标准品溶液。精密称取的安替比林和缬沙坦标准品以甲醇溶解,并制成浓度为100 ng/mL的混合内标溶液,于冰箱保存。各底物标准品以甲醇溶解后,用PBS溶液稀释至Phe、Tol、Mdzl、Chlo、Xds、Zsc和Dex最终浓度分别为10、5、5、5、50、10和5 μmol/L,制成混合底物溶液备用。
2.3.2 肝微粒体酶体外孵育体系体外孵化反应体系总体积为175 μL,含有人肝微粒体蛋白(1 mg/mL),混合探针底物溶液,NADPH溶液(5 mg/mL),将反应体系在37 ℃恒温水浴中预孵育10 min后加入25 μL的NADPH溶液作为启动液来启动反应,总孵育体系中甲醇及其他有机试剂的含量不得超过1%[13-14]。37 ℃恒温水浴孵育30 min,最后加入冰内标溶液100 μL终止反应。
2.3.3 样品的制备 2.3.3.1 实验分组设置对照组:肝微粒体50 μL+底物50 μL+PBS溶液50 μL,平行制备六份样品。实验组:肝微粒体50 μL+底物50 μL+PSO溶液50 μL,平行制备6份样品。
2.3.3.2 实验步骤按各分组设置,将150 μL溶液置于EP管中,于肝微粒体酶体外孵育体系中孵育。将样品涡旋2 min,14 000 r/min离心10 min,取上清液置于进样小瓶待检测。以检测所得代谢产物浓度与原底物浓度的比值所得转化率(%)为评价指标。
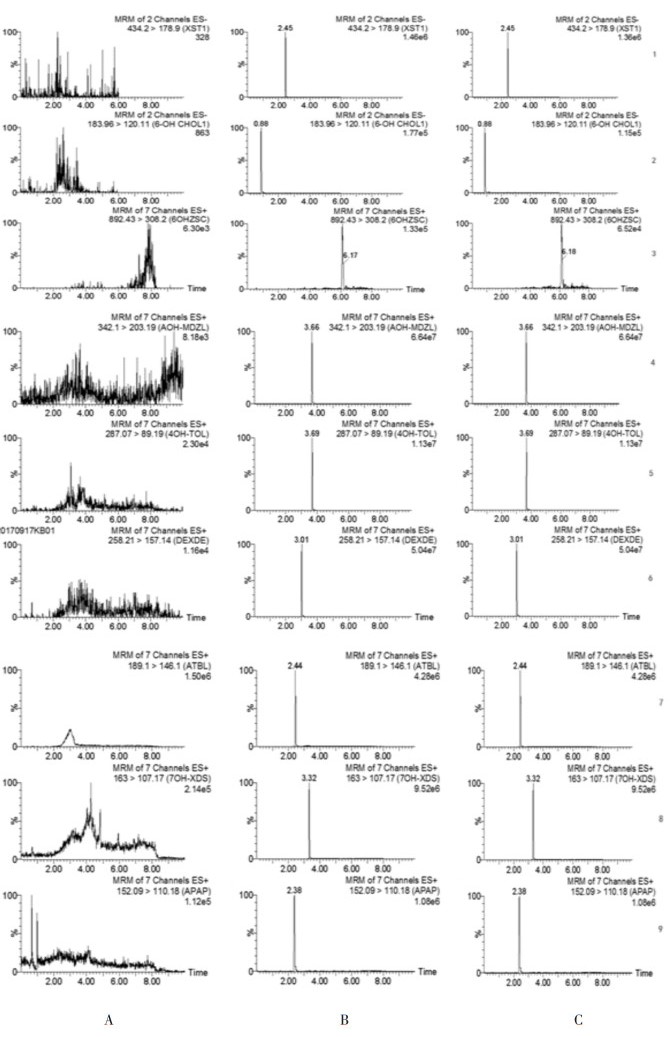
3 结果 3.1 专属性取空白人肝微粒体,加入各代谢产物标准品,按样品制备方法制备专属性考察样品,进样后所得检测结果显示肝微粒体中各种内源性物质对所测的9个化合物没有干扰,不影响结果测定,且各化合物在此条件下测定峰形良好,适合于实验测定,专属性结果见图 1。
|
| 注:1. 6α-OH Zsc;2. α-OH Mdzl;3. 4-OH Tol;4. Dexde;5. ATBL;6. 7-OH Xds;7. Apap;8.XST;9. 6-OH Chlo A:空白组; B:孵育制备后的样品; C:空白肝微粒体中加入产物标准品 图 1 CYP450酶各代谢产物多反映离子检测图 |
将系列混合标准品样品进样检测后,分析各成分与其对应内标物的峰面积比对浓度进行权重系数为1/X的线性回归,得到各成分的线性回归方程,各成分线性回归方程及线性相关系数以及定量限和检测限见表 2。各成分在1~200 ng/mL范围内线性关系良好。
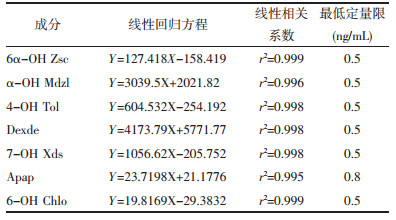
制备人肝微粒体中分别含有低、中、高3个浓度的各代谢产物的混合质控样品,与样品按照相同方法进行处理,每个浓度平行制备6份样品,各样品连续测定3 d,通过标准曲线来计算各成分的精密度和准确度,测定结果显示实验所用方法适合于肝微粒体中各代谢产物成分的检测,精密度与准确度结果见表 3。
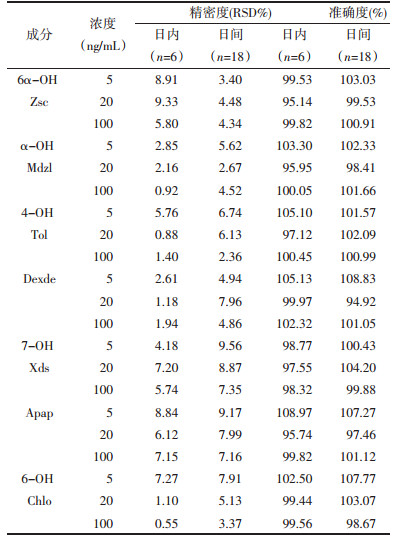
取空白人肝微粒体,配制高、中、低浓度的各代谢产物样品考察其在室温放置4 d、进样器(15 ℃)放置24 h、-20 ℃下放置48 h和-80 ℃下放置7 d以及冻融3次的稳定性,将样品实测值与实际值进行比较,以RSD值小于15%为标准,检测证明稳定性良好,实验结果准确可信,稳定性结果见表 4。
实验建立了LC-MS/MS方法同时检测人肝微粒体中各CYP450酶探针的代谢产物,方法学在生物样品分析方法指导原则下进行了标准曲线、稳定性、专属性、精密度及准确度等内容的全面考察与验证,证明所建立的检测方法灵敏度可靠,符合生物样品测定要求,可用于人肝微粒体中各CYP450酶探针的代谢产物的定量分析。
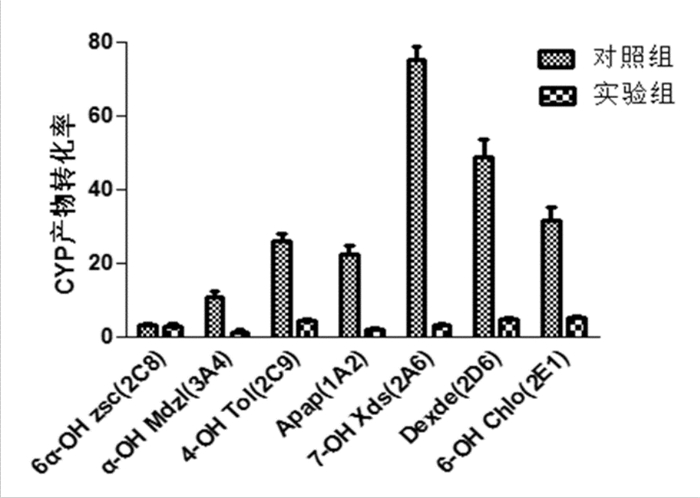
3.6 实验结果照实验分组和步骤制备样品,检测后计算得各组样品中各探针底物转化率(%)实验结果如图 2。
|
| 图 2 各分组CYP450酶代谢产物转化率实验结果 |
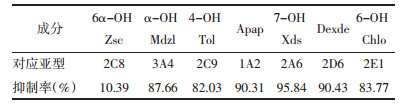
对比实验组与对照组转化率数据,以实验组转化率相对对照组降低的百分比计算补骨脂素对各人肝微粒体P450探针底物转化的抑制率(%)结果见表 5。
由图 2结果可知,与对照组相比,实验组中各探针底物的代谢产物的转化率均下降,说明PSO的加入能使人肝微粒体中Zsc、Mdzl、Tol、Phe、Xds、Dex和Chlo的代谢产物6α-OH Zsc、α-OH Mdzl、4-OH Tol、Apap、7-OH Xds、Dex de和6-OH Chlo的转化减弱。由表 5可知,虽然总体上各人肝微粒体P450酶代谢产物的转化率均下降,但PSO对各亚型的抑制程度并不相同。7种代谢产物中,以7-OH Xds的转化率下降最为显著,PSO对其转化的抑制率为95.84 %,而对6α-OH Zsc的转化的抑制最不明显,仅为10.39 %。PSO对其他几种代谢产物的转化抑制率均在82 %~91 %之间。
4 讨论PSO属于呋喃香豆素类化合物,其代谢主要包括7-羟化、内酯环开环等途径[15]。文献报道,呋喃香豆素类在体内主要经细胞色素P450酶(CYP)代谢并对CYP酶有抑制或诱导作用,应用大鼠肝微粒体研究发现,PSO对CYP1A2有较强的抑制作用[16]。研究显示[17],PSO在肝微粒体系中能够被代谢,PSO容易在肝脏内蓄积,酶亚型2E1、2D6等参与PSO的代谢。
本实验采用“Cocktail”体外探针法,通过PSO与探针药物的竞争性代谢,来研究其对人肝微粒体P450酶中CYP2C9、2D6、3A4、2A6、2E1、1A2和2C8 7种亚型的影响。由实验结果可知,7种代谢产物中,PSO对CYP2A6所对应代谢产物7-OH Xds的转化的抑制程度最强,其次为Apap和Dexde,而对6α-OH Zsc的抑制最不明显。即补骨脂素对CYP2A6亚型的代谢抑制作用最强,其次为CYP1A2和2D6及其他亚型,而对CYP2C8的作用不显著。说明补骨脂素在肝脏的代谢主要通过CYP2A6、1A2和2D6 3种亚型,CYP2C9、3A4和2E1也参与,对CYP2A6、1A2和2D6 3种亚型代谢依赖性药物需关注药物相互作用。硝苯地平为人肝微粒体中CYP3A4亚型的特异性底物[18],其代谢有3A4亚型的参与,故其与补骨脂联合使用时出现的体内药代动力学参数的变化也找到了原因。
联合用药中各药物之间产生代谢性相互作用的原因多为所含的各种有效成分对CYP酶产生诱导或抑制作用,从而造成与其合用药物的药代动力学行为特征的变化。
| [1] |
张红莲, 王雅楠, 王建华. 补骨脂的化学成分及药理活性研究概况[J]. 天然产物研究与开发, 2010, 22(5): 909-913, 918. DOI:10.3969/j.issn.1001-6880.2010.05.039 |
| [2] |
赵丕文, 牛建昭, 王继峰, 等. 6种中药活性成分植物雌激素作用的比较研究[J]. 中国药学杂志, 2007, 42(24): 1852-1855. DOI:10.3321/j.issn:1001-2494.2007.24.004 |
| [3] |
李祝, 宋宝安. 补骨脂素抗肿瘤机理及其应用研究进展[J]. 山地农业生物学报, 2007, 26(3): 255-260. DOI:10.3969/j.issn.1008-0457.2007.03.016 |
| [4] |
吴少华, 张仲海, 赵建斌. 补骨脂素体内外抗癌活性的实验研究[J]. 中国中药杂志, 1998, 23(5): 303-305. DOI:10.3321/j.issn:1001-5302.1998.05.022 |
| [5] |
Zhao G, Li S, Qin G W, et al. Inhibitive effects of Fructus Psoraleae extract on dopamine transporter and noradrenaline transporter[J]. J Ethnopharmacol, 2007, 112(3): 498-506. DOI:10.1016/j.jep.2007.04.013 |
| [6] |
宋殿荣, 宋红运, 王跃飞, 等. 补骨脂水煎液大鼠体内血清药物成分的初步研究[J]. 中华中医药杂志, 2010, 25(11): 1863-1865. |
| [7] |
Wang X, Lou YJ, Wang MX, et al. Furocoumarins affect hepatic cytochrome P450 and renal organic ion transporters in mice[J]. Toxicol Lett, 2012, 209(1): 67-77. DOI:10.1016/j.toxlet.2011.11.030 |
| [8] |
刘高峰, 甄立棉, 杨芳. Cocktail探针药物法在中药细胞色素P450酶代谢研究中的应用[J]. 医药导报, 2009, 28(8): 1049-1052. DOI:10.3870/yydb.2009.08.028 |
| [9] |
刘颖, 焦建杰, 娄建石. "Cocktail"探针药物法的研究进展[J]. 中国临床药理学与治疗学, 2006, 11(11): 1225-1229. DOI:10.3969/j.issn.1009-2501.2006.11.005 |
| [10] |
Fowler S, Zhang H. In vitro evaluation of reversible and irreversible cytochrome P450 inhibition:current status on methodologies and their utility for predicting drug-drug interactions[J]. AAPSJ, 2008, 10(2): 410-424. DOI:10.1208/s12248-008-9042-7 |
| [11] |
艾常虹, 孙汉雄, 李桦, 等. 中药有效成分对细胞色素P450酶的抑制活性评价[J]. 中国药理学通报, 2011, 27(4): 519-523. DOI:10.3969/j.issn.1001-1978.2011.04.019 |
| [12] |
杨少林, 熊友健, 方平飞, 等. 呋喃香豆素类化合物对CYP450酶系影响的研究进展[J]. 中南药学, 2011, 9(1): 45-49. DOI:10.3969/j.issn.1672-2981.2011.01.015 |
| [13] |
Chauret N, Gauthier A, Nicoll-Griffithd A. Effect of common organic solvents on invitro cytochrome P450-mediated metabolic activities in human liver microsomes[J]. Drug Metab Dispos, 1998, 26(1): 1-4. |
| [14] |
Busbyw FJR, Ackermann JM, et al. Effect of methanol, ethanol, dimethyl sulfoxide, and acetonitrile on invitro activities of cDNA-expressed human cytochromes P-450[J]. Drug Metab Dispos, 1999, 27(2): 246-249. |
| [15] |
Regueiro J, Vallverdú-Queralt, Negreira N, et al. Identification and quantification of grape fruit juice furanocoumarin metabolites in urine:an approach basedon ultraperformance liquid chromatography coupledto linear ion trap-orbitrap mass spectrometry and solid -phase xtraction coupled to ultraperformance liquid chromatography coupled to triple quadrupoletandem mass spectrometry[J]. Agric FoodChem, 2014, 62(9): 2134-2140. DOI:10.1021/jf405701a |
| [16] |
Zhuang XM, Zhong YH, Xiao WB, et al. Identification and characterization of psoralen andisopsoralen as potent CYP1A2 reversible and time-dependent inhibitors in human and rat preclinical studies[J]. Drug Metab Dispos, 2013, 41(11): 1914-1922. DOI:10.1124/dmd.113.053199 |
| [17] |
潘建超, 张雯, 李雨昕.补骨脂素的酶代谢亚型研究[R].呼和浩特: 内蒙古中医药, 2014: 44.
|
| [18] |
Patki KC, Von Moltke LC, Greenblatt DJ. In vitro metabolism of midazolam, triazolam, nifedipine, and testosterone by human liver microsomes and recombinant cytochomes P450:role of CYP3A4 and CYP3A5[J]. Drug Metab Dispos, 2003, 31(7): 938-944. DOI:10.1124/dmd.31.7.938 |
 2018, Vol. 37
2018, Vol. 37