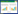文章信息
- 高笑笑, 李霞, 苗静, 宋嬿, 张玉莲, 吕婷婷, 高文远
- GAO Xiaoxiao, LI Xia, MIAO Jing, SONG Yan, ZHANG Yulian, LV Tingting, GAO Wenyuan
- 天麻炮制及其标准饮片的均匀化工艺研究
- Study on processing technology of Gastrodia elata Bl and homogenization technology of its standard pieces
- 天津中医药大学学报, 2018, 37(6): 500-505
- Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(6): 500-505
- http://dx.doi.org/10.11656/j.issn.1673-9043.2018.06.14
-
文章历史
收稿日期: 2018-07-25
2. 上海上药华宇药业有限公司科研管理部, 上海 200002
2. Research management department, Shanghai shangyao Huayu pharmaceutical co., ltd, Shanghai 200002, China
天麻饮片一般是由兰科植物天麻(Gastrodia elata Bl.)的干燥块茎经润切或蒸切两种炮制工艺得到[1-2]。其主要成分有天麻素,对羟基苯甲醇、对羟基苯甲醛和腺苷等[3-5]。目前已有学者对何首乌、制何首乌、槟榔、厚朴、姜厚朴、白附子、丹参、酒丹参等多种饮片进行了均匀化研究,为中药饮片的质量标准研究奠定了基础[6-12]。笔者对润切和蒸切两种炮制工艺进行优化,得到了最佳炮制工艺参数。采用正交试验设计结合综合评分优选出天麻标准饮片的最佳均匀化工艺。为天麻饮片的质量控制的提升以及天麻标准饮片的进一步研究提供参考依据。
1 仪器与试药 1.1 仪器岛津LC-2030高效液相色谱仪,KH-250B型数控超声波清洗器(昆山市禾创超声仪器有限公司),CP225D型Sartorius分析天平(北京赛多利斯仪器系统有限公司),LG-04型四两装高速中药粉碎机(瑞安市百信药机器械厂),RE-200A型旋转蒸发仪(上海亚荣生化仪器厂),SHZ-D(Ⅲ)循环水式真空泵(巩义市英峪仪器厂),Milli-Q超纯水系统(Millipore,Bedford,MA,USA),各种规格筛子。
1.2 试药天麻药材由上海上药华宇药业有限公司提供,均匀化用天麻饮片由天津市中药饮片厂有限公司提供(产地:安徽,批号:G1707152-01),经过天津大学药学院高文远教授鉴定为兰科植物天麻(Gastrodia elata B1.)的干燥块茎。D-无水葡萄糖(中国食品药品检定研究院,110833-201205,99.5%),天麻素对照品(中国食品药品检定研究院,110807-201306,96.8%),对羟基苯甲醇对照品(天津士兰科技有限公司,PCM-DQJ-001,98%)。乙腈为色谱纯,磷酸、乙醇、苯酚及浓硫酸均为分析纯,水为超纯水。
2 方法与结果 2.1 天麻饮片蒸切工艺 2.1.1 生产工艺流程原药材→除杂洗净→蒸透→切薄片→干燥。以天麻素、对羟基苯甲醇、总多糖含量为指标,考察浸泡时间、蒸制时间、干燥温度对天麻的影响,优选出最佳炮制工艺。见表 1。
参照2015版《中国药典》天麻项下天麻素和对羟基苯甲醇总含量测定方法。
2.1.2.2 总多糖含量测定对照品的制备:精密称取105 ℃干燥至恒重的D-无水葡萄糖103.0 mg,置50 mL容量瓶中加蒸馏水至刻度,浓度2.06 mg/mL。
标准曲线的制备:精密吸取标准溶液20,30,40,50,60 μL分别置于具塞试管中各加蒸馏水使体积为1.0 mL,再分别加入5%苯酚试液1.5 mL,摇匀,迅速滴加浓硫酸5.0 mL,摇匀后放置10 min,置沸水浴中15 min,取出,流水冷却至室温,另以蒸馏水1 mL,加苯酚和浓硫酸同上操作为空白试液,于490 nm处测定吸光度,以浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
天麻多糖的提取:分别精密称取天麻饮片粉末0.3 g,置于烧瓶中加95%乙醇100 mL,回流1 h,趁热过滤,残渣用95%热乙醇洗涤3次,残渣连同滤纸置于烧瓶中,加蒸馏水100 mL,加热提取2 h,趁热过滤,残渣用热水洗涤3次,洗涤液并入滤液中,放冷后移入500 mL量瓶,加水至刻度作为天麻多糖提取液,备用。
天麻多糖含量测定:分别精密吸取上述天麻多糖的提取液0.2 mL,置具塞试管中加蒸馏水至1.0 mL,摇匀,分别加入苯酚溶液1.5 mL,摇匀后迅速滴加浓硫酸5.0 mL,摇匀后放置10 min,置沸水浴中加热15 min,取出,每种方法提取液平行3次显色,分光光度法于490 nm处测定吸光度,按照标准曲线计算总多糖含量。
2.1.2.3 测定结果以天麻素、对羟基苯甲醇总含量为指标,各因素对其影响大小为:干燥温度>蒸制时间>浸泡时间,最佳炮制工艺为A1B2C2,即浸泡0 h,蒸制2.5 h,切片后于60 ℃烘干;以总多糖含量为指标,各因素对其影响大小为:浸泡时间>蒸制时间>干燥温度,最佳炮制工艺为A2B3C1,即浸泡3 h,蒸制3 h,切片后于40 ℃烘干;以综合评价指标(0.5×天麻素对羟基苯甲醇总含量+0.5×总多糖含量)为指标,各因素对其影响大小为:浸泡时间>蒸制时间>干燥温度,最佳炮制工艺为A2B3C1,即浸泡3 h,蒸制3 h,切片后于40 ℃烘干。结果见表 2。
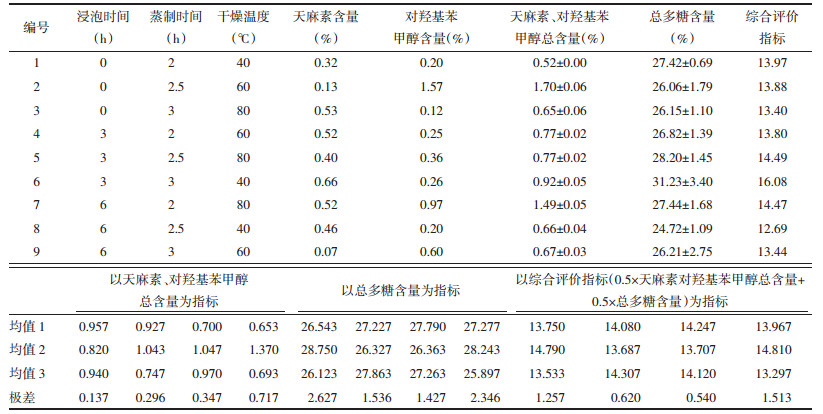
按照最佳炮制工艺,制备3批天麻饮片,测定天麻素、对羟基苯甲醇总含量和总多糖含量。验证实验结果表明,优选的炮制工艺稳定、可行。因此,天麻蒸切工艺的最佳炮制工艺为:取天麻药材,浸泡3 h,蒸制3 h,切片后于40 ℃烘干。结果见表 3。
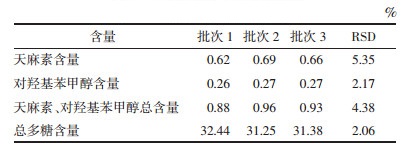
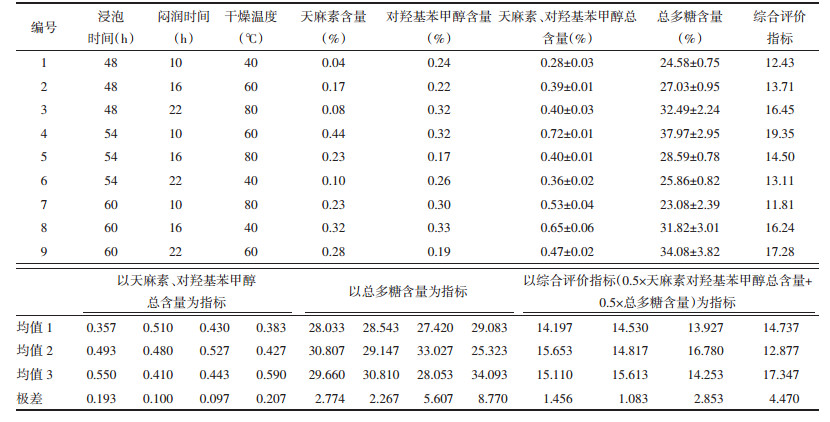
原药材→除杂洗净→浸泡→润透→切薄片→干燥。以天麻素、对羟基苯甲醇、总多糖含量为指标,考察浸泡时间、闷润时间、干燥温度对天麻的影响,优选出最佳炮制工艺。见表 4。
同“2.1.2.1”部分。
2.2.2.2 总多糖含量测定同“2.1.2.2”部分。
2.2.2.3 测定结果以天麻素、对羟基苯甲醇总含量为指标,各因素对其影响大小为:浸泡时间>闷润时间>干燥温度,最佳炮制工艺为A3B1C2,即浸泡60 h,闷润10 h,切片后于60 ℃烘干;以总多糖含量为指标,各因素对其影响大小为:干燥温度>浸泡时间>闷润时间,最佳炮制工艺为A2B3C2,即浸泡54 h,闷润22 h,切片后于60 ℃烘干;以综合评价指标(0.5×天麻素对羟基苯甲醇总含量+0.5×总多糖含量)为指标,各因素对其影响大小为:干燥温度>浸泡时间>闷润时间,最佳炮制工艺为A2B3C2,即浸泡54 h,闷润22 h,切片后于60 ℃烘干。结果见表 5。
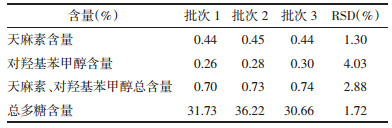
按照最佳炮制工艺,制备3批天麻饮片,测定天麻素、对羟基苯甲醇总含量和总多糖含量。验证实验结果表明,优选的炮制工艺稳定、可行。因此,天麻润切工艺的最佳炮制工艺为:取天麻药材,浸泡54 h,闷润22 h,切片后于60 ℃烘干。结果见表 6。
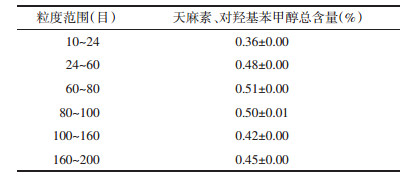
称取均匀化用天麻饮片适量,粉碎,制备不同粒度的标准饮片,采用2015版《中国药典》中天麻项下含量测定方法测定其中的天麻素和对羟基苯甲醇总含量。结果显示,能通过24目筛的粉末所含的天麻素和对羟基苯甲醇总含量相差不大,故筛选出的可作为最佳粒度的天麻标准饮片即为能通过2号筛(24目)的粉末。结果见表 7。
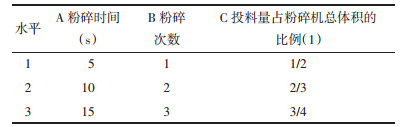
称取天麻饮片适量,用粉碎机进行粉碎,根据最佳粒度筛选结果,以粉碎时间(A)、粉碎次数(B)和投料量(C)为考察因素,选用L9(34)正交设计表。见表 8。
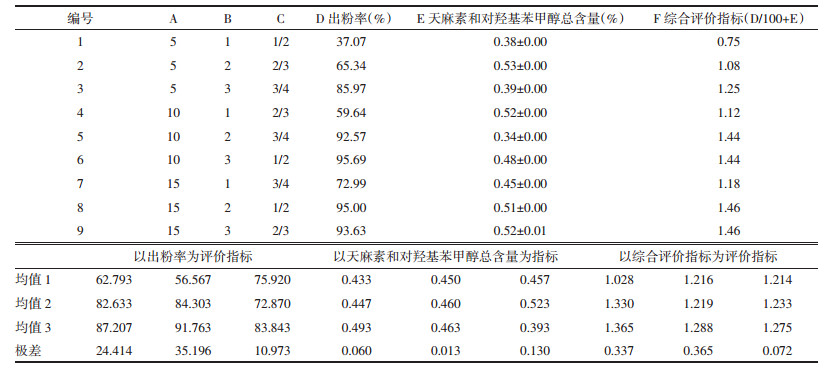
参照2015版《中国药典》天麻项下天麻素和对羟基苯甲醇总含量测定方法,分别对制得的9个粉末进行含量测定。测定结果见表 9。
称取相应质量的天麻饮片,按照正交试验设计方案进行粉碎,将所得粉末过2号筛(24目),可通过的粉末置于一边,未能通过筛网的粉末则返回粉碎机内再次粉碎,试验结束后合并,称量通过2号筛粉末的总重量,记为出粉量,计算出粉率。出粉率=出粉量/天麻饮片量×100%。结果见表 9。
2.3.3.3 综合指标评价由结果可知,各因素对出粉率的影响为B>A>C,即粉碎次数>投料量>单次粉碎时间;各因素对天麻素和对羟基苯甲醇总含量的影响为C>A>B,即投料量>单次粉碎时间>粉碎次数。以综合评价指标进行评价,各因素对其影响为B>A>C,即粉碎次数>投料量>单次粉碎时间,故最佳均匀化制备工艺为A3B3C3,即单次粉碎时间15 s,粉碎3次,投料量为粉碎机总体积的3/4。结果见表 9。
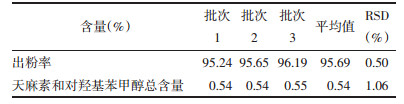
2.3.4 验证试验按上述最佳均匀化制备工艺进行验证,平行实验3次,分别测定出粉率、天麻素和对羟基苯甲醇总含量。验证结果显示,由最佳均匀化制备工艺制备的天麻标准饮片,各指标测定值稳定,RSD值均小于2%,验证了正交试验结果的准确性及所选工艺参数的合理性,表明该均匀化制备工艺稳定可行。见表 10。
2015年版《中国药典》中虽记载了各种中药饮片的炮制方法,却没有明确的工艺参数,例如温度,时间等均会影响到饮片的外观和内在品质。殷放宙等[13]研究了不同炮制温度及时间对栀子和山楂颜色值的影响,结果发现栀子中火及武火炒制的时间为7 min,炒山楂需文火炒制5 min,焦山楂需中火炒制6 min,山楂炭需武火炒制8 min可达到炮制所需的颜色要求。张影月等[14]考察了研究不同炮制时间对杜仲中4个指标成分在大鼠体内药代动力学行为的影响,结果显示炮制2 h杜仲中的主要成分相对于其他炮制时间杜仲在大鼠体内的吸收量有所提高,故杜仲炮制时间宜控制在2 h较为合理。本文考察了浸泡时间,闷润/蒸制时间以及干燥温度对天麻饮片的影响,优化了炮制工艺,明确了两种炮制工艺的参数。两种炮制方法进行比较,发现两种工艺的总多糖含量相差不大,蒸切工艺中天麻素和对羟基苯甲醇的总含量明显高于润切工艺,可能与闷润过程中有效成分在水中流失有关。
粉碎粒度对有效成分的溶出具有一定的影响。丁苗苗等[15]人对西洋参的超微粉和粗粉中人参皂苷Re、Rb1的溶出度进行研究,结果发现超微粉中人参皂苷Rb1的累积溶出度高于粗粉,人参皂苷Re的累积溶出度无显著性差异。笔者考察了不同粒度的天麻标准饮片,通过测定天麻素和对羟基苯甲醇的总含量,筛选出了最佳粒度的天麻标准饮片,保证了有效成分的含量。
出粉率反映了均匀化方法的粉碎效率,正交设计中的3个考察因素均会对其产生影响。中药标准物质不能工业化批量生产,存在供应不足的问题[16-17]。出粉率可作为均匀化制备工艺的一个重要指标,以避免中药标准饮片此后作为标准物质可能出现的供应不足问题。本研究采用正交设计结合综合评分法优选出最佳均匀化工艺,与单一指标评定饮片质量相比,优选出的天麻标准饮片均匀化方法更为合理和全面。
中药饮片的成分复杂,无规范化标准,大多数饮片多参考其药材标准来控制质量,中药标准饮片是衡量中药饮片质量最合适的标准物质[18-20]。本研究为天麻饮片的质量控制提供一种新的更具专属性、科学性的标准物质,可为中药标准饮片的均匀化研究提供参考,进一步提高中药饮片质量控制技术水平。
| [1] |
国家药典委员会.中华人民共和国药典[S].北京: 中国医药科技出版社, 2015.
|
| [2] |
周霞, 万军, 李祖伦, 等.天麻炮制的历史沿革[C].北京: 中华中医药学会中药炮制分会学术会议. 2005.
|
| [3] |
刘思婷, 单鸣秋, 郭舒臣, 等. HPLC法测定市售天麻饮片中6种活性成分的含量[J]. 中国现代中药, 2016, 18(9): 1204-1208. |
| [4] |
杜伟锋, 陈琳, 丛晓东, 等. 天麻化学成分及质量控制研究进展[J]. 中成药, 2011, 33(10): 1785-1787. DOI:10.3969/j.issn.1001-1528.2011.10.037 |
| [5] |
于雪, 胡文忠, 姜爱丽, 等. 天麻的活性成分及功能性研究进展[J]. 食品工业科技, 2016, 37(8): 392-395. |
| [6] |
任晶, 翟文泽, 梁生旺, 等. 何首乌标准饮片均匀化方法研究[J]. 亚太传统医药, 2017, 13(6): 16-19. |
| [7] |
翟文泽, 任晶, 孟江, 等. 制何首乌标准饮片的均匀化工艺研究[J]. 广东药科大学学报, 2017, 33(2): 172-176. |
| [8] |
窦珮丹, 李克宁, 龙琴, 等. 槟榔标准饮片均匀化方法研究[J]. 亚太传统医药, 2017, 13(9): 15-18. |
| [9] |
沈雨.厚朴标准饮片工艺及质量评价指标的研究[D].武汉: 湖北中医药大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10507-1017093709.htm
|
| [10] |
胡慧芬.姜厚朴均匀化饮片的工艺研究[D].武汉: 湖北中医药大学, 2015. http://cdmd.cnki.com.cn/Article/CDMD-10507-1015664928.htm
|
| [11] |
吴娜.白附子对照饮片研究[D].成都: 成都中医药大学, 2016. http://cdmd.cnki.com.cn/Article/CDMD-10633-1017032580.htm
|
| [12] |
付伟.丹参、酒丹参标准饮片的制备技术及其质量评价研究[D].武汉: 湖北中医药大学, 2017. http://cdmd.cnki.com.cn/Article/CDMD-10507-1017093719.htm
|
| [13] |
殷放宙, 吴晓燕, 李林, 等. 炮制火候对饮片颜色的影响[J]. 中草药, 2013, 44(16): 2252-2256. |
| [14] |
张影月, 韩亚亚, 郝佳, 等. 炮制时间对杜仲指标成分含量及药代动力学影响研究[J]. 天津中医药大学学报, 2016, 35(5): 322-326. |
| [15] |
丁苗苗, 杨凯伦, 王东亮, 等. 超微粉碎对西洋参中人参皂苷体外溶出的影响研究[J]. 天津中医药大学学报, 2016, 35(5): 327-331. |
| [16] |
马玲云, 马双成. 中药标准物质的发展现状与展望[J]. 中国药事, 2010, 24(12): 1232-1235. |
| [17] |
张琪, 叶晨, 王丽, 等. 中药对照药材粉碎的经验总结及方法探究[J]. 中国药事, 2013, 27(12): 1301-1304. |
| [18] |
肖永庆, 李丽, 刘颖. 加快中药标准饮片作为标准物质的研究[J]. 中国中药杂志, 2014, 39(13): 2428-2431. |
| [19] |
李丽, 刘颖, 肖永庆. 中药标准饮片作为标准物质应用若干问题探讨[J]. 北京中医药大学学报, 2015, 38(6): 411-412. DOI:10.3969/j.issn.1006-2157.2015.06.010 |
| [20] |
肖永庆, 李丽, 刘颖. 构建中药饮片质量保障体系的关键问题[J]. 世界科学技术(中医药现代化), 2015, 17(1): 167-172. |
 2018, Vol. 37
2018, Vol. 37