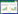文章信息
- 宋洪伟, 毛睿, 李丽红, 王飘, 窦志英, 马琳
- SONG Hongwei, MAO Rui, LI Lihong, WANG Piao, DOU Zhiying, MA Lin
- 延胡索炮制前后多组分质量控制方法的研究
- Study on the method of multi-component quality control before and after processing of corydalis yanhusuo
- 天津中医药大学学报, 2019, 38(1): 63-67
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(1): 63-67
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.01.17
-
文章历史
收稿日期: 2018-10-29
延胡索为罂粟科植物延胡索(Corydalis yanhusuoW. T. Wang)的干燥块茎,是常用理气止痛药[1]。临床常使用炮制品,用于治疗胸肋脘腹疼痛、胸痹心痛。从延胡索中分离得到的生物碱类成分约有30种[2]。单一延胡索乙素很难全面控制药材内部质量,相关的研究中仅对少数几种成分利用HPLC法检测[3-4],其中,罗琛艳[5]用UPLC法对延胡索药材中2种成分进行检测。HPLC多组分成分分析多有报道[6-10]。但该方法耗时长、效率低。因此,基于超高效液相色谱(UPLC)具有快速、分离度高的优点[11-14]。实验从多组分同时把控的角度,建立一种UPLC法同时测定延胡索药材炮制前后8种生物碱含量的方法,该方法操作简便快速,分离度好,为今后延胡索成分含量测定及质量控制标准的提升提供依据。
1 仪器与试药 1.1 仪器UPLC超高效液相色谱仪(安捷伦1290),超声波清洗器KQ-250E(昆山市超声洗器有限公司),数显恒温水浴锅(金坛市科析仪器有限公司),FA2004电子分析天平(上海舜宇恒平科学仪器有限公司);FW100高速万能粉碎机(天津市泰斯特仪器有限公司);离心机(北京时代北利离心机有限公司)。
1.2 试药四氢非洲防己碱(批号:W12N7Z24780),四氢黄连碱(批号:R18A6F2),非洲防己碱(批号:W30M7Z15501),盐酸小檗碱(批号:Y21A7S13543)均购自上海源叶生物科技有限供公司,盐酸巴马汀(批号:110732-201611)购自中国食品药品检定研究院,延胡索乙素(批号:W05-5-8)、去氢紫堇碱(批号:W14-2-4)、原阿片碱(批号:W14-2-6)均购自Zhongxin Innova Laboratories,醋(天津市天立独流老醋股份有限公司),乙腈(默克股份两合公司),甲酸(Anaqua chemicals supply),甲醇(分析纯/天津市化学试剂供销公司),氨水(分析纯/天津市风船化学试剂科技有限公司),蒸馏水(广州屈臣氏食品饮料有限公司),延胡索购于浙江省台州市仙居县朱溪镇,经本校中药鉴定教研室马琳教授鉴定为罂粟科植物延胡索(Corydalis yanhusuoW. T. Wang)的干燥块茎。
2 实验方法 2.1 延胡索样品的制备生品延胡索:按照2015版《中华人民共和国药典》制备。醋煮延胡索:按照2015版《中华人民共和国药典》制备。
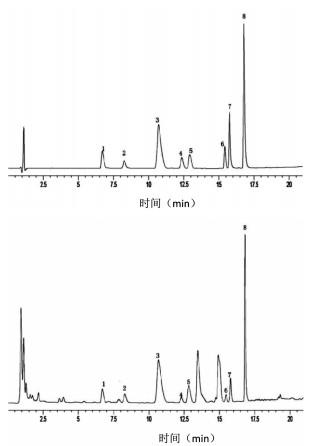
2.2 色谱条件ACQUITY UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm),乙腈(B)-0.2%甲酸水(A)溶液,流速:0.3 mL/min,柱温55 ℃,检测波长280 nm,进样量1 μL;梯度洗脱0~10 min,12%~14%B;10~14 min,14%~25%B;14~17 min,25%~40%B;17~20 min,40%~45%B;20~21 min,45%~12% B。见图 1。
|
| 1.四氢非洲防己碱;2.原阿片碱;3.四氢黄连碱;4.非洲防己碱;5.延胡索乙素;6.盐酸小檗碱;7.盐酸巴马汀;8.去氢紫堇碱 图 1 对照品溶液及延胡索样品UPLC色谱图 |
精密称定四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱分别置于10 mL容量瓶中,用甲醇溶解定容至刻度,得到浓度分别为988、1002、990、988、1004、990、996、1 000 μg/mL的对照品溶液。
量取上述四氢非洲防己碱对照品溶液0.5 mL,原阿片碱对照品溶液0.2 mL,四氢黄连碱对照品溶液1.5 mL,非洲防己碱对照品溶液0.1 mL,延胡索乙素对照品溶液0.5 mL,盐酸小檗碱对照品溶液0.1 mL,盐酸巴马汀对照品溶液0.2 mL,去氢紫堇碱对照品溶液0.5 mL,加甲醇定容至10 mL容量瓶中,配成浓度分别为49.4、20.0、148.5、9.9L、50.2、9.9、19.9、50.0 μg/mL的混合对照品溶液。
2.4 供试品溶液的制备精密称取延胡索样品粉末约0.500 g,置平底烧瓶中,精密加入浓氨试液-甲醇(1:20)混合溶液50mL,称定质量,冷浸1 h后加热回流1 h,放冷,再称定质量,用浓氨试液-甲醇(1:20)混合溶液补足失重,摇匀,4 000 r/min离心15 min,精密量取上清液25 mL,蒸干,残渣加甲醇溶解,转移至5 mL量瓶中,并稀释至刻度,摇匀,滤过,取续滤液,即得。
2.5 方法学考察 2.5.1 线性关系考察分别精密移取四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱储备液适量,用甲醇稀释一系列浓度的对照品溶液,四氢非洲防己碱的浓度分别为98.8、49.4、19.8、9.9、4.0、2.0、0.8、0.4 μg/mL,原阿片碱的浓度分别为100.2、50.1、20.0、10.0、4.0、2.0、0.8、0.4 μg/mL,四氢黄连碱的浓度分别为247.5、123.8、49.5、24.8、9.9、5.0、2.0、1.0 μg/mL,非洲防己碱浓度为49.4、24.7、9.9、4.9、2.0、1.0、0.4、0.2 μg/mL,延胡索乙素浓度为251.0、125.5、50.2、25.1、10.0、5.0、2.0、1.0 μg/mL,盐酸小檗碱浓度为49.5、24.8、9.9、5.0、2.0、1.0、0.4、0.2 μg/mL,盐酸巴马汀浓度分别为99.6、49.8、19.9、10、4.0、2.0、0.8、0.4 μg/mL,去氢紫堇碱浓度分别为250.0、125.0、50.0、25.0、10.0、5.0、2.0、1.0 μg/mL,进样量1 μL,测定峰面积。以峰面积为纵坐标(Y),质量浓度为横坐标(X),绘制标准曲线,回归方程见表 1。
取“2.3”项下混标溶液,在色谱条件“2.2”下,连续进样6针,测定8个生物碱的峰面积并计算RSD。结果显示四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱8种生物碱RSD分别为1.00%、1.92%、0.73%、1.66%、0.95%、1.75%、1.05%、0.80%,表明仪器精密度良好。
2.5.3 稳定性实验取同一供试品溶液,按“2.2”项下色谱条件在0、2、4、8、12、24 h分别进样,记录峰面积并计算RSD。结果显示四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱8种生物碱RSD分别为1.85%、1.83%、1.86%、1.49%、1.60%、1.28%、1.38%、0.29%,表明供试品溶液在24 h内稳定性良好。
2.5.4 重复性实验精密称取同一个样品6份,按“2.4”提取处理方法制备供试品溶液,在“2.2”项下色谱条件进行分析,测定峰面积,计算各对照品的质量分数,结果显示四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱8种生物碱RSD分别为1.52%、1.64%、1.05%、0.81%、1.66%、1.79%、1.94%、1.42%,表明重复性良好。
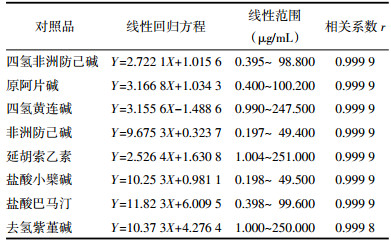
2.5.5 加样回收实验精密称取6份已测知含量的供试品各约0.25 g,如下表加入四氢非洲防己碱、原阿片碱、四氢黄连碱、非洲防己碱、延胡索乙素、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱,按“2.4”项下方法制备供试品溶液,按2.2项下色谱条件下分析。结果见表 2。
采用SPSS 18.0统计软件对数据进行处理和方差分析。
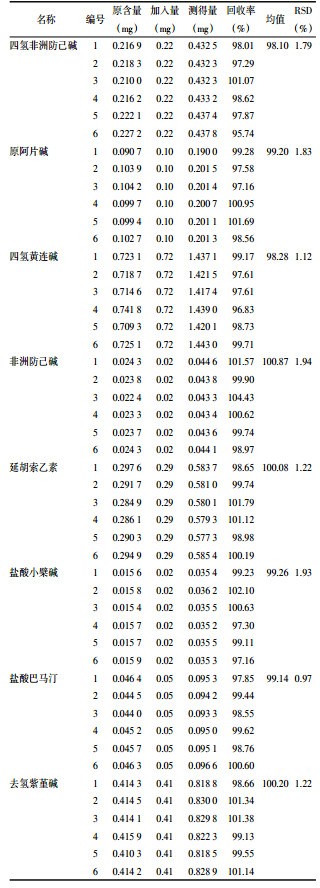
3 样品含量测定精密称取延胡索生品及其炮制品0.500 g,按“2.4”项下方法制备样品,按“2.2”项下色谱条件进行含量测定,计算各成分含量。结果见表 3。
近年来,随着毛细管电泳技术[15]、LC-MS质谱联用[16]等技术的成熟及运用,生物碱的分析方法有了较多的突破,但具体应用在延胡索中的并不太多,目前分析延胡索中生物碱最主要分析方法还是HPLC。多数学者均针对延胡索中延胡索乙素、去氢紫堇碱、四氢黄连碱、小檗碱、巴马汀进行比较研究,而赵新娟[9]等建立了HPLC法测定延胡索中7种异喹啉类生物碱的方法,分析时间为45 min,流动相为乙腈(B)-0.1%醋酸水(三乙胺调pH至5.0)(A),柱温30 ℃。UPLC法具有快捷高效的特点,因此,我们采用UPLC法建立了同时测定延胡索中8种生物碱的方法,分析时间为20 min,缩短了分析时间,提高了分析效率。流动相用量也较HPLC大大减少,减轻了有机试剂的回收的负担和成本。基于超高效液相色谱作为一种高效、精确的分析技术[17],目前已经应用到多种领域[18-19]。该方法从线性、精密度、稳定性、重复性以及加样回收等指标都有较好的对应关系,能够客观、全面评价延胡索生品及其炮制品多种生物碱质量,几种成分的含量较高,也是延胡索生物碱中的主要成分。为完善延胡索药材质量控制提供新技术方法以及科学依据。
流动相中的pH和温度对生物碱的分离度、保留时间影响比较大。在洗脱条件中考察了乙腈-氨水系统,分别加入氨水考察pH值(pH3、3.5、4、5),发现色谱峰拖尾以及基线漂移较严重,随后考察了乙腈-甲酸水系统,分别加入不同浓度的甲酸(0.05%、0.1%、0.15%、0.2%),发现随着酸度浓度增加到0.2%时各组分的峰形及分离度有显著提高。色谱柱温度考察了20 ℃、25 ℃、30 ℃、35 ℃、45 ℃、55 ℃,柱温越高有利于减小柱压,保护色谱柱,同时缩短分析时间,最后选取乙腈-0.2%甲酸水,柱温55 ℃进行分析,通过进一步梯度优化,可将各组分有效的分离。另外,对波长选择时进行全波长扫描,发现在280 nm处,8种生物碱成分吸收和峰形较好且基线比较稳定,故选择280 nm作为检测波长。
延胡索的主要生物碱活性成分为叔胺碱、季胺碱[20-21]。其中四氢非洲防己碱、原阿片碱四氢黄连碱、延胡索乙素属于几乎不溶或难溶于水的叔胺碱;非洲防己碱、盐酸小檗碱、盐酸巴马汀、去氢紫堇碱属于比较易溶于水的季胺碱。由实验结果可知,延胡索叔胺碱经过醋煮炮制后含量比延胡索生品高,由于炮制所用辅料食醋能与延胡索中生物碱结合成盐而增大溶解度,所以提高了生物碱的溶出率[22];延胡索季胺碱经醋煮炮制后含量比延胡索生品低,可能由于易溶于水的季胺碱经醋煮炮制后,生物碱成分分解或破坏。其中,四氢黄连碱含量在炮制前后无显著性差异。2015年版《中华人民共和国药典》规定的延胡索质量标准一般以延胡索乙素的含量为重要指标且不低于0.05%,按此标准,所有样品均符合规定。延胡索的镇痛活性是其所含的多种生物碱共同作用的结果,只对延胡索乙素含量进行控制是不够的,需要尽可能多地表征其他不同生物碱的含量[23]。多种生物碱指标全面评价延胡索药材的质量标准还有待进一步研究。
| [1] |
国家药典委员会.中国药典2015年版(一部)[S].北京: 中国医药科技出版社, 2015: 139-140.
|
| [2] |
贺凯, 高建莉, 赵光树. 延胡索化学成分、药理作用及质量控制研究进展[J]. 中草药, 2007, 38(12): 1909-1912. DOI:10.3321/j.issn:0253-2670.2007.12.050 |
| [3] |
马月光, 岳显可, 曹岗, 等. 不同产地延胡索饮片炮制前后有效成分含量的测定[J]. 中药材, 2013, 36(11): 1754-1758. |
| [4] |
肖辉. 不同炮制方法对延胡索中延胡索乙素含量的影响[J]. 中国药业, 2016, 25(4): 29-31. |
| [5] |
罗琛艳, 李浩, 肖洋, 等. 延胡索药材及饮片UPLC质量控制方法[J]. 天津中医药大学学报, 2015, 34(6): 357-360. |
| [6] |
高建莉, 陈兆飞, 石俊敏, 等. 延胡索中5种生物碱的含量测定及稳定性研究[J]. 中国药房, 2012, 23(15): 1386-1388. DOI:10.6039/j.issn.1001-0408.2012.15.16 |
| [7] |
雷云, 李先端, 杨洪军, 等. 基于成分分析和活性评价的延胡索醋制的研究[J]. 中草药, 2013, 44(21): 2992-2996. |
| [8] |
毕福钧, 林彤. RP-HPLC法同时测定醋延胡索配方颗粒中7种生物碱[J]. 中草药, 2016, 47(4): 606-609. |
| [9] |
赵新娟, 沈梅, 石俊敏, 等. 高效液相色谱法测定延胡索药材中7种异喹啉类生物碱的含量[J]. 天然产物研究与开发, 2015, 27(12): 2074-2078. |
| [10] |
陈东东, 毛坤军, 李祥, 等. HPLC法比较延胡索炮制前后7个生物碱成分的含量[J]. 药物分析杂志, 2015, 35(9): 1591-1595. |
| [11] |
印成霞. 超高效液相色谱法在药物分析中的应用研究[J]. 中国实用医药, 2013, 8(23): 230-231. DOI:10.3969/j.issn.1673-7555.2013.23.185 |
| [12] |
金高娃, 章飞芳, 薛兴亚. 超高速液相色谱在复杂体系中药分离分析中的应用[J]. 世界科学技术中医药现代化, 2006, 8(3): 106-111. |
| [13] |
Wren SAC, Tchelitcheff P. Use of ultra-performance liquidchromatography in pharmaceu tical developm ent[J]. J Chrom atogr A, 2006(1119): 140-146. |
| [14] |
Novakova LM atysova L, Solich P. Advantages of application of UPLC in pharmaceutica lanalysis[J]. Talanta, 2006, 68: 908-918. DOI:10.1016/j.talanta.2005.06.035 |
| [15] |
肖竦. 毛细管电泳测定钩藤中钩藤碱、异钩藤碱、去氢钩藤碱的含量[J]. 现代化工, 2011, 31(8): 90-92. |
| [16] |
沈小月, 宋敏, 杭太俊. LC-MS法鉴定桑叶中生物碱类成分[J]. 药物分析杂志, 2016, 36(10): 1737-1744. |
| [17] |
李翠翠. 超高效液相色谱法在西药分析中的应用探讨[J]. 科学与财富, 2014(4): 361. DOI:10.3969/j.issn.1671-2226.2014.04.331 |
| [18] |
陈静, 郑荣, 季申, 等. 超高效液相色谱法同时测定化妆品中的19种喹诺酮类抗生素[J]. 分析化学研究简报, 2013, 41(6): 931-935. |
| [19] |
张娜, 王国祥, Abacar Jose Daniel, 等. 超高效液相色谱法分析稻米酚酸化合物组分及其含量[J]. 中国农业科学, 2015, 48(9): 1718-1726. |
| [20] |
林武霖, 王如伟, 孙柳燕. 延胡索质量控制的研究进展[J]. 中草药, 2011, 42(2): 409-412. |
| [21] |
吴雪松, 许浚, 张喜民, 等. 元胡止痛方的化学成分及药理作用研究进展[J]. 中草药, 2015, 46(7): 1081-1095. |
| [22] |
窦志英, 孙巍, 田丽莉, 等. HPLC法比较延胡索生品与不同炮制品中3种有效成分的含量[J]. 中药材, 2007, 30(4): 399-401. DOI:10.3321/j.issn:1001-4454.2007.04.009 |
| [23] |
费艳美, 张玉萍, 方步武. 酸性染料比色法测定延胡索总生物碱的含量[J]. 现代中药研究与实践, 2012, 26(3): 66. |
 2019, Vol. 38
2019, Vol. 38