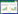文章信息
- 常梦春, 刘静静, 刘勃缨, 任静, 张丽娜, 李佳玮, 刘志东
- CHANG Mengchun, LIU Jingjing, LIU Boying, REN jing, ZHANG Lina, LI Jiawei, LIU Zhidong
- LC-MS/MS法测定升麻葛根汤颗粒在犬体内的药代动力学研究
- Study on the pharmacokinetics of Shengma Gegen decoction granule in beagle dogs by LC-MS/MS
- 天津中医药大学学报, 2019, 38(1): 68-73
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(1): 68-73
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.01.18
-
文章历史
收稿日期: 2018-10-25
2. 天津中医药大学, 天津市现代中药重点实验室-省部共建国家重点实验室培育基地, 天津 300193
2. Tianjin State Key Laboratory of Modern Chinese Medicine, Tianjin 300193, China
升麻葛根汤,方出自宋代阎孝忠的《阎氏小儿方论》,又名平血饮,后被收录于《太平惠民和剂局方》中,是方剂学“辛凉解表剂”的代表方。原方组成为:升麻2 g,葛根3 g,白芍2 g,炙甘草2 g。用法:研成粗末,每服三钱(9 g),水一盏半,煎取一中盏,去滓。具有解肌透疹、辛凉解毒的功效。主治:麻疹初期,疹发不出,身热头痛,咳嗽,目赤流泪,口渴,舌红、苔薄而干,脉浮数[1]。升麻性甘、辛,微寒,归肺、脾、胃、大肠经,具有发表透疹,淸热解毒,升举阳气的功效,为君药;葛根性甘、辛,凉,归脾、胃、肺经,为臣药,与君药升麻合用辛能达表,为透疹解肌之要药;白芍性味苦、酸,微寒,归肝、脾经,养血调经,敛阴止汗,柔肝止痛,平抑肝阳为佐药;炙甘草性味甘,平,归心、肺、脾、胃经,补脾和胃,益气复脉,调和药性,为佐使药[2]。临床升麻葛根汤主要用于治疗乙型、丙型病毒性肝炎、药物性肝病、耳鼻喉科疾病、痘疹未发,或发而不畅等病症[3-9]。
现代药理学研究表明,升麻中有机酸类成分主要有阿魏酸、异阿魏酸,具有抗炎、阵痛的功效[10-12],并以阿魏酸、异阿魏酸为指标控制其质量[13];异黄酮类化合物是葛根的主要活性成分,主要有葛根素、大豆苷、大豆苷元等,其中葛根素是葛根特有成分[14];白芍中主要含有成分为芍药总苷(TGP),包括芍药苷、芍药内酯苷、氧化芍药苷、苯甲酰芍药苷等[15]。TGP具有抗炎、抗溃疡、抗病毒、免疫抑制等多种药理作用,对于类风湿性关节炎、系统性红斑狼疮等疾病有确切的治疗作用[16-17]。本实验建立了液相色谱-质谱联用(LC-MS/MS)的方法测定犬血浆中异阿魏酸、葛根素、芍药苷的血药浓度,并对犬灌胃给予升麻葛根汤颗粒后异阿魏酸、葛根素、芍药苷的药代动力学进行了研究。
1 材料 1.1 仪器与试药液质联用仪(美国Agilent公司,包括1290型高效液相色谱仪、6460型三重四级杆质谱仪,MassHunter工作站);XW-80A型涡旋混合仪(上海沪西分析仪器厂有限公司);XP205型十万分之一天平(METTLER TOLEDO);ST16R型通用台式离心机(美国Thermo公司)。
升麻葛根汤颗粒(批号160503,由深圳华润三九医药股份有限公司提供);异阿魏酸(批号111698-201103,含量以99.2%计,中国食品药品检定研究院);葛根素(批号110752-201514,含量以95.5%计,中国食品药品检定研究院);芍药苷(批号110736-201539,含量以96.4%计,中国食品药品检定研究院);甲苯磺丁脲(批号20160802,Sigma公司);甲醇、乙腈均为色谱纯(购自Fisher Scientific公司);甲酸为色谱纯(购自Fluka公司)。
1.2 实验动物Beagle犬,雌雄各半,体质量10~12 kg,由沈阳军区总院实验动物科提供,许可证号:syxk(军)2012-0022。
2 方法 2.1 标准品溶液的配制精密称取对照品约5.0 mg,加甲醇溶解定容于25 mL量瓶中,得浓度为200 μg/mL的标准品溶液,4 ℃低温保存备用。
2.2 混标溶液的配制精密移取各对照品1 mL置于10 mL量瓶中,加甲醇定溶至刻度,摇晃均匀,得浓度为20 μg/mL的混标溶液,4 ℃低温保存备用。
2.3 内标溶液的配制精密称取甲苯磺丁脲对照品约5.0 mg,加甲醇定容于25 mL量瓶中,得浓度为200 μg/mL的内标溶液,4 ℃低温保存备用。
2.4 色谱条件色谱柱:Waters ACQUITY UPLC® BEH C18柱(2.1 mm×50 mm,1.7 μm,美国Waters公司);柱温:25 ℃;流速:0.2 mL/min;进样量:5 μL;检测波长:320 nm;流动相:0.05%甲酸水(A)-乙腈(B);梯度洗脱(0~2 min,5%B~70%B;2~4.5 min,70%B~100%B;4.5~5.5 min,100%B~100%B;5.5~6 min,100%B~100%B;6~7 min,5%B~5%B)。
2.5 质谱条件离子源:采用电喷雾离子源(ESI源);检测方式:负离子检测;扫描方式:多反应离子监测(MRM);干燥气:N2;干燥气温度:350 ℃;干燥气流量:11 L/min;雾化气压力:15 psi;毛细管电压:3 500 V,具体参数见表 1。
取200 μL血浆加入100 μL内标溶液(甲苯磺丁脲2 μg/mL),加入乙腈1 mL,涡旋5 min,10 000 r/min离心5 min,取1 mL上清液,氮气吹干。加入200 μL甲醇复溶,涡旋5 min,10 000 r/min离心5 min,取上清液进LC-MS/MS分析。
2.7 所用软件(版本)及统计分析方法使用WinNonlin6.4软件的非房室模型计算方法计算药代动力学参数。
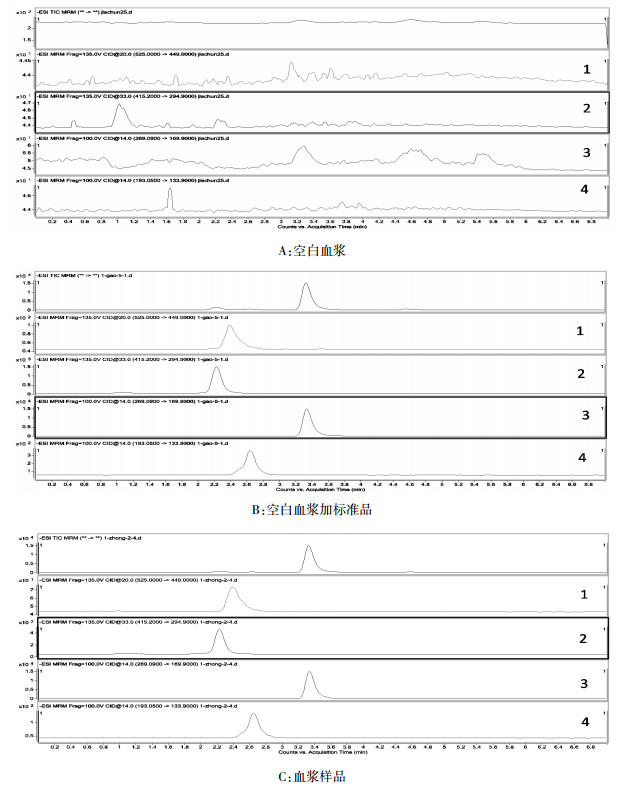
3 结果 3.1 专属性分别取空白血浆、空白血浆加标准品和血浆样品,按照“血浆样品处理方法”处理后进样。结果表明,血浆中的内源性物质不干扰测定。见图 1。
|
| 1.芍药苷;2.葛根素;3.内标;4.异阿魏酸 图 1 犬血浆LC-MS/MS色谱图 |
取混合标准品溶液200 μL,氮气吹干,加入空白血浆200 μL,使芍药苷浓度为4 144、2 072、1 036、518、207.2、103.6、51.8、10.36 ng/mL,葛根素浓度为4 160、2 080、1 040、520、208、104、52、10.4 ng/mL,异阿魏酸浓度为4 240、2 120、1 060、530、212、106、53、10.6 ng/mL,按照“血浆样品处理方法”处理后进样,建立标准曲线。以待测物浓度(ng/mL)为横坐标,待测物与内标物的峰面积比值为纵坐标,用加权(W=1/x)法进行回归运算,求得的直线回归方程即为标准曲线。异阿魏酸回归方程为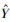
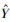
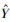
取200 μL混标,氮气吹干,按“血浆样品处理方法”项下的方法分别制备低、中、高3个浓度的质量控制(QC)样品(n=6),所得样品浓度与除用混标复溶,按“血浆样品处理方法”项下的方法分别制备低、中、高3个浓度的质量控制(QC)样品(n=6)浓度相比,测定提取回收率。结果显示该方法的提取回收率均在61.55%±(1.06~81.71)%±2.82之间,RSD<15%符合生物样品测定要求,结果见表 2。
取空白血浆200 μL,除去用混标复溶外,按“血浆样品处理方法”项下的方法分别制备低、中、高3个浓度的质量控制(QC)样品(n=6),所得的峰面积与标准品溶液直接进样所得峰面积相比,测定基质效应,结果显示不存在明显的基质效应,结果见表 2。
3.5 精密度及准确度取空白血浆200 μL,按“血浆样品处理方法”项下的方法分别制备低、中、高3个浓度的质量控制(QC)样品(n=6),在同日内用同一条标准曲线进行处理、分析,得到日内精密度RSD、日间精密度RSD和准确度RE。结果表明4个化合物日内精密度RSD<15%、日间精密度RSD<15%,准确度偏差RE值均在±15%以内,均符合目前生物样品分析方法指导原则的有关规定,结果见表 3。
取空白血浆200 μL,按“血浆样品处理方法”项下的方法分别制备低、中、高3个浓度的质量控制(QC)样品(n=6),考察样品在室温放置24 h(short-term stability)、-20 ℃反复冻融3次(freeze-thaw stability)、-20 ℃冻融30 d(long-term stability)。结果显示4个化合稳定性RE值均在±15%以内,表明芍药苷、葛根素、异阿魏酸在上述条件下可保持稳定,结果见表 4。
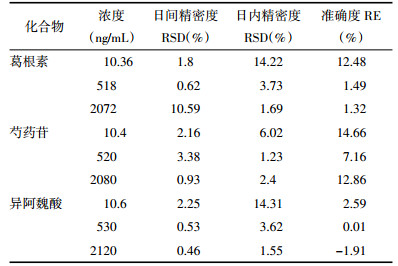
取受试犬6只,给药前禁食12 h,自由饮水。灌胃给予升麻葛根汤颗粒,剂量9 g/只(成人一天给药剂量为9 g)。于给药前0 h及给药后0.5、1、1.5、2、2.5、3、4、5、6、8、10、12、24 h取犬前腿静脉血2.5 mL,置肝素离心管中,3 000 r/min离心10 min,分离血浆至试管中,-80 ℃冷冻待测,作为血浆样品。测定时,取样品血浆按“2.6”项下方法处理,进样测定血药浓度,并计算芍药苷、葛根素、异阿魏酸的血药浓度,绘制平均药时曲线,结果见图 2。

|
| 图 2 犬灌胃给药升麻葛根汤颗粒后芍药苷、异阿魏酸和葛根素血浆药物浓度时间曲线(n=6) |
本实验对血浆样品中3种成分的提取方法进行了考察:甲醇沉淀、乙腈沉淀、乙酸乙酯提取、叔丁基甲醚提取,结果发现乙睛沉淀无内源性物质干扰,重现性好,可达实验测定要求。考察了不同比例甲醇-甲酸水、乙睛-甲酸水及乙睛-甲酸铵、乙睛-乙酸铵作为流动相,发现本实验所建立的流动相梯度洗脱程序能有效地将3个成分和内源性成分分离。
HPLC法同时检测异阿魏酸、葛根素、芍药苷的含量及指纹图谱文献多有报道[18-21],单个化合物的药代动力学也有较多文献研究[22-24],但是3种化合物同时检测未见报道。本文以甲苯磺丁脲为内标物质,采用LC-MS/MS建立了犬灌胃给予中药复方“升麻葛根汤”颗粒后血浆中异阿魏酸、葛根素、芍药苷的含量测定方法,为升麻葛根汤颗粒的质量控制及药理作用研究提供了依据。芍药苷属于苷类、中性化合物,正负离子检测模式均可,本实验通过条件优化结果比较可知,负离子检测模式较好,适合芍药苷的体内分析及药动学研究,具有较好的参考价值。该方法具有较高的专属性、灵敏度,且提取回收率和基质效应、精密度与准确度、稳定性均符合生物样品测定要求。
| [1] |
李冀. 方剂学[M]. 北京: 中国中医药出版社, 2012: 37.
|
| [2] |
国家药典委员会. 中华人民共和国药典(一部)[M]. 北京: 中国医药科技出版社, 2015: 73.
|
| [3] |
董德翠, 王璐瑜. 升麻葛根汤加味治疗带状疱疹后遗神经痛26例疗效观察[J]. 中国民族民间医药, 2009, 18(5): 103-104. DOI:10.3969/j.issn.1007-8517.2009.05.071 |
| [4] |
温红伟, 李岳军. "加味升麻葛根汤"治疗后循环缺血37例临床观察[J]. 江苏中医药, 2010, 42(6): 36-37. DOI:10.3969/j.issn.1672-397X.2010.06.024 |
| [5] |
李秀荣, 李世海, 马琪. 升麻葛根汤合四物汤配合针灸治疗面瘫30例[J]. 甘肃中医, 2011, 24(4): 51. |
| [6] |
张团昌. 升麻葛根汤临床应用举隅[J]. 山西中医学院学报, 2003, 1(4): 36. DOI:10.3969/j.issn.1671-0258.2003.04.021 |
| [7] |
王本祥, 刘媛. 升麻葛根汤在耳鼻喉科的运用[J]. 四川中医, 2002, 20(1): 70. DOI:10.3969/j.issn.1000-3649.2002.01.052 |
| [8] |
李德珍, 安德明, 王抗战, 等. 升麻葛根汤治疗免疫清除期慢性乙型肝炎临床研究[J]. 中西医结合肝病杂志, 2015, 25(2): 90-91. |
| [9] |
李光, 宋德新, 蒋凯. 升麻葛根汤加复方丹参注射液治疗丙肝78例[J]. 河南中医药学刊, 2001, 16(2): 36-37. |
| [10] |
Shiyi Ou, Kin-Chor Kwork. Ferulic acid:Pharmaceutical functions, preparation and applications in foods[J]. Science of Food and Agriculture, 2004, 84(11): 1261-1269. DOI:10.1002/(ISSN)1097-0010 |
| [11] |
韩斐, 王婷. 阿魏酸钠联合贝那普利治疗早期糖尿病肾病的疗效研究[J]. 新疆医科大学学报, 2012, 35(7): 942-945. DOI:10.3969/j.issn.1009-5551.2012.07.019 |
| [12] |
柯雪红, 陈为, 陈锦富, 等. HPLC法测定不同厂家补中益气丸中阿魏酸和异阿魏酸的含量[J]. 安徽医药, 2010, 14(7): 768-770. DOI:10.3969/j.issn.1009-6469.2010.07.011 |
| [13] |
刘颖, 张小茜. 升麻质量标准的研究[J]. 中草药, 2005, 36(9): 126-128. |
| [14] |
陈斌, 刘训红, 蔡宝昌. 葛根高效液相色谱指纹图谱的研究[J]. 时珍国医国药, 2005, 16(5): 384-385. DOI:10.3969/j.issn.1008-0805.2005.05.010 |
| [15] |
Huang TK. Handbook of the Composition and Pharmacology of Common Chinese Drugs[Z].Beijing: China Medico-Pharmaceutical Sciences and Technology Publishing House, 1994, 25(4): 745-749.
|
| [16] |
韩珍, 贺弋. 白芍总苷的药理作用及其毒性研究进展[J]. 宁夏医学院学报, 2008, 30(4): 538-554. DOI:10.3969/j.issn.1674-6309.2008.04.066 |
| [17] |
Kobayashi M, Ueda C, Aoki S, et al. Anticholinergic action Paeony root and its active constituents[J]. Yakugaku-Zasshi, 1990, 110(12): 964. DOI:10.1248/yakushi1947.110.12_964 |
| [18] |
姚少姿, 常梦春, 卢鹏, 等. HPLC法同时测定升麻葛根汤中3个有效成分的含量[J]. 天津中医药, 2017, 34(5): 349-352. |
| [19] |
彭晓一, 可成友, 王立立, 等. HPLC法同时测定升麻葛根汤中四种有效成分的含量[J]. 中国药师, 2010, 13(6): 835-837. DOI:10.3969/j.issn.1008-049X.2010.06.030 |
| [20] |
赵莹莹, 蔡皓, 刘晓, 等. 白芍硫磺熏蒸后导致升麻葛根汤HPLC指纹图谱变化的研究[J]. 南京中医药大学学报, 2014, 30(4): 365-369. |
| [21] |
郭珉, 李珠华, 张志勤, 等. RP-HPLC法同时测定复方升麻颗粒中异阿魏酸、葛根素和芍药苷[J]. 中成药, 2012, 34(6): 1081-1084. DOI:10.3969/j.issn.1001-1528.2012.06.024 |
| [22] |
李煦颖, 赵妍, 王琳, 等. 葛根素及葛根提取物在大鼠体内药代动力学研究[J]. 中国生化药物杂志, 2009, 30(6): 383-386. |
| [23] |
姜清华, 邓晶晶, 吴琼, 等. 芍药苷的药代动力学研究进展[J]. 实用药物与临床, 2010, 13(6): 451-453+478. DOI:10.3969/j.issn.1673-0070.2010.06.025 |
| [24] |
王晓明, 张帆, 刘莹, 等. LC-MS/MS法测定升麻中咖啡酸、阿魏酸、异阿魏酸含量的研究[J]. 天津中医药, 2014, 31(11): 686-689. DOI:10.11656/j.issn.1672-1519.2014.11.13 |
 2019, Vol. 38
2019, Vol. 38