文章信息
- 史文中, 黄培建, 阮静雅, 杨圣财, 王涛, 张祎
- SHI Wenzhong, HUANG Peijian, RUAN Jingya, YANG Shengcai, WANG Tao, ZHANG Yi
- 传统沙生蒙药沙芥的化学成分研究
- Study on the constituents of traditional arenicolous mongolian medicine Pugionium cornutum (L.) Gaerth.
- 天津中医药大学学报, 2019, 38(1): 74-77
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(1): 74-77
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.01.19
-
文章历史
收稿日期: 2018-11-02
沙芥[Pugionium cornutum(L.)Gaerth.]又名沙萝卜、沙盖、山羊沙芥,蒙名额乐森·老邦,主要含有矿物质、糖、微量元素、维生素、氨基酸、黄酮、生物碱和甾醇等化学成分[1],是被《中药大辞典》所收载的植物,具有行气、止痛、消食、解毒,治疗消化不良、胸胁胀满、食物中毒的作用[2];胃功能改善传统药物,它在传统蒙药与方剂中主治头痛、吐泻、胃胀腹痛,是沙区人民喜爱的野菜之一,其风味独特,营养保健价值高,有“沙漠人参”之称[3],并且是蒙古人民千百年来的食材、主治消化不良的药物、防风固沙的先锋植物,其药效物质的研究仍然不够深入,这限制了它的应用和推广。因此,笔者对蒙药沙芥的化学成分进行了初步研究,为其进一步的研究与开发利用提供物质基础。
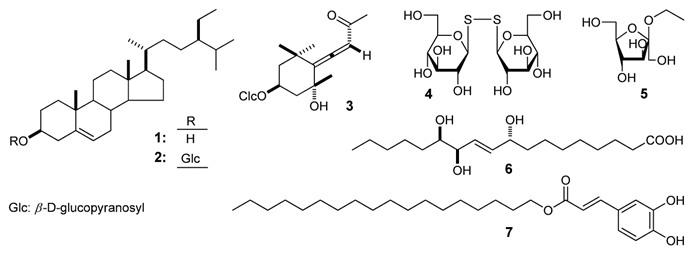
笔者采用多种色谱法相结合,对沙芥干燥根70%乙醇提取物的化学成分进行分离纯化,并利用与文献类似的方法[4-7]鉴定了7个单体化合物的结构,分别为β-谷甾醇(1)、胡萝卜素(2)、staphylionoside D(3)、TgSSTg(4)、乙基-α-D-果糖苷(5)、pinellic acid(6)、Z-咖啡酸硬脂醇酯(7)。其中,化合物3~7为首次从该属植物中分离得到。
1 实验材料与仪器正相柱色谱用硅胶(48~75 μm);ODS(Chromatorex ODS MB,40~75 μm,日本Fuji Silisia Chemical公司);Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司);D101大孔吸附树脂(净品级,天津海光化工有限公司);HPLC用分析柱以及制备柱型号分别为Cosmosil 5C18-MS-Ⅱ(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm,日本Nacalai Tesque公司);氘代试剂(北京崇熙科技孵化器公司)。
实验所用试剂(色谱纯或分析纯)均为天津康科德科技有限公司。
沙芥药材采自内蒙古阿拉善盟,由天津中医药大学李天祥教授鉴定为十字花科沙芥属植物沙芥[Pugionium cornutum(L.)Gaertn.]的干燥根。
2 提取与分离方法沙芥干燥根(4.8 kg)经70% EtOH加热回流提取,得浸膏1 740.0 g。取上述浸膏1 450.0 g溶于10 L水,用EtOAc-H2O(1:1,V/V)萃取,得到EtOAc层、H2O层萃取物分别为153.0 g和1 150.0 g。水层萃取物(1 035.0 g)经D101大孔吸附树脂分离(H2O→95% EtOH→Acetone),得H2O、95% EtOH和Acetone洗脱物各980.0 g、44.1 g和0.8 g。95% EtOH洗脱物(30.0 g)经ODS柱层析[MeOH-H2O(10:90→15:85→30:70→40:60→50:50→70:30,V/V)→MeOH],得8个组分(Fr. 1~Fr. 8)。Fraction 4(9.0 g)经Sephadex LH-20柱层析[MeOH-H2O(50:50,V/V)],得8个组分(Fr. 4-1~Fr. 4-8)。Fraction 4-2(2.0 g)经PHPLC分离制备[CH3CN-H2O(6:94→13:87→15:85,V/V)],得到15个组分(Fr. 4-2-1~Fr. 4-2-15)。Fraction 4-2-9(55.7 mg)经PHPLC分离制备[CH3CN-H2O(9:91,V/V)],得staphylionoside D(3,6.2 mg)。Fraction 5(5.0 g)经ODS柱层析[MeOH-H2O(10:90→20:80→30:70→40:60→50:50→60:40→70:30→80:20→100:0,V/V)],得7个组分(Fr. 5-1~Fr. 5-7)。Fraction 5-2(556.3 mg)经PHPLC分离制备[MeOH-H2O(4:96,V/V)],得TgSSTg(4,54.4 mg)。
EtOAc层萃取物(100.0 g)经硅胶柱层析[CHCl3→CHCl3-MeOH(100:3→100:5,V/V)→CHCl3-MeOH-H2O(10:3:1→7:3:1,下层,V/V)→MeOH],得12个组分(Fr. E 1~Fr. E 12)。Fraction E-3(4.7 g)经硅胶柱层析[石油醚-乙酸乙酯(100:1→50:1→20:1→10:1→5:1→1:1,V/V)],得12个组分(Fr. E-3-1~Fr. E-3-12)。Fraction E-3-10(500.0 mg)经PHPLC分离制备[CH3CN-MeOH(10:90,V/V)],得β-谷甾醇(1,17.9 mg)。Fraction E-5(1.0 g)经硅胶柱分离[CHCl3→CHCl3-MeOH(100:3→100:7,V/V)→CHCl3-MeOH-H2O(20:3:1,下层,V/V)],得到8个组分(Fr. E-5-1~Fr. E-5-8)。Fraction E-5-2(272.0 mg)经PHPLC分离制备(MeOH),得Z-咖啡酸硬脂醇酯(7,13.7 mg)。Fraction E-8(7.0 g)经ODS柱层析[MeOH-H2O(30:70→40:60→50:50→60:40→70:30→80:20→90:10→100:0,V/V)],得到11个组分(Fr. E-8-1~Fr. E-8-11)。Fraction E-8-1(490.0 mg)经PHPLC分离制备[MeOH-H2O(15:85,V/V)],得乙基-α-D-果糖苷(5,12.0 mg)。Fraction E-8-5(195.0 mg)经PHPLC分离制备[CH3CN-H2O(35:65,V/V)],得pinellic acid(6,11.0 mg)。Fraction E-8-10(1 250.0 mg)经硅胶柱层析[CHCl3→CHCl3-MeOH(100:3→100:7,V/V)→CHCl3-MeOH-H2O(20:3:1→6:4:1,下层,V/V)],分离得到8个组分(Fr. E-8-10-1~Fr. E-8-10-8)。Fraction E-8-10-4(92.2 mg)经PHPLC分离纯化(MeOH),得胡萝卜素(2,69.0 mg)。化合物结构如图 1所示。
|
| 图 1 化合物1-7的结构 |
化合物1:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 411.371 5[M-H]-(calcd for C29H47O,411.372 4),确定其分子式为C29H48O。1H NMR(CDCl3,500 MHz)谱数据:δ 0.68、1.01(3H each,both s,H3-18 and 19),0.84、0.82(3H each,both d,J=7.5 Hz,H3-26 and 27),0.85(3H,t,J=6.5 Hz,H3-29),0.92(3H,d,J=6.5 Hz,H3-21),3.52(1H,m,H-3),5.02(1H,dd,J=9.0、15.0 Hz,H-23),5.16(1H,dd,J=8.5、15.0 Hz,H-22),5.35(1H,m,H-6);13C NMR(CDCl3,125 MHz)谱数据:δ 37.3(C-1),31.7(C-2),71.8(C-3),42.4(C-4),140.8(C-5),121.7(C-6),31.9(C-7),31.7(C-8),50.2(C-9),36.5(C-10),21.1(C-11),39.8(C-12),42.4(C-13),56.8(C-14),24.3(C-15),28.3(C-16),56.1(C-17),11.9(C-18),19.4(C-19),36.2(C-20),18.8(C-21),34.0(C-22),26.1(C-23),45.9(C-24),29.2(C-25),19.1(C-26),19.8(C-27),23.1(C-28),12.0(C-29)。其1H、13C NMR谱数据与文献[8]相对照,鉴定该化合物为β-谷甾醇(β-sitosterol)。
化合物2:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 611.407 0[M+Cl]-(calcd for C35H60O6Cl,611.408 4),确定其分子式为C35H60O6。1H NMR(C5D5N,500 MHz)谱数据:δ 0.66、0.93(3H each,both s,H3-18 and 19),0.88、0.85(3H each,both d,J=7.5 Hz,H3-26 and 27),0.90(3H,t,J=7.5 Hz,H3-29),0.99(3H,d,J=6.5 Hz,H3-21),3.93(1H,m,H-3),5.34(2H,t,J=2.0 Hz,H2-6),5.02(1H,d,J=7.5 Hz,H-1’),4.02(1H,dd,J=7.5、8.5 Hz,H-2’),4.26(1H,dd,J=8.5、8.5 Hz,H-3’),4.24(1H,dd,J=8.5、8.5 Hz,H-4’),3.96(1H,m,H-5’),[4.38(1H,dd,J=5.5、12.0 Hz),4.53(1H,dd,J=2.5、12.0 Hz),H-6’];13C NMR(C5D5N,125 MHz)谱数据:δ 37.5(C-1),30.3(C-2),78.1(C-3),39.3(C-4),140.9(C-5),121.9(C-6),32.2(C-7),32.1(C-8),50.4(C-9),36.9(C-10),21.3(C-11),40.0(C-12),42.5(C-13),56.9(C-14),24.5(C-15),28.6(C-16),56.3(C-17),12.0(C-18),19.5(C-19),36.4(C-20),19.1(C-21),34.2(C-22),26.4(C-23),46.1(C-24),29.5(C-25),19.3(C-26),19.8(C-27),23.4(C-28),12.2(C-29),102.6(C-1’),75.3(C-2’),78.4(C-3’),71.7(C-4’),78.6(C-5’),62.8(C-6’)。其1H、13C NMR谱数据与文献[8]相对照,并结合2D NMR谱的解析,鉴定该化合物为胡萝卜素(daucosterol)。
化合物3:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 266.090 4[M+Cl]-,确定其分子式为C19H30O8(calcd for C19H30O8Cl,266.089 5)。1H NMR(CD3OD,500 MHz)谱数据:δ[1.46(1H,dd,J=12.5、14.0 Hz),2.37(1H,ddd,J=3.0、4.0、14.0 Hz),H2-2],[1.47(1H,dd,J=14.0、14.0 Hz),2.09(1H,ddd,J=2.0、4.0、14.0 Hz),H2-4],5.83(1H,s,H-8),2.19(3H,s,H3-10),1.38(3H,s,H3-11),1.16(3H,s,H3-12),1.39(3H,s,H3-13),4.44(1H,d,J=8.0 Hz,H-1’),3.15(1H,dd,J=7.5、8.0 Hz,H-2’),3.34(1H,m,overlapped,H-3’,3.30(1H,m,overlapped,H-4’),3.29(1H,m,overlapped,H-5’),[3.69(1H,dd,J=5.5、11.5 Hz),3.88(1H,dd,J=2.0、11.5 Hz),H2-6’];13C NMR(CD3OD,125 MHz)谱数据:δ37.0(C-1),46.6(C-2),72.5(C-3),48.1(C-4),72.4(C-5),120.0(C-6),211.5(C-7),101.2(C-8),200.8(C-9),26.6(C-10),29.4(C-11),32.3(C-12),30.8(C-13),102.7(C-1’),75.1(C-2’),78.1(C-3’),71.6(C-4’),77.9(C-5’),62.7(C-6’)。其1H、13C NMR谱数据与文献[9]相对照,鉴定该化合物为staphylionoside D。
化合物4:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 391.071 2[M-H]-(calcd for C12H21O10S2,391.072 7),确定其分子式为C12H22O10S2。1H NMR(DMSO-d6,500 MHz)谱数据:δ 4.33(2H,d,J=9.5 Hz,H-1,1’),3.25(2H,dd,J=9.0、9.5 Hz,H-2,2’),3.17(2H,dd,J=9.0、9.0 Hz,H-3,3’),3.08(2H,dd,J=9.0、9.0 Hz,H-4,4’),3.16(2H,m,H-5,5’),[3.44(2H,dd,J=5.5、11.5 Hz),3.69(2H,br. d,ca. J=12 Hz),H2-6,6'];13C NMR(DMSO-d6,125 MHz)谱数据:δ 89.9(C-1,1’),71.9(C-2,2’),77.9(C-3,3’),69.5(C-4,4’),81.1(C-5,5’),61.0(C-6,6’)。其1H、13C NMR谱数据与文献[10]相对照,并结合2D NMR谱的解析,鉴定该化合物为TgSSTg。
化合物5:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 207.086 2[M-H]-(calcd for C8H15O6,207.087 2),确定其分子式为C8H16O6。1H NMR(CD3OD,500 MHz)谱数据:δ[3.63(1H,d,J=12.0 Hz),3.69(1H,d,J=12.0 Hz),H2-1],4.05(1H,d,J=4.5 Hz,H-3),3.90(1H,dd,J=4.5、7.0 Hz,H-4),3.84(1H,ddd,J=2.0、4.0、7.0 Hz,H-5),[3.64(1H,dd,J=2.0、14.0 Hz),3.76(1H,dd,J=4.0、12.0 Hz),H2-6],[3.58(1H,m),3.66(1H,m),-CH2CH3],1.18(3H,t,J=7.0 Hz,-CH2CH3);13C NMR(CD3OD,125 MHz)谱数据:δ 61.6(C-1),109.0(C-2),83.1(C-3),78.6(C-4),84.1(C-5),62.7(C-6),57.7(-CH2CH3),16.0(-CH2CH3)。其1H、13C NMR谱数据与文献[11]相对照,并结合2D NMR谱的解析,鉴定该化合物为乙基-α-D-果糖苷(ethyl-α-D-fructofuranoside)。
化合物6:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 329.233 3[M-H]-(calcd for C18H33O5,329.233 3),确定其分子式为C18H34O5。1H NMR(CD3OD,500 MHz)谱数据:δ 2.24(2H,t,J=7.0 Hz,H2-2),1.58(2H,m,H2-3),4.04(1H,m,H-9),5.67(1H,dd,J=5.5、15.5Hz,H-10),5.70(1H,dd,J=5.5、15.5Hz,H-11),3.89(1H,m,H-12),3.41(1H,m,H-13),0.91(3H,t,J=7.0 Hz,H3-18),1.22~1.70(20H,H2-4~8 and 14~17);13C NMR(CD3OD,125 MHz)谱数据:δ 179.1(C-1),36.0(C-2),26.6(C-3),30.4(C-4),30.5(C-5),30.6(C-6),26.6(C-7),38.4(C-8),73.1(C-9),131.1(C-10),136.6(C-11),76.6(C-12),75.8(C-13),33.6(C-14),26.5(C-15)33.1(C-16),23.7(C-17),14.5(C-18)。其1H、13C NMR谱数据与文献[12]相对照,并结合2D NMR谱的解析,鉴定该化合物为pinellic acid。
化合物7:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 431.317 6[M-H]-(calcd for C27H43O4,431.326 7),确定其分子式为C27H44O4。1H NMR(C5D5N,500 MHz)谱数据:δ 4.29(2H,t,J=7.0 Hz,H2-1),1.67(2H,m,H2-2),1.35(2H,m,H2-3),1.25(2H,m,H2-16),1.23(2H,m,H2-17),0.87(3H,t,J=7.0 Hz,H3-18),7.62(1H,d,J=1.5 Hz,H-2’),7.22(1H,m,overlapped,H-5’),7.20(1H,m,overlapped,H-6’),8.01(1H,d,J=16.0 Hz,H-7’),6.65(1H,d,J=16.0 Hz,H-8’)。13C NMR(C5D5N,125 MHz)谱数据:δ 64.4(C-1),29.2(C-2),26.3(C-3),23.0(C-16),32.1(C-17),14.3(C-18),126.9(C-1’),115.8(C-2’),147.8(C-3’),150.5(C-4’),116.7(C-5’),122.0(C-6’),145.7(C-7’),115.1(C-8’),167.5(C-9’),29.6~30.0(C-4~15)。其1H、13C NMR谱数据与文献[13]相对照,并结合2D NMR谱的解析,鉴定该化合物为Z-咖啡酸硬脂醇酯(Z-octadecyl caffeate)。
4 结论与讨论蒙医药吸收了藏医、汉医及古印度医学理论的精华,逐步发展成具有独特理论体系和临床特点的民族传统医学。蒙医学认为人体的正常生理运动主要依赖于胃和肝脏内精华的分解,保护胃和肝脏消化功能及治疗消化系统疾病是预防与治疗各种疾病的前提。对胃肠道疾病的治疗蒙药有着独特的优势,并积累了丰富的临床经验。
蒙古族药食两用植物沙芥在临床治疗消化不良复方中较为常用,但对其药效物质基础的系统性研究资料尚不多见。本文对沙芥的化学成分进行了系统研究,为其进一步的开发利用提供了物质基础。
| [1] |
Li H, Li C, Zhang C, et al. Compositional and gastrointestinal prokinetic studies of Pugionium (L.)[J]. Food Chem, 2015(186): 285-291. |
| [2] |
江苏新医学院. 中药大辞典[M]. 上海: 上海人民出版社, 1977: 1162.
|
| [3] |
加建斌, 刘晓英. 沙芥的价值及开发与利用[J]. 安徽农学通报, 2007, 13(14): 82-83. DOI:10.3969/j.issn.1007-7731.2007.14.036 |
| [4] |
瞿璐, 刘艳霞, 李建良, 等. 祁菊叶化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2017, 36(1): 57-60. |
| [5] |
董勇喆, 史文中, 杨圣财, 等. 沙葱化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2016, 35(6): 404-408. |
| [6] |
刘丽丽, 李晓霞, 陈玥, 等. 槐米化学成分研究Ⅰ[J]. 天津中医药大学学报, 2014, 33(4): 230-233. |
| [7] |
刘丽丽, 李晓霞, 陈玥, 等. 槐米中酚酸类化学成分研究Ⅰ[J]. 天津中医药大学学报, 2014, 33(1): 39-41. |
| [8] |
施天一, 廖志新, 叶润, 等. 塔黄的化学成分研究[J]. 西北药学杂志, 2014, 29(6): 571-573. DOI:10.3969/j.issn.1004-2407.2014.06.008 |
| [9] |
Yu Q, Matsunami K, Otsuka H, et al. Staphylionosides A-K:megastigmane glucosides from the leaves of Staphylea bumalda DC[J]. Chem Pharm Bull, 2005, 53(7): 800-807. DOI:10.1248/cpb.53.800 |
| [10] |
Shaw CF, Eldridge J, Cancro MP. 13C NMR studies of aurothioglucose:ligand exchange and redox disproportionation reactions[J]. J Inorg Biochem, 1981, 14(3): 267-274. DOI:10.1016/S0162-0134(00)80007-0 |
| [11] |
黄娟娟, 胡长鹰, 潘慧芳. 番木瓜中糖类成分的纯化与鉴定[J]. 食品科学, 2011, 32(13): 89-151. |
| [12] |
Hong SS, Oh JS. Inhibitors of antigen-induced degranulation of RBL-2H3 cells isolated from Wheat Bran[J]. J Korean Soc Appl Biol Chem, 2012, 55(1): 69-74. DOI:10.1007/s13765-012-0012-5 |
| [13] |
孟凡成, 王磊, 张健, 等. 云南黄连中非生物碱类化学成分的研究[J]. 中国药科大学学报, 2013, 44(4): 307-310. |
 2019, Vol. 38
2019, Vol. 38