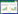文章信息
- 陈慧洁, 杨亚楠, 丁辉, 李薇, 余河水, 宋新波, 张丽娟
- CHEN Huiji, YANG Yanan, DING Hui, LI Wei, YU Heshui, SONG Xinbo, ZHANG Lijuan
- 养阴利咽半生制剂袋泡茶的制备及优化
- Preparing and optimizing the medical preparation of the half preparation tea-bag of nourishing yin and relieving sore-throat
- 天津中医药大学学报, 2019, 38(1): 78-83
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(1): 78-83
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.01.20
-
文章历史
收稿日期: 2018-10-21
2. 天津中一制药有限公司, 天津 301617
2. Tianjin Zhongyi Pharmaceutical co. LTD., Tianjin 301617, China
急、慢性咽炎为现代生活的常见病之一,它与咽部异物梗阻、咽痛的虚喉痹有相似的临床表现,为上呼吸道慢性炎症的一部分,病情反复,病程较长,迄今为止,还没有发现针对这种疾病的具体治疗方法[1-3]。为解决此种难治久愈的病症,天津中医药大学名老中医根据多年临床经验在经典利咽名方的基础上,总结出以北沙参、玄参、赤芍等为主要药物的有效利咽的处方,该方立法采用以滋养肺胃阴液为主治本,利咽化痰为辅治标,养阴利咽,达到标本兼治的目的。
中药袋泡茶是在中国散煮和茶剂的基础上结合现代热封纸质茶包工艺制成的一种新剂型,茶剂体积小,携带方便,含生药量大,溶出快,即泡即服,非常适合现代人的生活方式[4-5]。因此,现将该处方经过水提制剂和粉碎颗粒复配,并结合中药制剂和热封纸质茶包工艺制成一种快速、简单、易服的中药医疗制剂—养阴利咽半生制剂袋泡茶[6-8]。笔者通过对养阴利咽半生制剂袋泡茶处方药物的研究,建立了高效液相色谱(HPLC)同时测定本袋泡茶中有效利咽成分黄芩苷、黄芩素、芍药苷、甘草苷、甘草酸铵、牛蒡子苷和补骨脂素等多个指标成分含量的方法[9-11],以有效成分含量和感官评分的综合评审法为评价标准[12-13],优化制备工艺,为进一步研究开发这种新型利咽医疗制剂提供理论依据和参考。
1 仪器与材料 1.1 仪器Waters 2695型HPLC(美国沃特世公司);GL-21M湘仪离心机(湖南湘仪离心机有限公司);AL204型电子天平[梅特勒-托利多仪器(上海)有限公司];KQ2200DB型数控超声波清洗器(昆山超声仪器有限公司);ZDHW型调温电热套(北京中兴伟业仪器有限公司);旋转蒸发仪(上海亚荣生化仪器厂);全自动新型鼓风干燥箱(上海智城分析仪器制造有限公司);中草药粉碎机(天津市泰斯特仪器有限公司);标准筛(上虞市五星冲压筛工具)。
1.2 材料 1.2.1 处方组成处方由12种中药组方而成,处方主要组成为北沙参12 g,牛蒡子10 g,赤芍12 g,黄芩10 g,甘草6 g等。
1.2.2 处方药物北沙参、牛蒡子、赤芍、黄芩、甘草等均由北京同仁堂饮片有限责任公司提供。
1.2.3 化学试剂乙腈(色谱纯,美国Fisher公司);超纯水(美国PALL公司CascadaTM超纯水机);磷酸(分析纯,天津市风船化学试剂科技有限公司);甲醇(色谱纯,美国Fisher公司)。
1.2.4 HPLC对照品补骨脂素(纯度≥98%,批号YJ0731SA14)芍药苷(纯度≥98%,批号NO1129A02)、牛蒡子苷(纯度≥98%,批号NO1026A021)均购自Solarbio公司;黄芩苷(纯度≥98%,批号P16M8F31725)、黄芩素(纯度≥98%,批号P16M8F31725)购于上海源叶生物科技有限公司;甘草苷(纯度≥98%,批号11610-201106)、甘草酸铵(纯度≥93.1%,批号110731-201418)购自中国食品药品检定研究所。
1.2.5 包装材料根据前期实验选用薄滤纸。
2 实验方法 2.1 制备工艺流程养阴利咽半生制剂袋泡茶处方药材经过水提制剂和粉碎颗粒复配,并结合中药制剂和热封纸质茶包工艺成型,制备工艺流程见图 1。筛选制备工艺时首先进行预实验,进行3组单因素实验,单因素分别为粉碎药材与提取药液比例、颗粒粒径和填充量,确定不同水平,然后通过有效成分含量和感官评价,选出最优组合。在进行单因素实验时,袋泡茶浸泡时间为4 min,浸泡温度为85 ℃,加水量为150 mL,通过感官评价比较工艺效果。

|
| 图 1 养阴利咽半生制剂袋泡茶制备工艺流程图 |
牛蒡子有挥发性成分,直接粉碎;甘草含有甘草酸、黄酮等成分,水溶性好,易于溶出且具有较强的粉性;黄芩含有黄芩苷、黄芩素,易溶于水,故作粉碎药材。
2.2.2 粉碎与选粒粉碎药材的颗粒粒径应处于合理范围,不宜过大或过小,过大不利于有效成分的浸出,过小能透过包装袋,悬浮于水溶液中,影响外观及服用[14],根据前期预实验得出粉碎药材的最佳目数为24~60目。
2.3 提取药材预实验 2.3.1 提取药材的选择北沙参为君药含有香豆素类成分溶于沸水;赤芍主要含水溶性苷类成分,如芍药苷,故这几种药材均适于用水提取。
2.3.2 提取条件的选择药材和水的比例(固液比)、提取时间、提取次数均能影响提取药液的质量[15-16],本着节约成本、节能的目的,根据前期实验得出提取的最佳条件为固液比1:14,提取60 min,提取1次。
2.4 粉碎药材和提取药液混合的考察养阴利咽半生制剂袋泡茶需将粉粹药材与提取药液混合,使其充分吸汁后达到混合目的[17]。因此,要考察药粉与药液的混合比例,按固液比(g:mL)1:1.0、1:1.2、1:1.5、1:1.8、1:2.0进行5组平行实验,在进行实验时,其他工艺参数为颗粒粒径为40目,填充量3 g。
2.5 袋泡茶颗粒粒径的考察粒径大小控制在10~80目,因本袋泡茶中结合了中药茶剂和制剂颗粒的工艺,故粒径选择应根据粉碎药材粒径标准[12],因此选取了10、20、40、60、80目5种粒径进行5组平行实验,在进行实验时,其他工艺参数为粉碎药材与提取药液比1:1.5,装入量3 g。
2.6 袋泡茶装入量的考察袋泡茶的装入量不易过大或过小,过大药物浸出量增加影响口感,过小药物浸出量降低,达不到治疗的目的[5]。因此,选择2、2.5、3、3.5、4 g进行5组平行实验,在进行实验时,其他工艺参数为粉碎药材和提取药液比例1:1.5(g:mL),颗粒粒径为40目。
2.7 养阴利咽半生制剂袋泡茶的感官评价参照GB/T 23776-2009《茶叶感官评审方法》和GB/T 24690-2009《袋泡茶》规定[7],并结合养阴利咽半生制剂袋泡茶的特点,对品质特征的标准做了一些修改,以汤色、香气、滋味为因素,具体评分规则见表 1。本实验组织18人组成评定小组,进行感官评定,取平均得分作为最终感官评分。
色谱柱:Accurasil C18色谱柱(4.6 mm×250 mm,5 μm);流动相:乙腈(A)和0.2%磷酸水溶液(B);流速:1.0 mL/min;波长:232 nm;进样量:10 mL;柱温:30 ℃。梯度洗脱程序:0~10 min,10%~20% A;10~18 min,20%~25% A;18~25 min,25%~38% A;25~30 min,38%~43% A;30~40 min,43%~50% A;40~43 min,50%~95% A;理论塔板数按芍药苷峰计算不低于6 000。
2.8.2 对照品和供试品溶液的配制 2.8.2.1 对照品溶液配制分别精密称取芍药苷、甘草苷、补骨脂素、甘草酸、牛蒡子苷、黄芩苷、黄芩素,加甲醇配制成储备液。各储备液浓度分别为芍药苷0.403 mg/mL、甘草苷0.380 mg/mL、补骨脂素0.092 mg/mL、甘草酸0.392 mg/mL、牛蒡子苷0.488 mg/mL,黄芩苷0.097 mg/mL、黄芩素0.653 mg/mL。分别精密吸取各储备液1 mL加甲醇(色谱纯)定容之10 mL容量瓶中,配成混合对照品溶液。
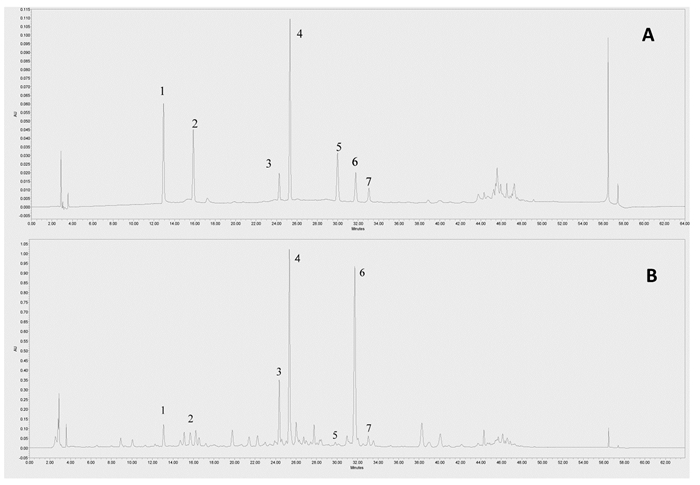
2.8.2.2 供试品溶液配制取3 g袋泡茶样品置于烧杯中,加入180 mL 85 ℃纯水,浸泡30 min;取1 mL样品溶液置于10 mL容量瓶中,加9 mL甲醇后超声30 min,冷却,转移至离心管,室温离心15 min(5 000 r/min),上清液转移至10 mL容量瓶,用90%甲醇定容,摇匀,用0.45 μm微孔滤膜过滤,即得,备用。混合对照品和样品的HPLC色谱图如图 2所示。
|
| 1.芍药苷;2.甘草苷;3.黄芩苷;4.牛蒡子苷;5.补骨脂素;6.黄芩素;7.甘草酸 图 2 混合对照品(A)和样品(B)HPLC色谱图 |
分别精密吸取“2.8.2.2”项下混合对照品溶液,采用逐级稀释法分别用甲醇稀释,配置成5个不同浓度的混合对照品溶液,按“2.8.1”项下的色谱条件,分别进样10 μL,以峰面积为纵坐标,浓度为横坐标,计算回归方程及线性范围,见表 2。由表 2可知:芍药苷、甘草苷、黄芩苷、牛蒡子苷、补骨脂素、黄芩素、甘草酸在以上表中范围内呈现良好的线性关系。
精密吸取“2.8.2.1”项下混合对照品溶液,按“2.8.1”项下色谱条件,连续进样6次,每次进样10 μL,测得芍药苷、甘草苷、黄芩苷、牛蒡子苷、补骨脂素、黄芩素、甘草酸峰面积的RSD%分别为1.17%、1.28%、1.05%、1.37%、1.78%、1.96%、0.51%,表明仪器精密度良好。
2.8.3.3 重复性实验按“2.8.2.2”项下方法制备6份供试品溶液,按“2.8.1”项下色谱条件,各进样10 μL,测得芍药苷、甘草苷、黄芩苷、牛蒡子苷、补骨脂素、黄芩素、甘草酸峰面积的RSD%分别为1.35%、0.82%、2.74%、0.95%、0.27%、1.02%、1.16%,表明该方法重复性良好。
2.8.3.4 稳定性实验取“2.8.2.1”项下制备的供试品溶液,按“2.8.1”项下色谱条件,分别在0、2、4、8、12、24 h进样1次,每次进样10 μL,测得芍药苷、甘草苷、黄芩苷、牛蒡子苷、补骨脂素、黄芩素、甘草酸峰面积的RSD%分别为0.53%、0.71%、2.51%、0.87%、2.14%、1.22%、1.21%,表明样品溶液在24 h内稳定性良好。
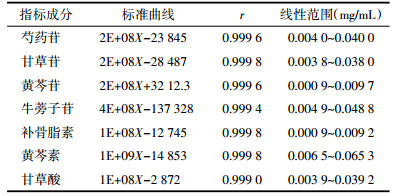
2.8.3.5 加样回收率实验精密称取9份1 g袋泡茶样品,每份样品中精密加入所含芍药苷、甘草苷、黄芩苷、牛蒡子苷、补骨脂素、黄芩素、甘草酸量的80%、100%、120%的对照品。按“2.8.2.1”项下方法制备供试品溶液,按“2.8.1”项下色谱条件进行分析,每次进样10 μL,计算回收率,结果见表 3。
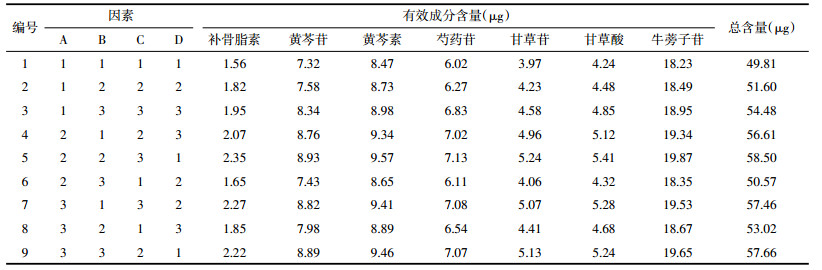
在单因素实验的基础上,考察粉碎药材与提取药液固液比、颗粒粒径、填充量3个因素间的交叉影响,以感官评分与有效成分含量相结合的综合审评法为标准,设计L9(34)正交实验,每组实验测定3次,以其平均值为实验结果。有效成分得分按照最高一组为100分得到各组的相对分值;感官评分按照“2.7”项下方法进行评分;因本品为袋茶饮,经讨论以感官评分为主,有效成分为辅,确定其制备工艺,综合评分得分=有效成分得分×0.4+感官评价得分×0.6。
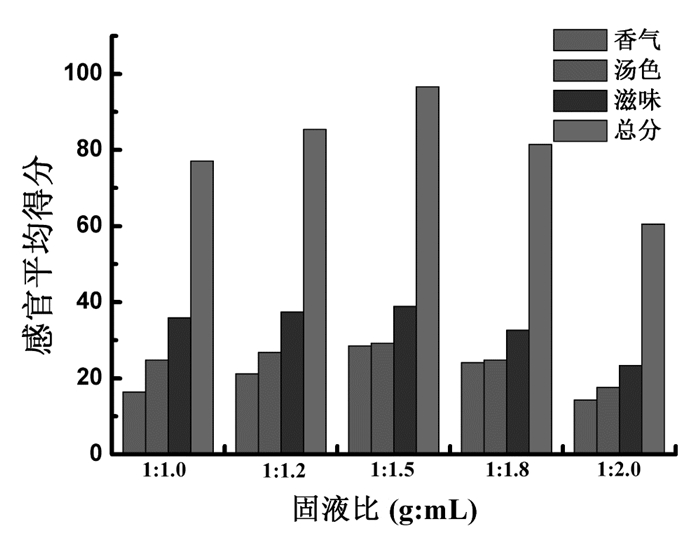
3 结果与分析 3.1 单因素实验结果与分析 3.1.1 粉碎药材与提取药材固液比在袋泡茶颗粒粒径为40目、填充量为3 g的条件下,粉碎药材与提取药材固液比(g:mL)为1:1.0、1:1.2、1:1.5、1:1.8、1:2.0时袋泡茶的感官评定结果见图 3。由图 3可知,在固液比较低时提取药材的有效成分含量不足,袋泡茶的香气偏淡、汤色偏清、滋味偏淡,感官得分降低;在固液比较高时提取药材的有效成分含量过高,袋泡茶的香气浓香、汤色浑浊、滋味浓涩,感官得分降低。综合分析,选择粉碎药材与提取药材固液比(g:mL)为1:1.2、1:1.5、1:1.8进行正交实验。
|
| 图 3 固液比对养阴利咽半生制剂袋泡茶感官评价的影响 |
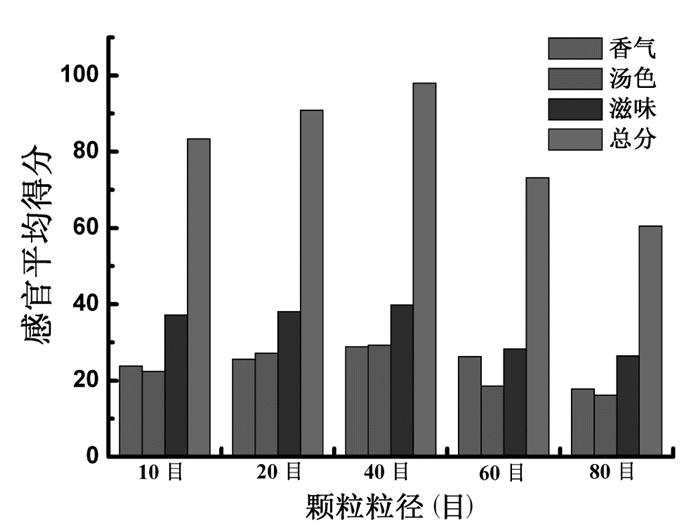
在粉碎药材与提取药液固液比(g:mL)为1:1.5、填充量为3 g的条件下,颗粒粒径为10、20、40、60、80目时袋泡茶的感官评定结果见图 4。当粒径过大,有效成分不容易溶解,粒径过小容易透过包装袋,悬浮于水溶液中,影响外观及服用。粒径在低目数时,袋泡茶香气偏淡、汤色偏清、滋味柔和;粒径在高目数时,袋泡茶香气偏浓、汤色浑浊,有漂浮物、滋味柔和苦涩。综合分析,选择粒径目数为20、40、60目进行正交实验。
|
| 图 4 颗粒粒径对养阴利咽半生制剂袋泡茶感官评价的影响 |
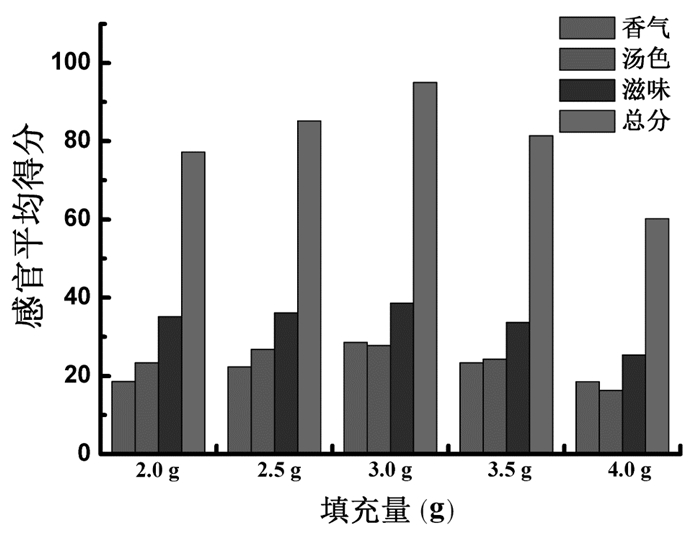
在粉碎药材与提取药液固液比(g:mL)为1:1.5,颗粒粒径为40目的条件下,填充量为2.0、2.5、3.0、3.5、4.0 g时袋泡茶的感官评定结果见图 5。填充量太少,影响口味及治疗效果;填充量太多,容易撑破茶袋,造成溶液浑浊。综合分析,选择2.5、3.0、3.5 g进行正交实验。
|
| 图 5 填充量对养阴利咽半生制剂袋泡茶感官评价的影响 |
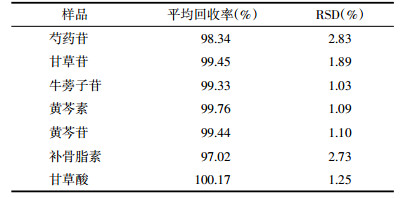
在单因素实验结果的基础上,得出正交实验因素和水平。见表 4。
正交实验各指标含量测定结果见表 5。
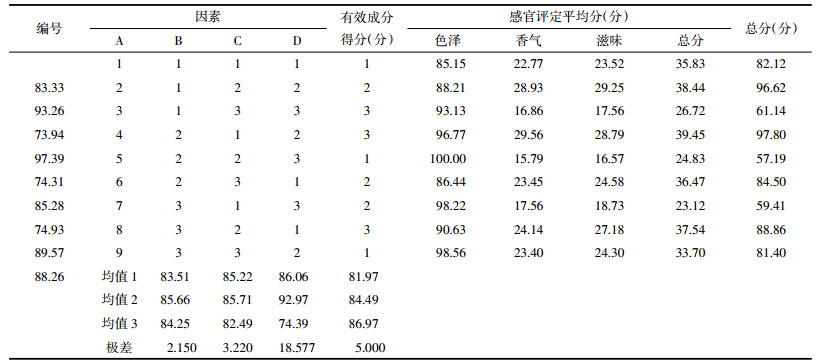
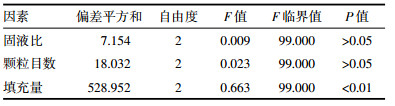
正交实验综合评分结果见表 6。由表 6可知,养阴利咽半生制剂袋泡茶制备工艺影响次序为C(填充量)>B(颗粒粒径)>C(固液比),最佳制备工艺为A3B3C1,即固液比(g:mL)为1:1.8,颗粒粒径为60目,填充量为2.5 g,从方差分析结果见表 7,填充量因素显著,与正交实验结果一致。但考虑到实际生产中粒径太细容易浸出纸袋,造成浪费和溶液浑浊,最终确定工艺为A3B2C1,即固液比(g:mL)为1:1.8,颗粒粒径为40目,填充量为2.5 g。
利用感官评分法和多指标成分含量测定相结合的综合评分法优化了以天津中医药大学名老中医方剂为基础的医疗制剂养阴利咽半生制剂袋泡茶的制备工艺,并结合实际生产经验最终确定养阴利咽半生制剂袋泡茶的最佳制备工艺为A3B2C1,即固液比(g:mL)为1:1.8,颗粒粒径为40目,填充量为2.5 g。本方法全面的优化了这一医疗制剂的制备工艺。
5 讨论本研究根据医疗制剂养阴利咽半生制剂袋泡茶处方中各味中药的理化性质初步制定了工艺流程,建立了多指标成分含量控制的方法[18-20],利用感官评分法和多指标成分含量相结合的综合评分法对其制备工艺进行正交优化,最终确定更优的制备工艺,为本医疗制剂的后期研究以及大生产提供理论依据,并为市场上同类商品的开发提供了方法和参考。
| [1] |
郭建, 郭艳春, 宋宏春. 清凉润喉片提取工艺与成型工艺研究[J]. 临床研究, 2015, 37(3): 258-263. |
| [2] |
刘世端, 蒋学华, 郑琰, 等. 百合固金汤冲剂质量控制方法的研究[J]. 华西药学杂志, 1994, 9(3): 145-148. |
| [3] |
王远.清喉利咽口含片制备工艺及质量标准研究[D].乌鲁木齐: 新疆大学, 2016: 29-32. http://cdmd.cnki.com.cn/Article/CDMD-10760-1016115391.htm
|
| [4] |
朱珍, 吴晖, 安辛欣, 等. 荷叶复合袋泡茶的研制[J]. 食品与机械, 2009, 25(4): 141-159. |
| [5] |
蒋晓峰, 李芳, 任雯雯, 等. 沙棘叶雪菊袋泡茶的研制[J]. 食品工业, 2015, 36(12): 52-55. DOI:10.3969/j.issn.1006-6195.2015.12.017 |
| [6] |
王强.老香黄袋泡茶和老药桔袋泡茶制备工艺的研究[D].乌鲁木齐: 新疆农业大学, 2015: 45-64. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D368585
|
| [7] |
楠极, 李远志, 梁焕秋, 等. 葛根袋泡茶的配方及冲泡参数优化[J]. 食品研究与开发, 2016, 37(13): 56-59. DOI:10.3969/j.issn.1005-6521.2016.13.014 |
| [8] |
张井印, 刘素稳, 常学东, 等. 山楂红枣袋泡茶的工艺优化[J]. 食品研究与开发, 2013, 34(11): 35-38. DOI:10.3969/j.issn.1005-6521.2013.11.009 |
| [9] |
张咪咪.高效液相色谱法在中药复方制剂有效成分含量测定的应用研究[D].延安: 延安大学, 2015: 12-18. http://cdmd.cnki.com.cn/Article/CDMD-10719-1015965523.htm
|
| [10] |
罗有华, 杨辉, 林雪晶, 等. HPCL法同时测定复方板蓝根利咽颗粒中6种成分[J]. 中成药, 2014, 36(7): 1435-1439. DOI:10.3969/j.issn.1001-1528.2014.07.020 |
| [11] |
何俊, 刘华明, 屠亚茹, 等. UPLC-MS/MS法同时测定血必净注射液中15种有效成分的含量[J]. 天津中医药大学学报, 2017, 36(6): 461-465. |
| [12] |
马娟.菏泽颗粒医院制剂的药学研究[D].武汉: 湖北中医药大学, 2016: 11-26. http://cdmd.cnki.com.cn/Article/CDMD-10507-1016226681.htm
|
| [13] |
刘影, 肖洋, 段金芳, 等. 综合加权评分法预测山茱萸饮片有效期[J]. 天津中医药大学学报, 2017, 36(5): 378-381. |
| [14] |
黎东明, 郑国栋, 尹忠平. 松针复合袋泡茶的研制[J]. 食品研究与开发, 2012, 33(4): 128-130. DOI:10.3969/j.issn.1005-6521.2012.04.036 |
| [15] |
李启泉, 赵福兰, 余小飞, 等. 正交试验法优选青诃袋泡茶水提取工艺[J]. 中国药业, 2015, 24(21): 74-76. |
| [16] |
曾菲, 魏芳, 夏道宗. 松针总黄酮提取工艺的优化及复合袋泡茶的研制[J]. 中国食物与营养, 2015, 21(2): 53-56. DOI:10.3969/j.issn.1006-9577.2015.02.014 |
| [17] |
李东波, 周天林. 金菊五加袋泡茶的研制[J]. 甘肃科技, 2015, 31(25): 107-110. |
| [18] |
秦昆明.百合知母汤质量控制及药效物质基础研究[D].南京: 南京中医药大学, 2010: 14-23. http://cdmd.cnki.com.cn/Article/CDMD-10315-2010245110.htm
|
| [19] |
蔡建明.参梅养胃颗粒制备工艺优化及质量标准研究[D].南京: 江苏大学, 2016: 37-53. http://cdmd.cnki.com.cn/Article/CDMD-10299-1016728413.htm
|
| [20] |
张晓雪, 武婕, 余河水, 等. 加味香连丸的质量控制研究[J]. 天津中医药大学学报, 2016, 35(6): 413-416. |
 2019, Vol. 38
2019, Vol. 38