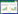文章信息
- 郑路静, 刘庆焕, 陶遵威
- ZHENG Lujing, LIU Qinghuan, TAO Zunwei
- 复方红景天滴丸的制备工艺研究
- Study on the preparation process of compound Rhodiola crenulata dropping pill
- 天津中医药大学学报, 2019, 38(1): 84-87
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(1): 84-87
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.01.21
-
文章历史
收稿日期: 2018-01-05
2. 天津市医药科学研究所, 天津 300020
2. Tianjin Institute of Medical and Pharmaceutical Sciences, Tianjin 300020, China
缺血性脑损伤可导致脑细胞坏死或凋亡,其高致残率、高致死率,给现代家庭与社会带来了沉重的负担[1-2]。随着人们对脑缺血认识的逐渐加深,大量科研数据为改善该病症提供了新的方法与思路。天津市医药科学研究所以“行气活血、化瘀通络”为原则,聚焦缺血性脑损伤“气虚血滞、脉络瘀阻”的病机,组方红景天、延胡索、川芎以及冰片为复方,成为第一个使用该方治疗脑缺血损伤的机构。药理学实验表明红景天复方可减缓海马组织神经细胞凋亡,对脑缺血损伤起到保护作用[3]。本研究对该方的提取及制剂工艺做进一步探究,运用高效液相色谱法(HPLC)技术,以君药中红景天苷的含量及干膏率为综合评价指标,采用正交实验优选复方红景天的醇提工艺,并考察了滴丸的成型工艺,以期为工业化生产提供理论依据。
1 仪器与材料 1.1 仪器高效液相色谱仪(岛津LC-20AT,日本岛津公司),PDA检测器(日本岛津公司),ME203E电子天平(METTLER TOLEDO上海有限公司)。
1.2 材料红景天、延胡索等药材均购自天津市中药饮片厂有限公司,红景天苷对照品购自中国药品生物制品检定所(批号:110818-201005),PEG4000、PEG6000(天津市瑞金特化学品有限公司),二甲基硅油(天津市化学试剂供销公司),甲醇为分析纯。
2 方法与结果 2.1 提取方法按处方比例精密称定各药材,放置圆底烧瓶中,在85℃条件下水浴加热,进行回流提取,收集滤液,测定相关理化指标。
2.2 评价指标的测定 2.2.1 干膏率的测定按处方配比称量各药材9份,根据L9(34)正交实验设计表加乙醇回流,过滤,合并滤液,精密吸取20.0 mL提取液至已干燥恒重的蒸发皿中,蒸干至恒质量,干燥器内冷却,称定干膏质量,计算。
2.2.2 红景天苷含量测定红景天苷检测波长的确定:通过查阅资料,红景天苷(Salidroside)在波长为223、275nm时均存有较强吸收峰[4-5]。实验前期将5 mg红景天苷标准品分别在223、275nm波长下进行检测,结果显示223 nm波长下,红景天苷的峰面积高于275 nm,且杂质干扰少,故本实验在223 nm波长下进行检测。
色谱条件:Agilent ZORBAX Eclipse XDB-C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(85:15);流速:1.0 mL/min;检测波长:223 nm;柱温:室温。
对照品溶液的制备:精密称定13.45 mg红景天苷标准品,置于100 mL量瓶,加70%甲醇溶解,配置成浓度为0.134 5 mg/mL溶液,摇匀,即得。
供试品溶液的制备精密吸取10 mL提取液,转移至蒸发皿,蒸干,加70%甲醇溶解,定容至10 mL,留取续滤液过0.45 μm滤膜,进样,计算含量。
2.2.3 方法学考察线性关系考察:配置系列浓度对照品溶液,进样到液相色谱仪,在上述色谱条件下分析,横坐标为对照品进样量,纵坐标为峰面积积分值,绘制标准曲线,得回归方程Y=1×106X-10 118(r=0.999 7),进样量线性范围0.134~2.69 μg。
精密度实验:取对照品溶液,连续进样6次,得红景天苷峰面积值RSD为0.67%,精密度良好。
稳定性实验:取“2.2.2”项下同一供试品,室温条件下,分别于0、2、4、8、12和24 h进行色谱测定。结果显示,红景天苷含量的RSD为1.90%,表明样品在24 h稳定。
重复性实验:相同条件下,按供试品储备液制备方法平行提取6份,进样测定,记录HPLC图,RSD1.28%,本方法重复性良好。
加样回收率:取6份已知含量的提取液各5 mL,精密量取,分别精密加入配制浓度为215.2 μg/mL的对照品溶液,各5 mL,折合成红景天苷的含量为1.076 mg。按“2.2.2”项下操作方法制备,进行色谱测定,计算平均回收率为100.27%,RSD 1.99%。
2.3 提取工艺设计结合药材性质和参考文献[6-7],确定采用乙醇回流提取,选定影响提取的几个主要因素。实验前期采用单因素实验,对时间、次数、浓度和倍数进行考察。其提取工艺因素与水平设计,见表 1。
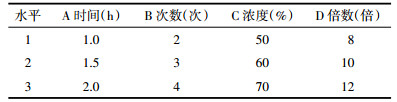
参照文献[8-9]。醇提部分以君药中红景天苷的提出量和干膏率作为考察指标。选用综合加权评分法优选提取工艺,权重系数分别为0.7,0.3,综合评分=(0.7×红景天苷含量/最大红景天苷含量)×100 +(0.3×干膏率/干膏收率最大值)×100。参考单因素的结果,选定影响提取工艺的3个水平(表 1),按照L9(34)表设计安排实验。采用正交实验助手IIV3.1进行正交设计分析,结果见表 2。
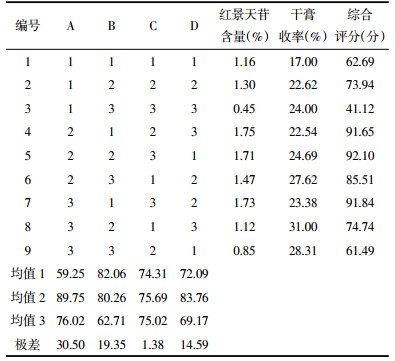
比较各因素的直观分析(见表 2)可知,各影响因素对醇提效果的影响大小为A>B>D>C。方差分析结果,A、B、D因素对提取结果有显著影响,综合极差分析、提取效率、提取成本等考虑,最优工艺确定为A2B1C2D2,即浓度为60%乙醇、10倍量、提取2次,每次1.5 h。
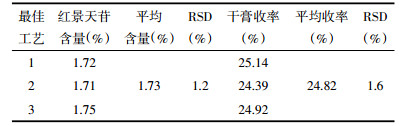
根据正交实验结果,为验证上述最佳工艺的稳定性,按处方称取红景天等药材,分别按优选工艺进行实验。测定两个考察指标,得出红景天苷平均含量为1.73%,RSD=1.2%;测得干膏收率平均值24.82%,RSD=1.6%(n=3)。验证结果显示,依据该实验方法确定的红景天复方醇提工艺合理,且稳定、可行。
2.6 滴丸的制备 2.6.1 冷凝剂的选择分别以二甲基硅氧烷的聚合物(二甲基硅油)、液体石蜡为冷却液,考察冷凝效果。结果表明液体石蜡为冷凝剂,下降快,易粘连,外形不圆整。而二甲基硅油中,滴丸间不粘连,下降速度适中,外形良好、圆整,因此本实验选取的冷凝剂为二甲基硅油。
根据药物性质和基质所特有的内聚力、分散力等理化特点,选用水溶性PEG6000和PEG4000作为制备滴丸所需基质。实验显示,以PEG4000作为滴丸唯一基质时,硬度欠佳,因此加入PEG6000调整,实验以硬度、是否圆整、脱尾情况、滴制的难易、是否漂浮为考察指标,综合考虑,选取PEG40000与PEG6000比例为2:1作为滴丸基质,表 5。
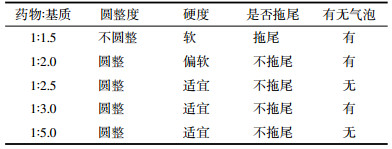
滴丸质量的优劣与载药量密切相关。选取PEG4000与PEG000比例为2:1,其他条件均固定,以软硬程度、是否拖尾、外观圆整度、以及有无气泡为评价标准,考察药基配比对滴丸成型性影响。结果显示,药物与基质选择1:2.5~1:5时滴丸成型性较好。见表 6。
滴丸为近几年中药制剂的新剂型,利用固体分散技术,使药物以分子、微晶或胶体状态分散于基质中,从而更有利于药物的溶解和吸收[10]。而滴丸的制备工艺比较复杂,除受上述冷凝剂、基质配比和载药量影响外,其质量和成型还与多种因素有关,因此想要制成滴丸,很难用单个指标衡量其可行性。本实验后期考察了熔融温度、滴距等因素通过影响滴丸粘连程度、圆整度、拖尾、硬度,结合量化指标丸重差异系数,综合评定制备工艺,并对溶散时限进行了考察。本研究最终选定的制备条件为二甲基硅油,PEG4000与PEG6000的最佳比例为2:1,药基比例1:2.5,滴速30 d/min,滴距4 cm,药液温度80 ℃。
2.6.5 溶散时限检查按照上述操作方法制备滴丸,并根据《中国药典》2015年版(四部),通则0108丸剂的规定进行实验。取3批红景天滴丸供试品,每批6丸,于升降式崩解仪内,不加挡板按崩解时限检查法进行测定,应在30 min内全部溶散。实验过程中3批滴丸溶散时间均小于30 min,表明本实验方法制备的复方红景天滴丸符合检测规定。结果见表 7。
复方红景天组方考究,君药红景天(Rhodiola crenulata)在《本草纲目》中被称为“经中上品”,味甘性寒,主治胸闷、体虚、周身乏力、恶心等症[11-12]。现代科学研究发现,红景天具有延缓衰老、抗肿瘤、抗缺氧及调节人体免疫的功能,并且能够保护脑缺血再灌注损伤[13-14]。川芎能活血、化瘀,止痛、行气。且其行气、活血、止痛的功能与抗脑缺血的作用机制紧密相关。其有效成分川芎嗪能够轻易地透过血脑屏障,从而对脑缺血起到保护作用[15]。冰片与川芎,两者配伍可以增强川芎的药效作用[16]。延胡索具有活血行气,镇痛的作用,治疗血瘀气滞等证,随着现代药理学的深入探究,发现其具有良好的抗脑缺血、抗心肌缺血等作用,其主要成分为延胡索乙素[17-18]。红景天、延胡索、川芎和冰片四味中药合用,探讨其改善脑缺血的作用。
方中君药为红景天,对病症起主要治疗作用,2015年版《中国药典》规定该药材质量的控制指标为红景天苷(Salidroside),因此选取Salidroside为本实验的含量指标性成分。干膏得率对工艺提取具有指标性意义,又是后期制剂成型的重要保障,对剂型的选择、制剂工艺的确定以及给药方案的确定具有重要意义。本实验研究了不同条件下复方红景天的提取效果,并采用正交实验法对提取工艺进行优化选择,并加以验证,所得最佳工艺为:10倍量浓度为60%的乙醇,回流提2次,每次1.5 h。
本实验药方的组建用于改善治疗脑缺血病症,探索其滴丸的制备将有助于各有效成分更加快速的达到血药浓度峰值,发挥其治疗作用。充分体现滴丸快速释药、生物利用度优良等优势,具有一定的临床意义[19]。提高基质与药物比例,可改善滴制溶液粘稠度,使滴丸圆整、不拖尾,增加PEG4000含量可增大药物在基质中的溶解度,减少气泡。基质所含比例高,易于滴出、圆整,成型性优良,考虑到基质与药物比例应尽可能小,增加载药量,确定药物与基质配比为1:2.5。本实验对滴丸进行了初步的探究,可为该组方的进一步开发提供研究基础。
| [1] |
王萍, 张密霞, 庄朋伟, 等. 脑缺血再灌注损伤的炎症反应机制研究进展[J]. 天津中医药大学学报, 2014, 33(5): 317-320. |
| [2] |
Kulik T, Kusano Y, Aronhime S, et al. Regulation of cerebral vasculature in normal and ischemic brain[J]. Neuropharmacol, 2008, 55(3): 281-8. DOI:10.1016/j.neuropharm.2008.04.017 |
| [3] |
王宏, 康利, 刘庆焕, 等. 复方红景天对大鼠缺血性脑损伤后海马组织细胞凋亡的影响[J]. 天津中医药, 2017, 34(8): 554-558. |
| [4] |
薛瑞, 郭东艳. 基于多指标综合评价的红景天提取工艺研究[J]. 西北药学杂志, 2012, 27(5): 407-409. DOI:10.3969/j.issn.1004-2407.2012.05.004 |
| [5] |
刘庆焕, 王宏, 张婷, 等. 多指标正交试验优化复方红景天颗粒的提取工艺[J]. 中国药房, 2017, 28(13): 1830-1833. DOI:10.6039/j.issn.1001-0408.2017.13.29 |
| [6] |
陈小明, 徐超群. 红景天中红景天苷的提取工艺研究[J]. 华西药学杂志, 2010, 25(3): 329-331. |
| [7] |
倪付勇, 陈重, 许琼明, 等. 高山红景天化学成分研究[J]. 中草药, 2013, 44(7): 798-802. |
| [8] |
韩忠耀, 周福军, 刘芳, 等. 多指标综合评分法优选柴胡桂枝颗粒提取工艺[J]. 天津中医药大学学报, 2015, 34(2): 108-111. |
| [9] |
吴月国, 张萍, 赵铮蓉, 等. 红杞胶囊提取工艺的研究[J]. 中国现代应用药学, 2012, 29(10): 910-913. |
| [10] |
吴雪旖, 闫雪生, 赵许杰, 等. 茯苓皮总三萜滴丸制备工艺的优化[J]. 中成药, 2016, 38(4): 934-937. |
| [11] |
贺美艳, 张小龙. 唐古特红景天提取工艺研究[J]. 中国现代应用药学, 2012, 29(6): 495-497. |
| [12] |
蒲位凌, 李文华, 白茹玉, 等. 红景天及其抗炎和抗肿瘤活性成分药理作用研究进展[J]. 天津中医药, 2017, 34(12): 856-859. DOI:10.11656/j.issn.1672-1519.2017.12.18 |
| [13] |
季宇彬, 耿欣, 汲晨锋. 红景天研究进展[J]. 天津中医药, 2007, 24(1): 81-85. DOI:10.3969/j.issn.1672-1519.2007.01.039 |
| [14] |
Zhu Y, Shi YP, Wu D, et al. Salidroside protects against hydrogen peroxide-induced injury in cardiac H9c2 cells via PI3K-Akt dependent pathway[J]. DNA Cell Biol, 2011, 30(10): 809-819. DOI:10.1089/dna.2010.1183 |
| [15] |
金玉青, 洪远林, 李建蕊, 等. 川芎的化学成分及药理作用研究进展[J]. 中药与临床, 2013, 4(3): 44-48. |
| [16] |
万国靖. 中药川芎与冰片配伍使用的研究[J]. 黑龙江医药, 2012, 25(6): 892-894. DOI:10.3969/j.issn.1006-2882.2012.06.035 |
| [17] |
梁健, 王富强, 郑平香, 等. 延胡索乙素抗脂质过氧化作用与对脑缺血再灌注大鼠行为及病理改变的保护[J]. 中国药理学通报, 1999, 15(2): 167-169. DOI:10.3321/j.issn:1001-1978.1999.02.020 |
| [18] |
杨娟, 张莉蓉. 延胡索乙素抗大鼠血栓作用研究[J]. 药学与临床研究, 2012, 20(5): 399-401. DOI:10.3969/j.issn.1673-7806.2012.05.004 |
| [19] |
周礼玲, 张师愚. 双黄连滴丸的最佳制备工艺和溶出时限检查[J]. 天津中医药大学学报, 2007, 26(2): 79-80. DOI:10.3969/j.issn.1673-9043.2007.02.010 |
 2019, Vol. 38
2019, Vol. 38