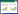文章信息
- 田浩林, 田金洲, 倪敬年, 李婷, 魏明清, 张学凯, 张天清, 周梦玲, 周沪方, 贾冬冬, 魏欣如, 林乐颖, 扎木, 姚璇, 梁俊杰, 时晶
- TIAN Haolin, TIAN Jinzhou, NI Jingnian, LI Ting, WEI Mingqing, ZHANG Xuekai, ZHANG Tianqing, ZHOU Mengling, ZHOU Hufang, JIA Dongdong, WEI Xinru, LIN Leying, ZHA Mu, YAO Xuan, LIANG Junjie, SHI Jing
- 中西医结合治疗帕金森病非运动症状的系统评价与Meta分析
- Integrated traditional Chinese and western medicine for the Non-motor symptoms of parkinson's disease: a systematic review and meta-analysis
- 天津中医药大学学报, 2019, 38(2): 147-154
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(2): 147-154
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.02.12
-
文章历史
收稿日期: 2018-12-11
帕金森病(PD)作为最常见的神经变性疾病之一,目前在发达国家普通人口发病率约0.3%,60岁以上发病率约1.0%,而到了80岁以上发病率则高达3.0%。而中国老年人群PD的患病率与发达国家相近,年龄在65岁以上人群PD发病率为1.7%。2005年,通过2种方法学调查发现在5个欧洲国家及10个人口最多的国家中年龄超过50岁患PD人数达410~460万,而到2030年人数将会翻倍至870~930万人[1-4]。PD是以运动迟缓,僵直,静止性颤抖及姿势平衡障碍作为四大主症,同时可伴有多种非运动症状(如抑郁、痴呆、睡眠障碍、便秘、失眠等)。其非运动症状已经作为一个整体贯穿疾病的各个阶段而成为影响PD病人生活质量的关键因素[5]。而中医药作为目前治疗PD应用最多的替代医学之一,近期临床前研究已经证实其具有神经保护作用[6-7]。因此,为客观评价其疗效,本文对中药在西医基础上治疗PD非运动症状的有效性和安全性进行系统评价与Meta分析,为临床合理用药提供依据和参考。
1 资料与方法 1.1 文献检索依据系统综述和荟萃分析优先报告条目(PRISMA)指导进行。应用计算机检索英文数据库包括Pubmed、Cochrane Library、ClinicalTrials、Embase、Web of science;中文数据库包括CNKI、VIP、CBM、万方数据库。检索时间均为自建库起至2018年07月。其中英文检索词以Parkinson Disease、Medicine,traditional Chinese、Herbal Medicine、Randomized作为主题词,通过Pubmed进行MESH自由词筛选,以确定英文检索条目;中文检索条目为:帕金森病、帕金森氏病、颤证、震颤麻痹、中医、中药、中西医结合、随机。文献检索语言为中文、英文。
1.2 纳入标准 1.2.1 纳入文献研究类型为平行对照的随机对照研究。
1.2.2 研究对象原发性帕金森病病人;年龄20~85岁,性别、种族不限。(帕金森病的诊断可参考任意一个标准如果没有介绍诊断标准,只要文中提到“患者被诊断为PD”也可纳入)。
1.2.3 干预措施两组均在西医治疗基础上,治疗组采用中药治疗或治疗组采用中药治疗同时对照组采用中药安慰剂对照。中药可以是任何剂型,比如汤、散、颗粒、中成药等。
1.2.4 结局指标主要结局指标:帕金森病非运动症状量表(NMs),非运动症状调查问卷(NMS-Quest);次要指标:帕金森病统一症状量表(UPDRSI、Ⅱ),帕金森病问卷39项(PDQ-39);附加指标:汉密尔顿抑郁量表(HAMD),汉密尔顿焦虑量表(HAMA),帕金森病睡眠障碍量表(PDSS),蒙特利尔认知评估量表(MoCA),简易精神状态检查(MMSE),日常生活能力量表(ADL),总有效率(参照《中医老年颤证诊断和疗效评定标准》),中医证候积分(参照《中药新药临床研究指导原则》)以及不良反应。
1.3 排除标准1)年龄范围不在纳入标准要求范围内。2)治疗组或(和)对照组西医治疗基础上涉及心理咨询、针灸、拔罐、按摩、熏蒸等非单纯中药治疗的研究。3)采用辨证分型治疗大于2种及以上中药复方或治疗中加用非西药与中药的第3种疗法。4)无法获得原文,且向原作者索要无果或文章数据结果欠真实。5)文章结局指标不符合要求或采用的量表类型不能明确。
1.4 方法学质量通过数据提取和偏倚风险评估,经文献筛选、数据提取及偏倚风险评估完成依据Cochrane Handbook提供的ROB量表对纳入的文献进行质量评价。评价条目主要包括以下项目:1)随机序列产生方法(Random Sequence Generation);2)分配隐藏(Allocation Concealment);3)对受试者和研究者施盲(Blinding of patients and personnel);4)对结果测量者的盲法(Blinding of Outcome Assessment);5)不完整的结果数据(Incomplete Outcome Date);6)选择性报告(Selective Reporting);7)其他偏倚(Other Bias)。根据评估项目,对7个偏倚风险项目做出评估。每个条目可被评为低偏倚风险、高偏倚风险、偏倚风险不确定3个等级。见图 1。

|
| 图 1 纳入研究偏倚评价 |
采用Cochrane协作网提供的RevMan 5.3软件对数据进行分析。二分类变量采用RR值(相对危险度,rate ratios)表示,连续变量采用MD值(均数差,meandifference)表示,两者均用95%可信区间(CI)表示。
1.5.2 异质性评估及meta分析研究结果合并前,对所有的结果进行异质性检验。当I2值< 50%时,说明异质性较小,采用固定效应模型进行合并;当I2>50%时,表明纳入文献异质性较大,采用随机效应模型,查找原因以降低异质性,否则放弃合并。Meta分析结果用森林图展示。
1.5.3 发表偏倚分析以漏斗图展示主要结局指标的发表偏倚。
2 检索结果根据PRISMA声明和国际Cochrane协作网工作手册标准,采用计算机和手工相结合的方式进行检索。
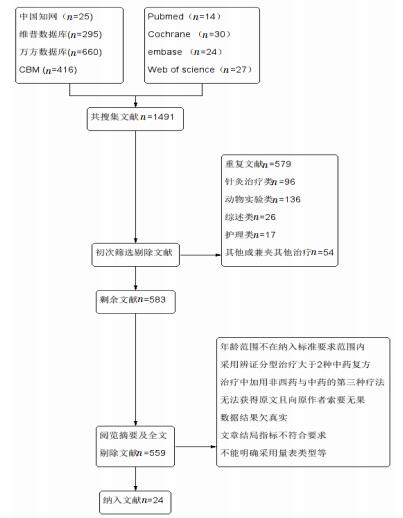
2.1 检索情况通过主题词检索数据库,共搜得文献1 491篇,运用Endnote进行筛选,首先排除重复文献、非中药治疗文献、非原发性帕金森病患者、动物实验文献、护理相关文献、综述等,共计908篇,两名研究者分别独立通过阅读题目及摘要对剩余文献进行初步筛选,通过初筛的文章进入全文筛选。按照已制定的纳排标准及质量评价要求进行全文筛选最终选定纳入的文献。两名研究者根据预设的数据提取表对纳入的文献进行数据提取。缺失的数据尽可能与原作者联系获得,对有分歧的文献通过讨论及第三方商议决定。最后筛选剩余24篇文献,进行Meta分析。共计1 836例患者。文献检索最终纳入24篇RCT文献,文献检索筛选流程及结果见图 2。
|
| 图 2 文献筛选流程图 |
所有纳入的文献均为中文文献及英文文献,研究时间从2009—2018年。所有患者均被诊断为原发性帕金森病。所有文献提示了组间基线特征具有可比性,其中4篇文献报道了NMSS量表评分,8篇文献报道了NMS-Quest量表评分,11篇文献报道了UPDRS Ⅰ,14篇文献报道了UPDRS Ⅱ,6篇文献报道了PDQ-39量表评分;4篇文献报道了HAMD量表评分,1篇文献报道了HAMA量表评分,2篇文献报道了ADL量表评分,2篇文献报道了MMSE量表评分,2篇文献报道了MoCA量表评分,4篇文献报道了临床疗效,3篇文献报道了中医证候积分,3篇文献报道了不良反应发生率。见表 1。
根据结局指标,分别以主要结局指标及次要结局指标进行分析。
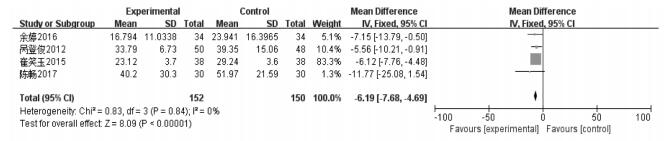
3.1 主要指标 3.1.1 帕金森病非运动症状量表(NMSS)4篇文献采用NMSS量表测量帕金森病非运动症状积分水平,由于异质性较低(P=0.84,I2=0%),采用固定效应模型合并分析,进行Meta分析且两组差异有统计学意义[MD=-6.19,95%CI=(-7.68,-4.69),Chi2=0.83,DF=3,P < 0.000 01,n=302],结果提示中药联合抗PD药物在减少NMSS量表评分方面优于单纯抗PD西药治疗,见图 3。
|
| 图 3 治疗组与对照组NMSS评分 |
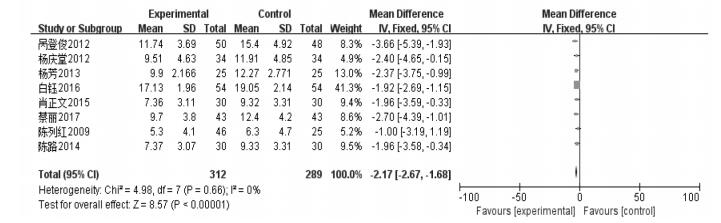
8篇文献采用NMS-Quest量表测量非运动症状积分水平,由于异质性较低(P=0.66,I2=0%),采用固定效应模型合并分析,进行Meta分析[MD=-2.17,95%CI=(-2.67,-1.68),P<0.000 01,n=601]。结果提示中药联合抗PD药物在减少NMS-Quest量表评分方面优于单纯抗PD西药治疗,见图 4。
|
| 图 4 治疗组与对照组NMS-Quest评分 |
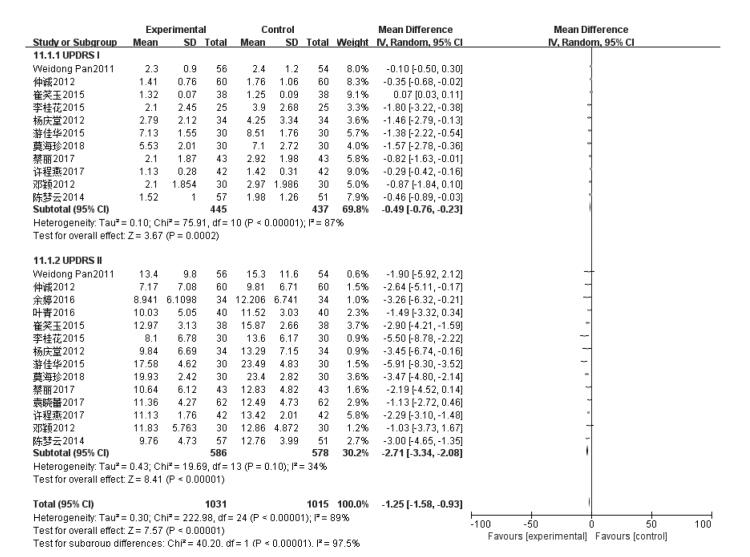
11篇文献采用UPDRS Ⅰ量表测量精神行为及情绪评分,由于异质性较高(P < 0.000 001,I2 =87%),采用随机效应模型,未进行Meta分析[Chi2=75.91,DF=10,P=0.000 2 < 0.05,n=882]。而14篇文献对UPDRS Ⅱ量表测量日常生活活动评分,结果发现其异质性较低(P=0.10,I2=34%),采用随机效应模型,进行Meta分析后,得到[MD=-2.71,95%CI=(-3.34,-2.08),P < 0.000 01,n=1 164]。结果提示中药联合抗PD西药治疗PD在UPDRS Ⅱ方面相比较单纯抗PD西药治疗有一定优势,见图 5。
|
| 图 5 治疗组与对照组UPDRSI Ⅱ评分 |
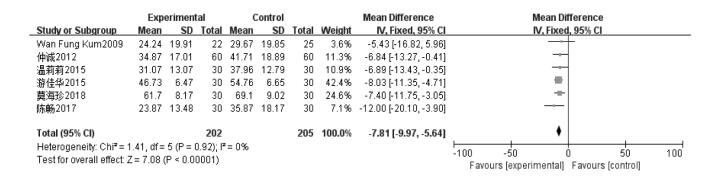
6篇文献采用PDQ-39量表测量PD生存质量问卷,由于异质性较低(P=0.92,I2=0%),采用固定效应模型,进行Meta分析[MD=-7.81,95%CI=(-9.97,-5.64),P < 0.000 01,n=407]。结果提示中药联合抗PD药物在改善PDQ-39评分方面优于单纯抗PD西药,见图 6)。
|
| 图 6 治疗组与对照组PDQ-39评分 |
4篇文献采用HAMD量表测量抑郁症状积分水平,由于异质性较高(P < 0.000 1,I2=88%),未进行Meta分析,[Chi2=25.17,DF=3,P < 0.000 01 < 0.05,n=304]。4篇文献均报道了中药联合抗PD药物(和抗抑郁药物)在减少HAMD量表评分方面仍优于单纯抗PD西药(和抗抑郁药物)。
3.3.1.2 汉密尔顿焦虑量表(HAMA)1篇文献采用HAMA量表测量焦虑症状积分水平,未进行数据合并及分析。
3.3.2 认知障碍 3.3.2.1 简易精神状态检查(MMSE)2篇文献采用MMSE量表测量认知水平,由于异质性较高(P=0.13,I2=57%),未进行Meta分析,[Chi2=2.33,DF=1,P=0.02 < 0.05,n=140]。2篇文献均报道了中药联合抗PD药物在改善MMSE量表评分方面优于单纯抗PD西药。
3.3.2.2 蒙特利尔认知评估量表(MoCA)2篇文献采用MoCA量表测量认知水平,由于异质性较高(P=0.02,I2=83%),未进行Meta分析,[Chi2=2.91,DF=1,P=0.05,n=140]。2篇文献均报道了中药联合抗PD药物在改善MoCA量表评分方面优于单纯抗PD西药。
3.3.3 日常生活能力量表(ADL)2篇文献采用ADL量表测量生活能力水平,由于异质性较高(P=0.02,I2=83%),未进行Meta分析,[Chi2=5.41,DF=1,P=0.02,n=140]。2篇文献均报道了中药联合抗PD药物在改善ADL量表评分方面仍优于单纯抗PD西药。
3.3.4 帕金森病睡眠障碍量表(PDSS)4篇文献采用PDSS量表测量睡眠水平,由于异质性较高(P=0.000 2,I2=88%),未进行Meta分析,[Chi2=17.11,DF=2,P < 0.000 01 < 0.05,n=340]。4篇文献均报道了中药联合抗PD药物在改善PDSS量表评分方面仍优于单纯抗PD西药。
3.3.5 有效率4篇文献依据《中医老年颤证诊断和疗效评定标准》进行疗效判定,依据有效率进行中药联合西药基础上与西药常规治疗两组间差异性,由于异质性较低(P=0.98,I2=0%),采用固定效应模型,进行Meta分析[OR=2.78,95%CI=(1.69,4.57),P < 0.000 01,n=334]。结果提示中药联合抗PD西药治疗PD在有效率方面分析中优于单纯抗PD西药治疗(注:有效性分级,将痊愈、有效、显效均归为有效,无效、恶化归为无效,进行分析)。见图 7。
|
| 图 7 治疗组与对照组有效率 |
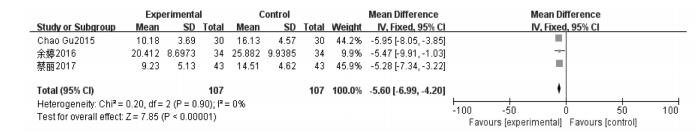
3篇文献《中药新药临床研究指导原则》采用中医证候积分评价中药联合西药基础上与西药常规治疗两组间差异性,由于异质性较低(P=0.90,I2=0%),采用固定效应模型,进行Meta分析[MD=-5.60,95%CI=(-6.99,-4.20),P < 0.000 01,n=214]。结果提示中药联合抗PD西药治疗PD在减低中医证候积分方面优于单纯抗PD西药治疗。见图 8。
|
| 图 8 各组中医证候积分 |
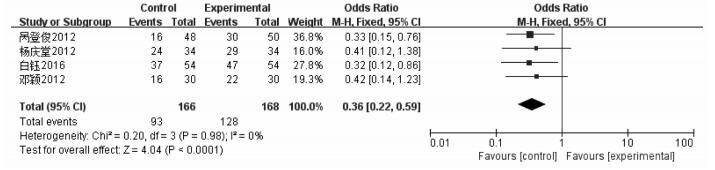
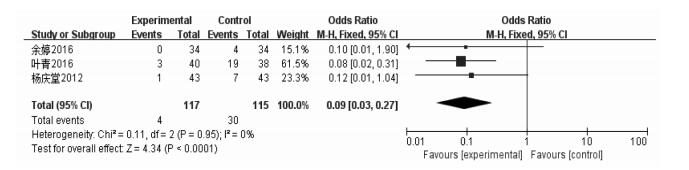
3篇文献依据治疗期间发生不良反应患者例数进行分析中药联合西药基础上与西药常规治疗两组间差异性,由于异质性较低,采用固定效应模型(P=0.95,I2 =0%),采用固定效应模型,进行Meta分析[OR=0.09,95%CI=(0.03,0.27),P=0.000 1 < 0.05,n=232]。结果提示中药联合抗PD西药治疗相比较单纯抗PD西药治疗在不良反应发生方面更佳。见图 9。
|
| 图 9 各组不良反应发生率 |
随着中国老龄化社会日趋加重,PD的患病和发病人数持续增长,有研究证实,几乎所有的PD患者至少具有一种非运动症状,并与PD的持续时间、疾病严重程度及认知功能损害都有密切关系,这也是影响患者生活质量甚至晚期致残的主要因素。而在西医治疗方面,左旋多巴仍是被报道过的仅有的可以延长生活期望的药物,但在长期的替代疗法治疗后,就会越来越不具优势,甚至超过50%的PD患者最终会经历严重运动障碍、睡眠发作以及不良反应等,进而为患者、家庭及社会造成难以估量的负担[31-33]。而中医药在减轻多种症状上,尤其是年龄相关性症状效果显著。同时中医药辅助西医抗PD药物治疗与西医传统抗PD治疗相比,能够延长西医抗PD药物剂量的增加及联合用药的时程,同时中医药本身毒副作用较小,根据药物偏性以偏纠偏,因此发挥中医药优势,不仅能够改善PD的临床症状严重程度积分,且不良反应少[34-37]。
本研究结果表明中西医结合治疗帕金森病非运动症状在减少NMS-Quest及NMSS量表评分方面优于单纯抗PD西药治疗,在减轻UPDRS Ⅱ评分和改善PDQ-39方面同样优于单纯抗PD西药治疗。在中医评价方面的有效率、中医证候积分和多种非运动症状量表以及不良反应等方面均具有一定优势。尽管以量表评分存在一定主观因素及评分水平的差异,同时存在所纳入的文献质量局限等问题,但确已证实中西医结合在治疗PD患者与单纯西医抗PD治疗相比具有确切优势,能够改善患者症状,提高生活质量,减轻不良反应。为进一步证实中西医结合在治疗PD方面的临床疗效,得出更为可靠的结论指导临床,仍需更多的高质量、大样本、多中心临床随机对照试验深入全面研究。
| [1] |
Dorsey ER, Constantinescu MR, Thompson JP, et al. Projected number of people with parkinson disease in the most populous nations, 2005 through 2030[J]. American Academy of Neurology, 2007, 384-386. |
| [2] |
Lee A, Gilbert RM. Epidemiology of parkinson disease[J]. Neurologic clinics, 2016, 34: 955-965. DOI:10.1016/j.ncl.2016.06.012 |
| [3] |
Robert L, Nussbaum MD, Christopher E, et al. Alzheimer's disease and parkinson's disease[J]. The New England Journal of Medicine, 2003, 1356-1364. |
| [4] |
Zhang ZX, Roman GC, Hong Z, et al. Parkinson's disease in china:Prevalence in beijing, xian, and shanghai[J]. The Lancet, 2005, 365: 595-597. DOI:10.1016/S0140-6736(05)70801-1 |
| [5] |
Pan W, Kwak S, Liu Y, et al. Traditional Chinese Medicine Improves Activities of Daily Living in Parkinson's Disease[J]. Parkinson's Disease, 2011, 1-7. |
| [6] |
Song L, Jie D, Cheng C, et al. Therapies for Parkinson's diseases:alternatives to cuMDent Pharmacological interventions[J]. Neural Transm, 2016. |
| [7] |
Chua KK, Wong A, Chan KW. A randomized controlled trial of Chinese medicine on nonmotor symptoms in Parkinson's disease[J]. Parkinson's Disease, 2017, 1-8. |
| [8] |
Chao Gu, Ting Shen, Hongmei An, et al. Combined therapy of Di-Huang-Yi-Zhi with Donepezil in patientswith Parkinson's disease dementia[J]. Neuroscience Letters, 2015, 13-17. |
| [9] |
Wan FK, Siva SKD, Zhao XB, et al. Treatment of idiopathic parkinson's disease with traditional Chinese herbal medicine:A randomized placebo-controlled pilot clinical study[J]. Evidence-Based Complementaryand Alternative Medicine, 2011, 1-8. |
| [10] |
袁晓蕾, 叶青, 袁灿兴, 等. 滋肾平颤颗粒治疗帕金森病非运动症状临床研究[J]. 中国中医药信息杂志, 2017, 24(9): 25-29. DOI:10.3969/j.issn.1005-5304.2017.09.007 |
| [11] |
陈畅, 梁艳, 唐莉莉, 等. 温肾养肝方治疗帕金森病非运动症状30例临床研究[J]. 时珍国医国药, 2017, 28(3): 636-638. |
| [12] |
杨庆堂, 宋颖民. 芍药甘草汤合甘麦大枣汤加减治疗帕金森病临床观察[J]. 中医临床研究, 2012, 4(11): 1-2. DOI:10.3969/j.issn.1674-7860.2012.11.001 |
| [13] |
杨芳.郁乐疏合剂对帕金森病肝郁血瘀证非运动症状的影响研究[D].成都: 成都中医药大学, 2013. http://d.g.wanfangdata.com.cn/Thesis_D667639.aspx
|
| [14] |
呙登俊, 王浩, 胡智伟, 等. 人参归脾汤治疗气血亏虚型老年颤证非运动症状50例观察[J]. 浙江中医杂志, 2012, 47(3): 175-176. DOI:10.3969/j.issn.0411-8421.2012.03.014 |
| [15] |
蔡丽, 刘毅, 李文涛. 止颤汤联合西药治疗帕金森病43例随机双盲对照研究[J]. 江苏中医药, 2017, 49(11): 33-35. DOI:10.3969/j.issn.1672-397X.2017.11.013 |
| [16] |
崔笑玉, 李文涛. 中西医结合治疗肝肾阴虚型帕金森病非运动症状38例临床研究[J]. 江苏中医药, 2015, 47(2): 30-31. |
| [17] |
陈列红, 谈友芬. 益元饮治疗帕金森病非运动症状46例[J]. 南京中医药大学学报, 2009, 25(6): 472-473. |
| [18] |
仲诚, 黄萍, 孙照国, 等. 补肾活血通络胶囊治疗原发性帕金森病120例[J]. 中国实验方剂学杂志, 2012, 18(24): 343-346. |
| [19] |
肖正文. 滋肾益髓方在治疗帕金森病运动及非运动症状中的疗效分析[J]. 中外医疗, 2015(8): 175-179. DOI:10.3969/j.issn.1674-0742.2015.08.080 |
| [20] |
白钰, 吕书勤, 马晓. 滋肾柔经汤改善帕金森病肝肾阴虚证的非运动症状[J]. 中国实验方剂学杂志, 2016, 22(8): 182-186. |
| [21] |
余婷.脑康颗粒治疗雪域东风型帕金森病的临床研究[D].广州: 广州中医药大学, 2016.
|
| [22] |
陈路, 陈志刚, 侯月. 滋肾益髓方治疗帕金森病运动及非运动症状的疗效观察[J]. 北京中医药大学学报, 2014, 37(3): 209-212. DOI:10.3969/j.issn.1006-2157.2014.03.014 |
| [23] |
莫海珍, 胡玉英, 梁慧荟, 等. 益肾调肝解郁法治疗肝肾阴虚型帕金森病抑郁的临床研究[J]. 天津中医药, 2018, 35(1): 11-14. |
| [24] |
叶青, 张红智, 蔡定芳, 等. 益智平颤方治疗帕金森病合并轻度认知障碍疗效观[J]. 上海中医药杂志, 2016, 50(7): 47-62. |
| [25] |
温莉莉, 贺燕, 姬琳. 苁乌熄风颗粒对帕金森病中医证候.运动症状和生存质量的干预研究[J]. 辽宁中医药大学学报, 2015, 17(4): 130-132. |
| [26] |
邓颖, 顾锡镇, 袁昌文, 等. 定颤颗粒联合美多巴治疗帕金森病疗效探析[J]. 实用中西医结合临床, 2012, 12(3): 21-22. DOI:10.3969/j.issn.1671-4040.2012.03.012 |
| [27] |
游佳华, 娄艳芳, 姚建景, 等. 舒筋定颤汤对帕金森病非运动症状的影响[J]. 河南中医, 2015, 35(12): 3120-3121. |
| [28] |
李桂花, 张震中, 杨新玲. 益肾填髓通络方在改善精亏髓减型帕金森患者的临床观察[J]. 辽宁中医杂志, 2015, 42(10): 1906-1909. |
| [29] |
许程燕. 滋阴息风汤联合美多芭治疗肝肾阴虚型帕金森病非运动症状的临床疗效研究[J]. 中医临床研究, 2017, 9(30): 13-14. DOI:10.3969/j.issn.1674-7860.2017.30.005 |
| [30] |
陈梦云, 刘毅, 阮克锋, 等. 止颤颗粒联合常规西药治疗肝肾不足、气血两虚型帕金森病的随机.双盲.安慰剂对照临床研究[J]. 上海中医药杂志, 2014, 48(10): 27-30. |
| [31] |
Muangpaisan W, Hori H. A systematic review of the worldwide prevalence and incidence of Parkinson's disease[J]. Journal of the Medical Association of Thailand Chotmaihet Thangphaet, 2011, 94(6): 749-755. |
| [32] |
Katunina E, Titova N. The epidemiology of nonmotor symptoms in parkinson's disease (cohort and other studies)[J]. InTernational Review of Neurobiology, 2017, 133: 91-110. DOI:10.1016/bs.irn.2017.05.012 |
| [33] |
Rubenstein LM, Deleo A, Chrischilles EA. Economic and health-related quality of life consider-ations of new therapies in Parkinson's disease[J]. Pharmacoeconomic, 2001, 19(7): 729-752. DOI:10.2165/00019053-200119070-00003 |
| [34] |
Kleinman M, Frank S. Epidemiology and clinical diagnosis of parkinson disease[J]. PET Clinics, 2013, 8: 447-458. DOI:10.1016/j.cpet.2013.08.005 |
| [35] |
Lange R, Erbguth F. Parkinson's disease in the elderly[J]. Zeitschrift fur Gerontologie und Geriatrie, 2017, 50: 547-559. DOI:10.1007/s00391-017-1284-5 |
| [36] |
Wei W, Chen HY, Fan W, et al. Chinese medicine for idiopathic parkinson's disease:A meta analysis of randomized controlled trials[J]. Chinese Journal of InteGrative Medicine, 2017, 23: 55-61. DOI:10.1007/s11655-016-2618-7 |
| [37] |
Paolo Barone MD, Angelo Antonini MD, Carlo Colosimo MD, et al. The Priamo Study:A Multicenter Assessment ofNonmotor Symptoms and Their Impact onQuality of Life in Parkinson's Disease[J]. Movement Disorders, 2009(24): 1641-1649. |
 2019, Vol. 38
2019, Vol. 38