文章信息
- 王剑丽, 瞿璐, 阮静雅, 孙璠, 王涛, 张祎
- WANG Jianli, QU Lu, RUAN Jingya, SUN Fan, WANG Tao, ZHANG Yi
- 花生衣化学成分的分离与结构鉴定
- Study on the constituents of Arachis hypogaea Linn.
- 天津中医药大学学报, 2019, 38(2): 175-179
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(2): 175-179
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.02.18
-
文章历史
收稿日期: 2018-09-21
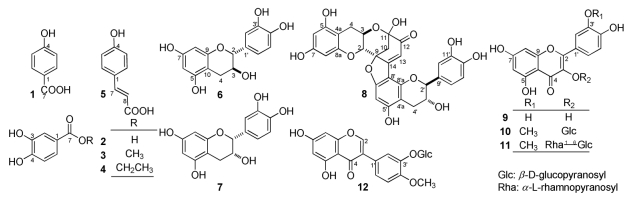
花生衣(Arachis hypogaea Linn.),又称花生皮,是一味传统中药,性味甘、涩、平,入肺、脾、肝经,具有健脾和胃、养血止血,散瘀消肿之功[1]。现代药理研究表明,花生衣具有抗氧化、抗过敏、降血糖、降血脂及防止血小板减少等多种生理活性[2-3]。花生衣作为花生加工中的副产物,来源广泛,价格低廉,但目前多作为饲料和燃料,利用度低,难以体现其应用价值。为扩大花生衣的应用范围,提高其药用植物资源利用率,本课题对花生衣的化学成分进行了初步研究,为该植物的进一步研究与开发利用提供物质基础。作者采用多种色谱法对花生衣50%乙醇提取物的化学成分进行分离制备,并利用与文献[4-8]类似的方法,鉴定了12个单体化合物的结构,分别为对羟基苯甲酸(1)、原儿茶酸(2)、原儿茶酸甲酯(3)、原儿茶酸乙酯(4)、对香豆酸(5)、儿茶素(6)、表儿茶素(7)、rhodonidin A(8)、槲皮素(9)、异鼠李素-3-O-β-D-葡萄糖苷(10)、异鼠李素-3-O-芸香糖苷(11)、3′,5,7-trihydroxyisoflavone-4′-methoxy-3′-O-β-glucopyranoside(12)。其中8为首次从落花生属中分离得到,3为首次从该植物中分离得到的化合物,见图 1。
|
| 图 1 化合物1-12的结构 |
Bruker 500MR超导核磁共振波谱仪(德国Bruker公司,Avance Ⅲ 500 MR),安捷伦6500系列四级杆-飞行时间质谱仪(美国Aglient公司,6520 Accurate-Mass Q-TOF LC/MS)。正相柱色谱用硅胶(48~75 μm),高效液相色谱法(HPLC)用分析柱以及制备柱[Cosmosil 5C18-MS-Ⅱ(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm);Cosmosil PBr(250 mm×4.6 mm,5 μm)及(250 mm×20 mm,5 μm),日本Nacalai Tesque公司],氘代甲醇(CD3OD)和二甲基亚砜(DMSO-d6,北京崇熙科技孵化器公司)。分析和色谱纯二氯甲烷(CH2Cl2)、乙酸乙酯(EtOAc)、甲醇(MeOH)、乙腈(CH3CN)、冰醋酸(HAc)等试剂购自天津康科德科技有限公司。
花生衣由山东翔宇健康制药有限公司提供,由天津中医药大学李天祥教授鉴定为落花生属植物花生的干燥种皮。标本保存于天津中医药大学中医药研究院。
2 提取与分离取干燥花生衣(8.0 kg),用50%乙醇溶液依次加热回流提取,减压回收溶剂,得浸膏2 024.4 g。取上述浸膏1 518.3 g溶于水,用EtOAc-H2O(1:1,v/v)萃取,得EtOAc层和H2O层萃取物分别为389.1 g和830.0 g,不溶性沉淀253.7 g。EtOAc层萃取物(150.0 g)经硅胶柱层析[CH2Cl2→CH2Cl2-MeOH(100:3→100:7,v/v)→CH2Cl2-MeOH-H2O(10:3:1→7:3:1→6:3:1→6:4:1,下层,v/v)],得到12个组分(Fr.1~Fr.12)。Fraction 5(2.8 g)经硅胶柱层析[CH2Cl2→CH2Cl2-MeOH(100:1→100:3→100:5→100:7,v/v)],得到9个组分(Fr.5-1~Fr.5-9)。Fractions 5-3(117.0 mg)和5-4(263.5 mg)分别经制备型高效液相色谱法(PHPLC)分离制备[MeOH-H2O(40:60,v/v)+ 1% HAc,5C18-MS-Ⅱ柱],得对羟基苯甲酸(1,5.6 mg)、原儿茶酸乙酯(4,8.0 mg)和对香豆酸(5,15.5 mg)。Fraction 6(2.9 g)经Sephadex LH-20凝胶柱层析[CH2Cl2-MeOH(1:1,v/v)],得到7个组分(Fr.6-1~Fr.6-7)。Fraction 6-4(940.0 mg)经PHPLC分离制备[MeOH-H2O(20:80,v/v)+ 1% HAc,5C18-MS-Ⅱ柱]以及Sephadex LH-20柱层析(MeOH)纯化,得到原儿茶酸(2,147.0 mg)、儿茶素(6,439.2 mg)和表儿茶素(7,105.3 mg)。Fraction 6-5(396.2 mg)经Sephadex LH-20凝胶柱层析(MeOH),得到5个组分(Fr.6-5-1~Fr.6-5-5)。Fraction 6-5-4(15.3 mg)经硅胶柱纯化[CH2Cl2-MeOH(100:3,v/v)],得到槲皮素(9,5.2 mg)。Fraction 7(2.5 g)经ODS柱层析[MeOH-H2O(20:80→30:70→40:60→50:50→60:40→70:30→80:20→100:0,v/v)]得到12个组分(Fr.7-1~Fr.7-12)。Fraction 7-7(113.2 mg)经Sephadex LH-20凝胶柱层析(MeOH),得到5个组分(Fr.7-7-1~Fr.7-7-5)。Fraction 7-7-3(28.7 mg)经PHPLC分离制备[MeOH-H2O(35:65,v/v)+ 1% HAc,5C18-MS-Ⅱ柱],得到rhodonidin A(8,11.0 mg)。Fraction 7-8(61.4 mg)经Sephadex LH-20凝胶柱层析(MeOH)和PHPLC分离制备[CH3CN-H2O(22:78,v/v)+ 1% HAc,5C18-MS-Ⅱ柱],得到异鼠李素-3-O-β-D-葡萄糖苷(10,5.2 mg)和3′,5,7-trihydroxyisoflavone-4′-methoxy-3′-O-β-glucopyranoside(12,3.5 mg)。Fraction 9(5.0 g)经ODS柱层析[MeOH(10:90→20:80→30:70→40:60→50:50→60:40→70:30→100%,v/v)],得到12个组分(Fr.9-1~Fr.9-12)。Fraction 9-6(1.1 g)经Sephadex LH-20凝胶柱层析(MeOH)和PHPLC分离制备[CH3CN-H2O(17:83,v/v)+ 1% HAc,5C18-MS-Ⅱ柱],得到原儿茶酸甲酯(3,2.6 mg)。Fraction 9-9(110.2 mg)经PHPLC分离制备[MeOH-H2O(67:33,v/v)+ 1% HAc,PBr柱],得到3个组分(Fr.9-9-1~Fr.9-9-3)。Fraction 9-9-3(25.5 mg)经PHPLC分离制备[CH3CN-H2O(22:78,v/v)+ 1% HAc,PBr柱],得到异鼠李素-3-O-芸香糖苷(11,4.5 mg)。
3 结构鉴定 3.1 化合物1白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 139.039 1[M+H]+ (calcd for C7H7O3,139.039 0),确定其分子式为C7H6O3。1H NMR(CD3OD,500 MHz)谱数据:δ 7.87(2H,d,J=9.0 Hz,H-2,6),6.81(2H,d,J=9.0 Hz,H-3,5)。13C NMR(CD3OD,125 MHz)谱数据:δ 123.0(C-1),133.0(C-2,6),116.0(C-3,5),163.0(C-4),170.3(C-7)。其1H、13C NMR谱数据与文献[9]相对照,鉴定该化合物为对羟基苯甲酸(p-hydroxybenzoic acid)。
3.2 化合物2白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 153.019 1[M-H]-(calcd for C7H5O4,153.019 3),确定其分子式为C7H6O4。1H NMR(CD3OD,500 MHz)谱数据:δ 7.57(1H,d,J=2.0 Hz,H-2),6.90(1H,d,J=8.5 Hz,H-5),7.54(1H,dd,J=2.0、8.5 Hz,H-6)。13C NMR(CD3OD,125 MHz)谱数据:δ 123.1(C-1),117.8(C-2),145.9(C-3),151.4(C-4),116.0(C-5),124.2(C-6),170.7(C-7)。其1H、13C NMR谱数据与文献[10]相对照,鉴定该化合物为原儿茶酸(protocatechuic acid)。
3.3 化合物3白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 169.049 5[M+H]+(calcd for C8H9O4,169.049 5),确定其分子式为C8H8O4。1H NMR(CD3OD,500 MHz)谱数据:δ 7.42(1H,br.s,H-2),6.80(1H,d,J=9.0 Hz,H-5),7.40(1H,dd,J=2.0、7.5 Hz,H-6),3.83(3H,s,7-OCH3)。13C NMR(CD3OD,125 MHz)谱数据:δ 122.6(C-1),117.5(C-2),146.3(C-3),151.8(C-4),115.9(C-5),123.7(C-6),168.9(C-7),52.3(7-OCH3)。其1H、13C NMR谱数据与文献[11]相对照,鉴定该化合物为原儿茶酸甲酯(protocatechuic acid methyl ester)。
3.4 化合物4白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 183.064 7[M+H]+(calcd for C9H11O4,183.0652),确定其分子式为C9H10O4。1H NMR(CD3OD,500 MHz)谱数据:δ 7.42(1H,d,J=2.0 Hz,H-2),6.79(1H,d,J=8.5 Hz,H-5),7.40(1H,dd,J=2.0、8.5 Hz,H-6),4.29(2H,q,J=6.5 Hz,H2-8),1.35(3H,t,J=6.5 Hz,H3-9)。13C NMR(CD3OD,125 MHz)谱数据:δ 122.9(C-1),115.9(C-2),146.2(C-3),151.7(C-4),117.4(C-5),123.6(C-6),168.5(C-7),61.7(C-8),14.7(C-9)。其1H、13C NMR谱数据与文献[12]相对照,鉴定该化合物为原儿茶酸乙酯(protocatechuic acid ethyl ester)。
3.5 化合物5淡黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 165.053 8[M+H]+(calcd for C9H9O3,165.054 6),确定其分子式为C9H8O3。1H NMR(CD3OD,500 MHz)谱数据:δ 7.44(2H,d,J=8.5 Hz,H-2,6),6.81(2H,d,J=8.5 Hz,H-3,5),7.60(1H,d,J=16.0 Hz,H-7),6.28(1H,d,J=16.0 Hz,H-8)。13C NMR(CD3OD,125 MHz)谱数据:δ 127.3(C-1),131.1(C-2,6),116.8(C-3,5),161.2(C-4),146.6(C-7),115.8(C-8),171.2(C-9)。其1H、13C NMR谱数据与文献[13]相对照,鉴定该化合物为对香豆酸(p-coumaric acid)。
3.6 化合物6淡黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 289.072 4[M-H]-(calcd for C15H13O6,289.071 8),确定其分子式为C15H14O6。1H NMR(CD3OD,500 MHz)谱数据:δ 4.67(1H,d,J=7.5 Hz,H-2),4.08(1H,m,H-3),[2.61(1H,dd,J=8.0、16.0 Hz),2.91(1H,dd,J=5.0、16.0 Hz),H2-4],6.05(1H,d,J=2.0 Hz,H-6),6.00(1H,d,J=2.0 Hz,H-8),6.92(1H,d,J=1.5 Hz,H-2′),6.83(1H,d,J=8.0 Hz,H-5′),6.77(1H,dd,J=1.5、8.0 Hz,H-6′)。13C NMR(CD3OD,125 MHz)谱数据:δ 82.4(C-2),68.5(C-3),28.0(C-4),157.2(C-5),96.4(C-6),157.1(C-7)95.7(C-8),156.6(C-9),101.0(C-10),131.9(C-1′),115.2(C-2′),145.8(C-3′),145.8(C-4′),116.3(C-5′),120.2(C-6′)。其1H、13C NMR谱数据与文献[14]相对照,鉴定该化合物为儿茶素(catechin)。
3.7 化合物7淡黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 289.072 7[M-H]-(calcd for C15H13O6,289.071 8),确定其分子式为C15H14O6。1H NMR(CD3OD,500 MHz)谱数据:δ 4.81(1H,br.s,H-2),4.17(1H,m,H-3),[2.74(1H,dd,J=3.0、17.0 Hz),2.86(1H,dd,J=5.0、17.0 Hz),H2-4],5.96(1H,d,J=1.5 Hz,H-6),5.94(1H,d,J=1.5 Hz,H-8),6.98(1H,d,J=2.0 Hz,H-2′),6.77(1H,d,J=8.5 Hz,H-5′),6.80(1H,d,J=2.0、8.5 Hz,H-6′)。13C NMR(CD3OD,125 MHz)谱数据:δ 79.8(C-2),67.5(C-3),29.2(C-4),157.3(C-5),96.5(C-6),157.5(C-7),96.0(C-8),157.9(C-9),100.1(C-10),132.3(C-1′),115.3(C-2′),145.9(C-3′),145.7(C-4′),116.0(C-5′),119.5(C-6′)。其1H、13C NMR谱数据与文献[15]相对照,鉴定该化合物为表儿茶素(epicatechin)。
3.8 化合物8黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 575.120 7[M-H]-(calcd for C30H23O12,575.119 5),确定其分子式为C30H24O12。1H NMR(CD3OD,500 MHz)谱数据:δ 3.96(1H,d,J=9.0 Hz,H-2),3.99(1H,m,H-3),[2.52(1H,dd,J=9.5、14.5 Hz),2.95(1H,dd,J=6.0、14.5 Hz),H2-4],5.90(1H,d,J=2.5 Hz,H-6),5.54(1H,d,J=2.5 Hz,H-8),[2.50(1H,d,J=11.5 Hz),2.67(1H,d,J=11.5 Hz),H2-10],6.42(1H,s,H-13),4.92(1H,d,J=7.0 Hz,H-2′),4.10(1H,m,H-3′),[2.60(1H,dd,J=7.5、16.5 Hz),2.85(1H,dd,J=5.5、16.5 Hz),H2-4′],6.12(1H,s,H-6′),6.84(1H,d,J=2.0 Hz,H-10′),6.79(1H,d,J=8.5 Hz,H-13′),6.74(1H,dd,J=2.0、8.5 Hz,H-14′)。13C NMR(CD3OD,125 MHz)谱数据:δ 79.6(C-2),66.9(C-3),28.4(C-4),100.5(C-4a),157.7(C-5),97.1(C-6),158.1(C-7)95.9(C-8),156.4(C-8a),89.9(C-9),46.0(C-10),95.3(C-11),194.1(C-12),112.8(C-13),164.4(C-14),83.5(C-2′),67.9(C-3′),27.8(C-4′),104.0(C-4′a),166.3(C-5′),91.0(C-6′),168.1(C-7′),105.6(C-8′),155.2(C-8′a),131.3(C-9′),114.9(C-10′),146.5(C-11′),146.6(C-12′),116.4(C-13′),119.7(C-14′)。其1H、13C NMR谱数据与文献[16]相对照,鉴定该化合物为rhodonidin A,并结合2D NMR谱的解析,对文献中C-4和C-4′位之间的化学位移进行了调换。
3.9 化合物9黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 303.051 2[M+H]+(calcd for C15H11O7,303.049 9),确定其分子式为C15H10O7。1H NMR(DMSO-d6,500 MHz)谱数据:δ 6.19(1H,d,J=2.0 Hz,H-6),6.41(1H,d,J=2.0 Hz,H-8),7.67(1H,d,J=2.0 Hz,H-2′),6.89(1H,d,J=8.5 Hz,H-5′),7.54(1H,d,J=2.0、8.5 Hz,H-6′),12.50(1H,br.s,5-OH)。13C NMR(DMSO-d6,125 MHz)谱数据:δ 146.7(C-2),135.6(C-3),175.7(C-4),160.6(C-5),98.1(C-6),163.8(C-7),93.3(C-8),156.0(C-9),102.9(C-10),121.9(C-1′),115.0(C-2′),145.0(C-3′),147.6(C-4′),115.5(C-5′),119.9(C-6′)。其1H、13C NMR谱数据与文献[17]相对照,鉴定该化合物为槲皮素(quercetin)。
3.10 化合物10黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 477.105 0[M-H]-(calcd for C22H21O12,477.103 8),确定其分子式为C22H22O12。1H NMR(DMSO-d6,500 MHz)谱数据:δ 6.20(1H,br.s,H-6),6.43(1H,br.s,H-8),7.94(1H,d,J=2.0 Hz,H-2′),6.91(1H,d,J=8.5 Hz,H-5′),7.50(1H,dd,J=2.0、8.5 Hz,H-6′),5.56(1H,d,J=7.0 Hz,H-1″),3.23(1H,dd,J=7.0、7.0 Hz,H-2″),3.25(1H,m,overlapped,H-3″),3.11(1H,m,overlapped,H-4″),3.11(1H,m,overlapped,H-5″),[3.33(1H,m,overlapped),3.59(1H,br.d,ca.J=12 Hz),H2-6″],3.84(3H,s,3′-OCH3),12.60(1H,br.s,5-OH)。13C NMR(DMSO-d6,125 MHz)谱数据:δ 156.1(C-2),132.9(C-3),177.3(C-4),161.1(C-5),98.7(C-6),164.5(C-7)93.7(C-8),156.3(C-9),103.8(C-10),121.0(C-1′),113.4(C-2′),146.8(C-3′),149.3(C-4′),115.1(C-5′),121.9(C-6′),100.7(C-1″),74.3(C-2″),76.3(C-3″),69.7(C-4″),77.4(C-5″),60.5(C-6″),55.6(3′-OCH3)。其1H、13C NMR谱数据与文献[18]相对照,并结合2D NMR谱的解析,鉴定该化合物为异鼠李素3-O-β-D-葡萄糖苷(isorhamnetin-3-O-β-D-glucoside)。
3.11 化合物11黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 623.163 0[M-H]-(calcd for C28H31O16,623.161 8),确定其分子式为C28H32O16。1H NMR(DMSO-d6,500 MHz)谱数据:δ 6.17(1H,d,J=2.0 Hz,H-6),6.39(1H,d,J=2.0 Hz,H-8),7.85(1H,d,J=2.0 Hz,H-2′),6.91(1H,d,J=8.5 Hz,H-5′),7.51(1H,dd,J=2.0、8.5 Hz,H-6′),5.43(1H,d,J=7.5 Hz,H-1″),3.22(1H,dd,J=7.5、7.5 Hz,H-2″),3.24(1H,dd,J=7.5、9.0 Hz,H-3″),3.05(1H,dd,J=9.0、9.5 Hz,H-4″),3.28(1H,m,H-5″),[3.34(1H,dd,J=5.0、11.0 Hz),3.71(1H,br.d,ca.J=11 Hz),H2-6″],4.42(1H,d,J=1.5 Hz,H-1″′),3.40(1H,dd,J=1.5、3.5 Hz,H-2″′),3.26(1H,dd,J=3.5、9.5 Hz,H-3″′),3.08(1H,dd,J=9.0、9.5 Hz,H-4″′),3.27(1H,m,H-5″′),0.98(3H,d,J=6.0 Hz,H3-6″′),3.83(3H,s,3′-OCH3),12.57(1H,br.s,5-OH)。13C NMR(DMSO-d6,125 MHz)谱数据:δ 156.4(C-2),132.8(C-3),177.0(C-4),161.0(C-5),98.9(C-6),164.2(C-7),93.8(C-8),156.2(C-9),103.9(C-10),120.9(C-1′),113.1(C-2′),146.7(C-3′),149.3(C-4′),115.1(C-5′),122.1(C-6′),101.2(C-1″),74.2(C-2″),76.3(C-3″),70.0(C-4″),75.8(C-5″),66.7(C-6″),100.8(C-1″′),70.2(C-2″′),70.5(C-3″′),71.7(C-4″′),68.2(C-5″′),17.6(C-6″′),55.5(3′-OCH3)。其1H、13C NMR谱数据与文献[19]相对照,并结合2D NMR谱的解析,鉴定该化合物为异鼠李素-3-O-芸香糖苷(isorhamnetin-3-O-rutinoside)。
3.12 化合物12黄色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 485.107 0[M+Na]+(calcd for C22H22O11Na,485.105 4),确定其分子式为C22H22O11。1H NMR(CD3OD,500 MHz)谱数据:δ 8.11(1H,s,H-2),6.21(1H,br.s,H-6),6.32(1H,br.s,H-8),7.39(1H,d,J=2.0 Hz,H-2′),7.06(1H,d,J=8.5 Hz,H-5′),7.22(1H,dd,J=2.0、8.5 Hz,H-6′),4.96(1H,d,J=7.5 Hz,H-1″),3.52(1H,dd,J=7.5、9.5 Hz,H-2″),3.48(1H,dd,J=8.5、9.5 Hz,H-3″),3.38(1H,dd,J=8.5、9.0 Hz,H-4″),3.43(1H,m,H-5″),[3.68(1H,dd,J=6.0、12.0 Hz),3.90(1H,dd,J=2.0、12.0 Hz),H2-6″],3.90(3H,s,4′-OCH3)。13C NMR(CD3OD,125 MHz)谱数据:δ 155.3(C-2),124.9(C-3),181.9(C-4),159.2(C-5),100.2(C-6),166.7(C-7),95.1(C-8),158.2(C-9),106.0(C-10),125.4(C-1′),119.2(C-2′),147.7(C-3′),151.0(C-4′),113.6(C-5′),124.1(C-6′),102.8(C-1″),75.0(C-2″),77.9(C-3″),71.6(C-4″),78.3(C-5″),62.7(C-6″),56.8(4′-OCH3)。其1H、13C NMR谱数据与文献[20]相对照,并结合2D NMR谱的解析,鉴定该化合物为3′,5,7-trihydroxyisoflavone-4′-methoxy-3′-O-β-glucopyranoside。
4 结果与讨论花生衣产量大,价格低廉,但目前多作为饲料和燃料等低附加值产品使用,利用率低。加大对花生衣的研究和应用,可以提高花生的综合利用价值和经济价值,对促进中国食品工业的发展、增强人们的身体健康有重要的现实意义。笔者通过对花生衣的化学成分的研究,为其综合开发利用提供了实验依据。在此过程中,从花生衣50%乙醇提取物中鉴定了12个单体成分。其中化合物8为首次从落花生属中分离得到,化合物3为首次从该植物中分离得到。
| [1] |
严丹, 赵重博, 解达帅, 等. 花生衣开发利用研究进展[J]. 亚太传统医药, 2015, 11(20): 51-54. |
| [2] |
张慧文.花生红衣原花青素化学成分、衍生物和生物活性研究[D].呼河浩特: 内蒙古大学, 2014.
|
| [3] |
李孔燕.花生衣对环磷酰胺诱导的小鼠血小板减少症模型的作用研究[D].广州: 暨南大学, 2010.
|
| [4] |
晁利平, 阮静雅, 刘艳霞, 等. 绵萆薢化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2016, 35(5): 336-339. |
| [5] |
瞿璐, 刘艳霞, 李建良, 等. 祁菊叶化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2017, 36(1): 57-60. |
| [6] |
董勇喆, 史文中, 杨圣财, 等. 沙葱化学成分的分离与结构鉴定Ⅱ[J]. 天津中医药大学学报, 2016, 33(6): 404-408. |
| [7] |
李晓霞, 瞿璐, 刘丽丽, 等. 国槐化学成分与药理作用的研究进展[J]. 天津中医药大学学报, 2016, 35(3): 211-216. |
| [8] |
张祎, 晁利平, 陈秋, 等. 维药蜀葵花黄酮类成分的分离与结构鉴定[J]. 天津中医药大学学报, 2016, 35(1): 36-39. |
| [9] |
李艳茸, 李春, 王智民, 等. 藏药甘青乌头化学成分研究(Ⅲ)[J]. 中国中药杂志, 2014, 39(7): 1163-1167. |
| [10] |
傅志勤, 黄泽豪, 林婧, 等. 蛇附子化学成分及抗氧化活性研究[J]. 中草药, 2015, 46(11): 1583-1588. |
| [11] |
朱仝飞, 陈日荣, 孙庆文, 等. 西藏胡黄连化学成分研究[J]. 中草药, 2017, 48(2): 263-265. |
| [12] |
张航旗, 周戚, 付艳辉, 等. 头序瓜馥木化学成分研究[J]. 天然产物研究与开发, 2017, 29(2): 245-248. |
| [13] |
谢雪, 张宏达, 温建辉, 等. 桂枝茯苓胶囊化学成分研究(Ⅵ)[J]. 中草药, 2016, 47(21): 3795-3797. |
| [14] |
马强, 房鑫, 李俊, 等. 羊踯躅的化学成分研究[J]. 中草药, 2018, 49(5): 1013-1018. |
| [15] |
张翠, 刘占云, 於洪建, 等. 黑豆种皮的酚酸类成分研究[J]. 中草药, 2013, 44(24): 3440-3443. |
| [16] |
Wang CM, Hsu YM, Jhan YL, et al. Structure elucidation of procyanidins isolated from Rhododendron formosanum and their anti-oxidative and anti-bacterial activities[J]. Molecules, 2015, 20(7): 12787-12803. DOI:10.3390/molecules200712787 |
| [17] |
李蓉, 杨春涛, 田凯, 等. 东方草莓的化学成分研究[J]. 云南民族大学学报(自然科学版), 2014, 23(5): 313-316. DOI:10.3969/j.issn.1672-8513.2014.05.001 |
| [18] |
昶国平, 李广雷, 刘博譞, 等. 小花棘豆的化学成分研究[J]. 中医药学报, 2014, 42(4): 15-16. DOI:10.3969/j.issn.1002-2392.2014.04.006 |
| [19] |
张成刚, 卢叶, 王峥涛, 等. 阔刺兔唇花全草的化学成分研究[J]. 中草药, 2014, 45(22): 3224-3229. DOI:10.7501/j.issn.0253-2670.2014.22.003 |
| [20] |
Lou H, Yuan H, Yamazaki Y, et al. Alkaloids and flavonoids from peanut skins[J]. Planta medica, 2001, 67(4): 345-349. DOI:10.1055/s-2001-14319 |
 2019, Vol. 38
2019, Vol. 38