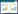文章信息
- 闫晓鑫, 张志强, 杜守颖
- YAN Xiaoxin, ZHANG Zhiqiang, DU Shouying
- 独活标准汤剂UPLC特征图谱的研究和分析
- Study and analysis of UPLC characteristic spectrum of duhuo standard decoction
- 天津中医药大学学报, 2019, 38(3): 267-273
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(3): 267-273
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.03.16
-
文章历史
收稿日期: 2019-02-20
2. 北京中医药大学, 北京 100029
2. Beijing University of Chinese Medicine, Beijing 100029, China
独活为伞形科植物重齿毛当归(Angelica pube-scens Maxim.f.biserrata Shan et Yuan)的干燥根,属祛风除湿类中草药[1]。具有祛风除湿,通痹止痛之功效。可用于风寒湿痹,腰膝疼痛,少阴伏风头痛,风寒挟湿头痛[2-3]。其主要化学成分为蛇床子素、二氢欧山芹醇当归酸酯等为主的香豆素类及挥发油类成分。但是中药为多类成分的共存体,内部种类众多,变化复杂,单一的成分用于中药质量评价已经无法满足实际需要[4]。
中药饮片标准汤剂是以中医药理论为指导,临床应用为基础,经标准化工艺制备而成的单味中药饮片水煎液[5-6]。该理论被提出之后,便成为了中药现代工艺转化的标尺,也为不同来源、形式的中药,提供了参照物,以保证所得产品的质量。
本研究从独活的道地及主产区收集了18批独活,用于建立其标准汤剂的特征图谱,使用高效液相色谱-质谱联用(LC-MS)对特征图谱中不同成分进行分析指认,使用SPSS软件对特征图谱进行主成分分析(PCA)和聚类分析(HCA)评价,并对煎煮过程的转移概率进行量化,研究煎煮过程的内在成分变化,阐释煎煮对于独活内在成分的影响规律,以建立独活标准汤剂超高效液相色谱(UPLC)特征图谱,为完善独活配方颗粒的特征图谱质量控制奠定基础。
1 实验材料 1.1 仪器岛津LC-30AD超高效液相色谱仪,LC-30AD四元泵,SIL-30AC自动进样器,SPD-20A紫外检测器,CTO-20A柱温箱(日本岛津株式会社),Labsolution DB工作站;Waters ACQUITY UPLC®H-Class超高效液相色谱仪;PDA Detector检测器;TUV Detector检测器;Empower 3色谱工作站;岛津LC-20A高效液相色谱仪,LC-20A四元泵,SIL-20AC自动进样器,SPD-20A紫外检测器,CTO-10A柱温箱(日本岛津株式会社);JY20002电子天平(上海舜宇恒平科学仪器有限公司);BSA124S电子天平[赛多利斯科学仪器(北京)有限公司];ME104E电子天平[梅特勒·托利多仪器(上海)有限公司];XP-26电子天平[梅特勒·托利多仪器(上海)有限公司];ET18电位滴定仪[梅特勒·托利多仪器(上海)有限公司];KQ-500DB超声波清洗器(昆山市超声仪器有限公司);DZKW-4电子恒温水浴锅(北京中兴伟业仪器有限公司);DHG-9140A电热鼓风干燥箱(上海一恒科学仪器有限公司)。
1.2 试药与试剂蛇床子素对照品(批号:110822-201609,纯度99.6%),二氢欧山芹醇当归酸酯对照品(批号:111583-201304,纯度98.3%)均购自中国食品药品检定研究院;甲醇(Fisher Chemical)、乙腈(默克)、甲酸(Fisher Scientific)为色谱纯;水为蒸馏水;甲醇为分析纯。
1.3 药材 1.3.1 独活药材独活药材共18批,见表 1。
按照《中华人民共和国药典》2015年版独活项下方法“除去杂质,洗净,润透,切薄片,低温干燥”制备,见表 1。
2 方法 2.1 独活标准汤剂的制备以卫生部、国家中医药管理局发布的《医疗机构中药煎药室管理规范》和国家药典委员会发布的《中药配方颗粒质量控制与标准制定技术要求》为依据[7],考察独活标准汤剂工艺条件,以制备“独活标准汤剂”。
取独活饮片100 g,置于砂锅中,一煎加入饮片量9倍水,浸泡30 min,武火煮沸后,文火煎煮30 min,趁热过滤,迅速冷却,备用;二煎加饮片量7倍水,武火煮沸后,文火煎煮20 min,趁热150目纱布过滤,迅速冷却备用;合并滤液,减压浓缩(≤50℃),浓缩至料液比约为1:1,冷冻干燥,即得。
2.2 独活配方颗粒特征图谱的建立 2.2.1 参照物溶液的制备分别取蛇床子素、二氢欧山芹醇当归酸酯对照品适量,精密称定,加甲醇制成每1 mL含蛇床子素20 μg、含二氢欧山芹醇当归酸酯2 μg的溶液,即得。
2.2.2 供试品溶液的制备取本品0.2 g,精密称定,置锥形瓶中,精密加入70%甲醇20 mL,称定质量,超声处理20 min,放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.2.3 色谱条件以十八烷基硅烷键合硅胶为填充剂,Extend C18色谱柱(2.1 mm×100 mm,1.8 μm);以甲醇为流动相A,水为流动相B,按表 2中的规定进行梯度洗脱,检测波长为330 nm,柱温35 ℃,流速0.3 mL/min,进样量:5 μL。理论塔板数按二氢欧山芹醇当归酸酯峰计算应不低于10 000[8-10]。
取独活标准汤剂冻干粉(批号:180209-445800-18)按2.2.3项下方法测定,连续检测6次,获得其特征图谱,以8号峰(蛇床子素)为参照峰,计算其相对峰面积和相对保留时间,并计算RSD。各特征峰的相对保留时间RSD在0 %~0.9%范围内,相对峰面积的RSD在0%~3.8%范围内,表明该特征图谱的精密度较好。
2.2.4.2 重复性考察取独活标准汤剂冻干粉(批号:180209-445800-18)6份,按2.2.3项下方法测定,获得其特征图谱,以8号峰(蛇床子素)为参照峰,计算其相对峰面积和相对保留时间。并计算RSD。各特征峰的相对保留时间RSD在0 %~0.1%范围内,相对峰面积的RSD在0.1%~0.3%范围内,表明该特征图谱的重复性较好。
2.2.4.3 中间精密度考察采用Waters UPLC H-Class,TUV检测器,取独活标准汤剂冻干粉(批号:180209-445800-18)6份,按2.2.3方法测定,获得其特征图谱,以8号峰(蛇床子素)为参照峰,计算其相对峰面积和相对保留时间。并计算RSD。
采用Waters UPLC H-Class,TUV检测器获得的特征图谱中,各特征峰的相对保留时间RSD在0%~0.1%范围内,相对峰面积的RSD在0%~0.4%范围内。不同仪器间相对保留时间RSD范围是0.1%~5.2%,相对峰面积RSD%范围是0.3%~5.1%,表明该特征图谱的中间精密度符合分析要求。
2.2.4.4 稳定性考察取独活标准汤剂冻干粉(180209-445800-18),按2.2.3项下方法制备供试品溶液,分别于0、2、4、8、12、24 h按正文方法进行测定,获得其特征图谱,以8号峰(蛇床子素)为参照峰,计算其相对峰面积和相对保留时间。并计算RSD。稳定性实验结果可知,溶液中化学成分在24 h稳定性,各特征峰的相对保留时间RSD在0%~0.1%范围内,相对峰面积的RSD在0.1%~0.9%范围内。
2.2.5 质谱成分指认质谱条件:Agilent Jet Stream ESI源,干燥气流速:11 L/min,干燥气温度:350 ℃,鞘气温度:400,鞘气流速:11 L/min,雾化器压力:35 psi,Fragmentor电压:130 V。正模式采集,喷嘴电压:500 V,毛细管电压:4 000 V;负模式采集,喷嘴电压:1 000 V,毛细管电压:3 500 V。
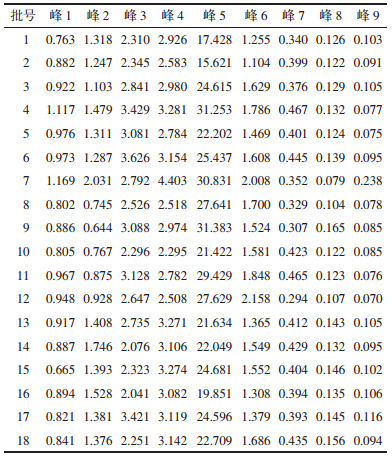
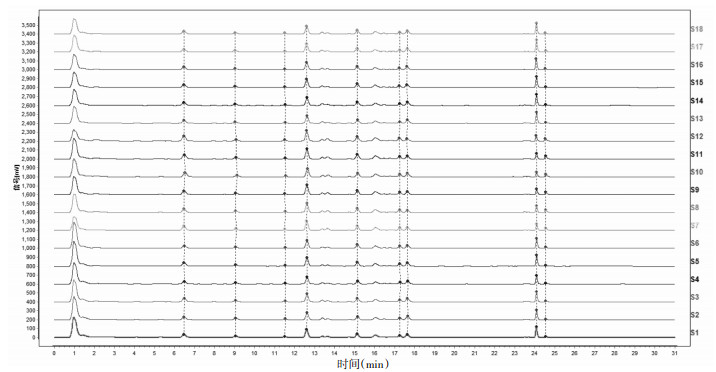
3 结果 3.1 样品检测取18批次独活标准汤剂冻干粉,照2.2.2项下方法制备供试品溶液,再照2.2.3项下方法检测,结果见表 3,图 1、2。
|
| 图 1 18批独活标准汤剂冻干粉液相图谱 |
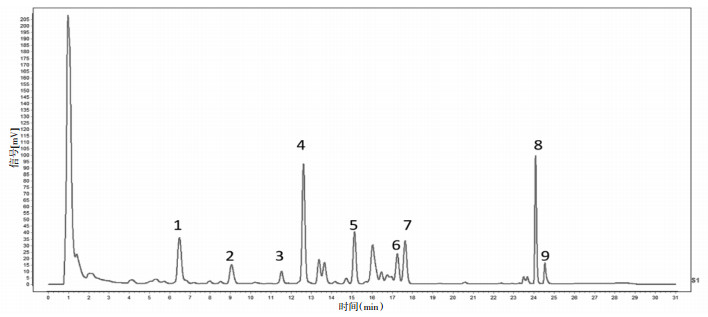
|
| 图 2 独活标准汤剂冻干粉对照图谱及共有峰标识 |
通过对特征图谱的紫外光谱信息及所采集的一级质谱图信息的研究,同时参考文献[11]对独活中的主要化学成分进行结构推测,结果见表 4。
采用2.2.3项下方法对18批独活饮片和18批独活标准汤剂冻干粉进行检测,经软件积分处理,得到相应特征图谱9个特征峰的峰面积。
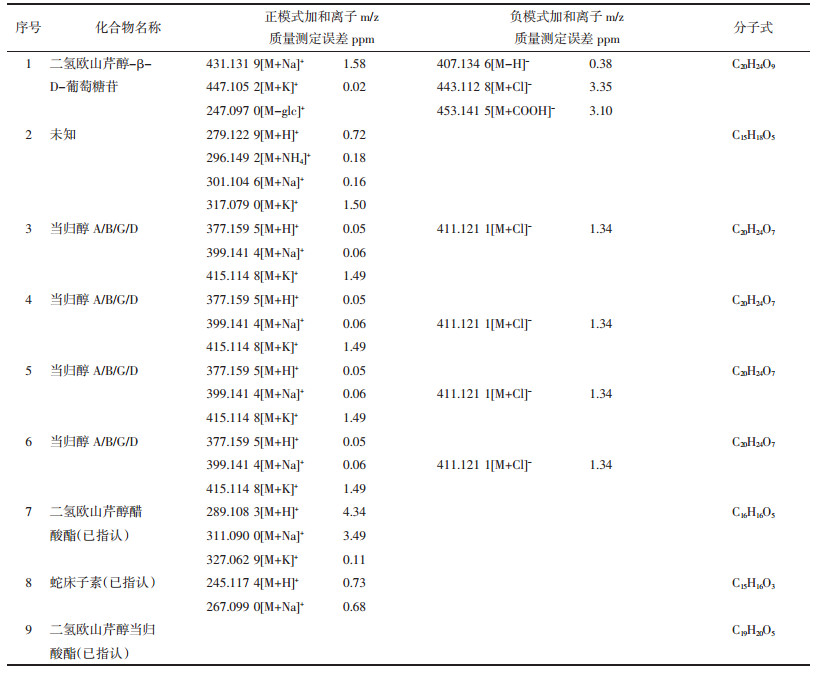
采用SPSS 20.0统计软件对18批独活饮片和18批独活标准汤剂冻干粉特征图谱进行PCA,求出相关矩阵方差,见表 5。以特征值>1未提取标准,得到前两个主成分的累计方差贡献率为90.520%(大于80%),故选择前两个主成分即可进行评价,它代表了独活中9个成分量的90.520%的信息量,具有很好的代表性,足以评价独活饮片及独活标准汤剂的质量,进而用于独活配方颗粒特征图谱的分析[12-14]。
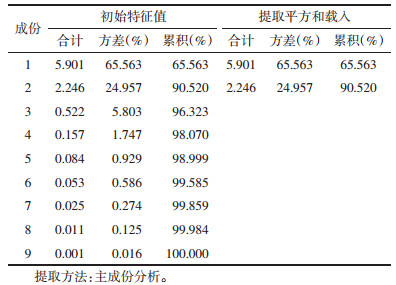
从表 6中可以看出,第1个主成分的信息主要来自色谱峰3、4、5、6、7、8,第2个主成分的信息主要来自色谱峰1、2、9。
将PCA所得的两个主成分对18批独活饮片和18批独活标准汤剂冻干粉特征图谱进行打分,所得第1个和第2个主成分进行聚类分析,以组间连接和欧氏距离作为样品测度,采用Q型聚类进行HCA。
结果显示,独活饮片和标准汤剂冻干粉均可根据产地差异分为两大类,四川省和湖北恩施样品聚为一类,湖北宜昌聚为一类,煎煮以后的标准汤剂冻干粉单独聚为一类,并与饮片相区分,样品间的距离低于饮片之间的距离。
3.3.2 饮片、标准汤剂化学成分转移概率的量化取上述实验所得18批独活饮片(称样量使用收率折算)和18批独活标准汤剂冻干粉特征图谱,得到9个特征峰峰面积,计算特征峰在煎煮过程中的转移值,计算方式为标准汤剂冻干粉的峰面积/饮片的峰面积。

|
| 图 3 聚类分析结果 |
若转移值>1,该成分在煎煮过程中以积累为主;若转移值小于1,该成分不易被水提取或分解为主。在整个煎煮过程中峰3、4、5、6以积累为主,峰1、7、8、9分解或不易转移,峰2在不同批次中出现了不同的变化趋势。
批次1~6(四川)和13~18(湖北恩施)的各峰转移情况相近,但是批次7~12(湖北宜昌)各峰转移与前两者有较大差异,主要体现在峰2、4、8、9,见表 7、图 4。
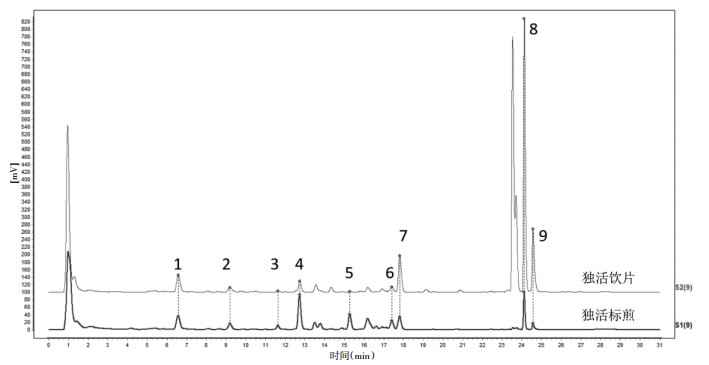
|
| 图 4 独活饮片和标准汤剂冻干粉特征图谱对比 |
中药配方颗粒是由单味中药饮片经提取浓缩制成的、供中医临床配方用的颗粒。但因中药配方颗粒受到原料、炮制加工、生产等多方面环节的限制,中药配方颗粒目前没有统一的国家质量标准。独活配方颗粒的质量标准建立也是迫在眉睫。根据国家药典委员会发布的《中药配方颗粒质量控制与标准制定技术要求》的要求,为了有效表征独活配方颗粒整体质量,需使用标准汤剂,本研究建立了对照特征图谱质量控制方法,可用于独活配方颗粒的产地来源鉴别及全面的质量控制。
本实验建立了独活标准汤剂的UPLC特征图谱对照图谱,可以全面反映样品的内在质量,评价独活标准汤剂的内在质量。本方法在色谱柱型号、流速、柱温等方面还进行了相关耐用性考察,结果表明,本方法可适用于不同型号色谱柱,在柱温28~35 ℃、流速为0.28~0.32 mL/min之间耐用性良好。
结合PCA和HCA分析方法对独活的煎煮过程进行了分析,发现产地差异是导致独活原料和独活标准汤剂差异的主要因素,煎煮可缩小这种差异。独活煎煮过程,并非单纯的成分溶出及转移,还发生了相互转化。批次1~6(四川)和13~18(湖北恩施)的各峰转移情况相近,但是批次7~12(湖北宜昌)各峰转移与前两者有较大差异,主要体现在峰2、4、8、9。通过比较各特征峰的转移值,发现在整个煎煮过程中峰3、4、5、6以积累为主,以峰5的转化生成最多;峰1、7、8、9分解或不易转移,峰2在不同批次中出现了不同的变化趋势。经过质谱指认峰3、4、5、6可能为当归醇类化合物,可能是经过水煮以后,发生了水解,导致含量升高。
研究过程中,采用多元的评价方法可更加全面对独活标准汤剂特征图谱进行分析,所得结果更加全面、直观,进一步确定此方法可用于独活标准汤剂的质量评价。
| [1] |
国家药典委员会编.中华人民共和国药典[S].北京: 中国医药科技出版社, 2015.
|
| [2] |
陈宇. 独活化学成分研究进展[J]. 辽宁中医药大学学报, 2014, 16(5): 255-256. |
| [3] |
张才煜, 张本刚, 杨秀伟. 独活化学成分的研究[J]. 解放军药学学报, 2007, 25(4): 241-245. DOI:10.3969/j.issn.1008-9926.2007.04.001 |
| [4] |
周刚, 马宝花. 中药独活的研究进展[J]. 中国当代医药, 2012, 19(16): 15-16. DOI:10.3969/j.issn.1674-4721.2012.16.006 |
| [5] |
陈士林, 刘安, 李琦, 等. 中药饮片标准汤剂研究策略[J]. 中国中药杂志, 2016, 41(8): 1367-1375. |
| [6] |
陈士林, 刘昌孝. 中药饮片标准汤剂(第一卷)[M]. 北京: 科学出版社, 2018.
|
| [7] |
药典委员会.中药配方颗粒质量控制与标准制定技术要求(征求意见稿)[S].北京: 人民卫生出版社, 2016.
|
| [8] |
高必兴, 兰志琼, 邓晶晶, 等. 白亮独活的HPLC指纹图谱[J]. 中国实验方剂学杂志, 2015, 21(8): 61-63. |
| [9] |
常艳旭, 朱子微, 李晋, 等. 高效液相色谱法同时测定独活中七种有效成分含量及在质量评价中应用(英文)[J]. 内蒙古大学学报(自然科学版), 2011, 42(2): 215-223. |
| [10] |
石燕红, 赵森淼, 王瑞, 等. RP-HPLC同时测定独活中蛇床子素和二氢欧山芹醇当归酸酯的含量[J]. 中国药学杂志, 2010(16): 156-163. |
| [11] |
孙东东, 徐晓芳, 严世海, 等. 独活水提部位化学成分的HPLC-ESI-Q-TOF-MS分析[J]. 天然产物研究与开发, 2014, 26(1): 69-76. |
| [12] |
简颖.丝瓜络抗氧化谱效关系研究[D].哈尔滨: 黑龙江大学, 2017.
|
| [13] |
费晓冬. 丹参等11种中药金属元素含量测定及聚类分析[J]. 光明中医, 2017, 32(14): 2042-2044. DOI:10.3969/j.issn.1003-8914.2017.14.026 |
| [14] |
武松, 潘发明. SPSS统计分析大全[M]. 北京: 清华大学出版社, 2014.
|
| [15] |
何军, 朱旭江, 杨平荣, 等. 中药配方颗粒的现状与发展新思路[J]. 中草药, 2018, 49(20): 4717-4725. DOI:10.7501/j.issn.0253-2670.2018.20.001 |
 2019, Vol. 38
2019, Vol. 38