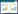文章信息
- 毛睿, 刘亚男, 李丽红, 田盼, 王迎, 窦志英, 王飘
- MAO Rui, LIU Yanan, LI Lihong, TIAN Pan, WANG Ying, DOU Zhiying, WANG Piao
- 麻黄饮片等级质量标准研究
- Study on the grade quality standard of Ephedra Sinica
- 天津中医药大学学报, 2019, 38(3): 274-278
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(3): 274-278
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.03.17
-
文章历史
收稿日期: 2019-01-20
麻黄为麻黄科植物草麻黄(Ephedra sinica Stapf)中麻黄(Ephedra intermedia Schrenk et C.A.Mey.)或木贼麻黄(Ephedra equisetina Bye.)的干燥草质茎,是一种常用中药,其性温,味辛、微苦,具有发汗解表、宣肺平喘、利水消肿的功能[1]。首载于《神农本草经》:“主中风,伤寒头痛,温疟,发表出汗,去邪热气,止咳逆上气,除寒热,破症坚积聚。”[2-3]麻黄的化学成分复杂,含有生物碱类、黄酮类、挥发油、有机酚酸、糖类及鞣质、单萜糖苷类、木脂素类等多种化学成分[4-5],药理作用丰富[6-7]。2015年版《中华人民共和国药典》(以下简称《中国药典》)规定以盐酸麻黄碱和盐酸伪麻黄碱的总质量分数不得少于0.80%作为麻黄质量控制的标准,而麻黄有诸多功效,且其量有限,导致市场混乱。
本研究共收集31个批次的麻黄饮片,依照《中国药典》进行浸出物、灰分、水分检测;采用HPLC测定31批麻黄饮片中麻黄碱和伪麻黄碱的含量;运用化学计量学,即利用计算机系统和相应的程序分析采集到的药材及饮片的总成分提取物的光谱、色谱数据以及某些经量化后的指标,获取用于中药材分析鉴别的有用信息,运用计算机代替人力对中药材进行分类和鉴别真伪。近年来CA、PCA及PLS-DA已广泛应用于中药质量评价[8-11]。建立两种无监督的化学模式识别方法:CA、PCA以及一种有监督的化学模式识别方法PLS-DA对麻黄饮片质量进行整体分析,初步阐述了麻黄饮片的质量等级分类标准,对临床安全用药及制剂、调剂都具有重要的意义。
1 实验材料与仪器 1.1 实验仪器HPLC高效(岛津LC-2010AHT,LC solution工作站),超声波清洗器KQ-250E(昆山市超声洗器有限公司),数显恒温水浴锅(金坛市科析仪器有限公司),FA2004电子分析天平(上海舜宇恒平科学仪器有限公司),FW100高速万能粉碎机(天津市泰斯特仪器有限公司)。
1.2 实验材料采集中国31个不同厂家批次的麻黄饮片,经天津中医药大学中药学院李天祥教授鉴定均为麻黄科植物草麻黄Ephdra sinica Stapf.的干燥草质茎,详见表 1。乙腈为色谱纯(SIGMA-ALORICH),水为娃哈哈纯净水,磷酸及三乙胺购自天津市化学试剂供销公司,麻黄碱对照品(No.171241-201508)、伪麻黄碱对照品(No.171237-2015010)购自中国药品生物制品检定所。
按2015年版《中国药典》通则0832项下水分测定中烘干法、通则2201项下冷浸法中水溶性浸出物测定法、通则2302项下总灰分测定法测定。31批麻黄饮片含水量范围为2.36%~5.33%;浸出物含量范围13.05%~28.11%;灰分含量范围为5.84%~8.94%,均符合2015年版《中国药典》的要求。
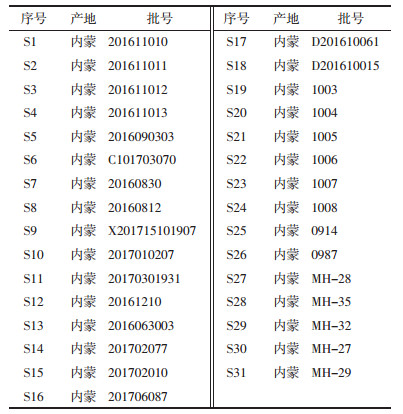
2.2 麻黄碱与伪麻黄碱含量测定 2.2.1 色谱条件色谱条件的选择,对《中国药典》2015年版1部的规定中麻黄药材的色谱条件进行优化,文献记录研究者采用乙腈:0.1%磷酸水溶液(3:97)为流动相,测定麻黄碱与伪麻黄碱,分离度良好。通过实践发现,流动相中加入0.1%的三乙胺,可以将麻黄碱、伪麻黄碱完全分离,且分离度良好。本实验采用色谱条件如下:色谱柱:Kromasil C18柱250 mm×4.6 mm,5.0 μm),流动相:0.1%磷酸溶液(0.1%三乙胺)(A)-乙腈(B)=96:4,等度洗脱,流速:1 mL/min,柱温:25 ℃,检测波长:210 nm,进样量10 μL。麻黄药材及标准品HPLC色谱图见图 1,分离效果很好。
|
| 1:麻黄碱;2:伪麻黄碱。 图 1 麻黄药材(A)和标准品(B)HPLC色谱图 |
精密称取盐酸麻黄碱对照品、盐酸伪麻黄碱对照品适量于100 mL容量瓶,加甲醇制得麻黄碱42 μg/mL、伪麻黄碱38 μg/mL的混合对照品溶液。
2.2.3 供试品溶液的制备取本品细粉约0.500 0 g,精密称定,置具塞锥形瓶中,精密加入1.44%磷酸溶液50 mL,称定质量,超声处理(功率600 W,频率50 kHz)20 min,放冷,再称定质量,用1.44%磷酸溶液补足失重,摇匀,滤过,取续滤液,即得。
2.3 方法学考察 2.3.1 线性关系分别精密移取盐酸麻黄碱、盐酸伪麻黄碱储备液适量,用甲醇稀释一系列浓度的对照品溶液,盐酸麻黄碱的浓度分别为,盐酸伪麻黄碱的浓度分别为,进样量10 μL,测定峰面积。以峰面积为纵坐标(
取“2.2.2”项下混标溶液,在“2.2.1”项下色谱条件下,连续进样6针,记录麻黄碱与伪麻黄碱的峰面积并计算RSD值。麻黄碱、伪麻黄碱RSD值分别为0.29%、0.62%。表明仪器精密度良好。
2.3.3 稳定性实验取同一供试品溶液,按“2.2.1”项下色谱条件在0、2、4、8、12 h分别进样,进样10 μL,记录峰面积并计算RSD值。麻黄碱与伪麻黄碱RSD值分别为2.14%,1.87%。表明样品溶液在室温条件下12 h内稳定。
2.3.4 重复性实验精密称取同一个样品6份,按“2.2.3”提取处理方法制备供试品溶液,在“2.2.1”项下色谱条件进行分析,记录峰面积,计算各对照品的质量分数,结果显示麻黄碱与伪麻黄碱RSD值分别为2.17%、2.15%,表明方法重复性良好。
2.3.5 加样回收率实验精密称取已知含量的麻黄饮片粉末9份,每份0.25 g,按照表加入对照品溶液。按“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件分析,结果见表 2。
将31批样品按“2.3.3”提取处理方法制备供试品溶液,在“2.2.1”项下色谱条件进行分析,测定峰面积,计算含量,结果见表 3。
运用SPSS 19.0软件对31批麻黄饮片进行系统聚类分析。本研究以其水分、灰分、浸出物、麻黄碱含量、伪麻黄碱含量和总含量为指标,采用组间连接法,利用欧式距离作为样品的测度,对数据进行分析,结果见图 4。本次系统聚类分析可分为两大类:S12、S13、S14、S15、S6、S30、S31分为一类,剩余为另一类,与PCA、PLS-DA分类一致,且S12、S13、S14、S15、S6、S30、S31麻黄饮片质量均一,麻黄碱、伪麻黄碱总含量较高。
|
| 图 4 31批麻黄饮片偏最小二乘法回归分析结果 |
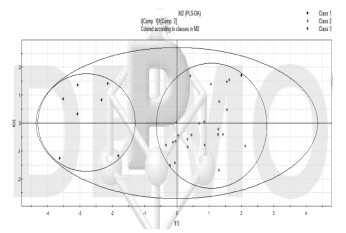
将31批麻黄饮片的水分、灰分、浸出物、麻黄碱含量、伪麻黄碱含量和两者总含量为分析变量,导入SIMCA-P 11.5统计软件进行主成分分析,主成份分析法作为数据挖掘的一种方法,将高维空间的问题转化到低维空间处理,在不损失或较少损失原有指标信息特征的情况下,将多个具有相关性的指标转换成少数几个相互独立的综合指标(即主成分),从而使繁多的求解目标简化[12],见图 2。采用主成份分析来描述生麻黄饮片质量的分布情况,根据特征值获取的结果两个主成份的累积贡献率达到了98.0%,其中PC1(即麻黄碱与伪麻黄碱总含量)贡献率达到了71.2%,为分类中的关键因素,能反映大部分质量信息。交叉验证系数为0.766,说明模型预测能力合理,见图 3。主成份分析分析结果表明,麻黄饮片可分为两类。

|
| 图 2 31批麻黄饮片聚类图 |

|
| 图 3 31批麻黄饮片主成份分析分结 |
主成份分析与聚类分析过程中能自动生成各主成份的权重,在很大程度上避免了人为因素在评价过程中的干扰;主成份分析能够找到隐藏在众多共性下的差异,对提取的数据进行客观充分的多元分析,因此两者能较好地保证评价结果的客观性。
2.4.2 有监督化学模式识别偏最小二乘法判别分析,是判别分析的多变量统计分析方法。判别分析是一种根据观察或测量到的若干变量值,来判断研究对象如何分类的常用统计分析方法。其原理是对不同处理样本(如观测样本、对照样本)的特性分别进行训练,产生训练集,并检验训练集的可信度。本研究将31批麻黄饮片的水分、灰分、浸出物、麻黄碱含量、伪麻黄碱含量和两者总含量为分析变量,导入SIMCA-P 11.5统计软件进行偏最小二乘回归的计算,建立有监督的模式识别模型偏最小二乘法判别分析,根据软件自动拟合31批麻黄饮片的质量信息,将31批麻黄饮片分为两类,可验证主成份分析结果,得散点图 4,本实验所拟合的模型解释能力参数R2X=0.705,R2Y=0.809,预测能力参数Q=0.788,表示所建模型稳定、合理。故由以上实验结果可将麻黄饮片分为两个等级。
3 讨论与结论本研究共收集了31批麻黄饮片,建立优化的HPLC含量测定条件,增加水溶性浸出物作为检测指标,并依据2015年版《中国药典》进行了水分、灰分以及水溶性浸出物含量测定,初步评价了麻黄饮片的质量。但目前《中国药典》仅规定了药材的合格标准,而优质的中药饮片是生产优质中成药的必要条件,因此,制定药材的等级标准势在必行。研究采用两种无监督的化学模式识别模型将麻黄饮片分为两类,由主成份分析给出麻黄碱与伪麻黄碱总含量为优质分类的关键因素,且水分、灰分、浸出物受人为影响较大,故本实验以麻黄碱与伪麻黄碱的总含量为分级标准将31批麻黄饮片分为两个等级,优等:麻黄碱及伪麻黄碱总含量≥2.6%;统货:麻黄碱及伪麻黄碱总含量在0.8%~2.6%。并利用偏最小二乘法判别分析进一步验证,以科学、客观的质量评价标准,取代以往仅凭外观、经验等主观的质量评价方法,对于有效监控饮片质量具有现实意义[13]。本实验只对麻黄中草麻黄的麻黄饮片进行了研究,拟定的各项指标限量在蜜炙麻黄以及木贼麻黄和中麻黄中有待进一步研究。
| [1] |
国家药典委员会.中华人民共和国药典(一部)[S].北京: 中国医药科技出版社, 2015.
|
| [2] |
杨继荣, 王艳宏, 关枫. 麻黄本草考证概览[J]. 中医药学报, 2010, 38(2): 51-52. DOI:10.3969/j.issn.1002-2392.2010.02.020 |
| [3] |
陈利平, 孙志高, 王发渭, 等. 麻黄临床功用探悉[J]. 中华中医药学刊, 2012, 30(7): 1576-1578. |
| [4] |
周玲, 吴德康, 唐于平, 等. 麻黄中化学成分研究进展[J]. 南京中医药大学学报, 2008, 24(1): 71-72,74. DOI:10.3969/j.issn.1000-5005.2008.01.025 |
| [5] |
赵巍.草麻黄化学成分研究[D].北京: 中国协和医科大学, 2009.
|
| [6] |
丁丽丽, 施松善, 崔健, 等. 麻黄化学成分与药理作用研究进展[J]. 中国中药杂志, 2006, 31(20): 1661-1664. DOI:10.3321/j.issn:1001-5302.2006.20.001 |
| [7] |
范彦博.麻黄中非生物碱类成分活性研究[D].武汉: 湖北中医药大学, 2010.
|
| [8] |
郝燕, 董鸿晔, 姜楠, 等. 基于主成分分析的中药色谱指纹图谱多维多息特征数据挖掘方法研究[J]. 中南药学, 2007, 5(3): 267-272. DOI:10.3969/j.issn.1672-2981.2007.03.024 |
| [9] |
戴晓燕, 盛振华, 郝云云, 等. 不同产地大黄中微量元素含量的主成分分析及聚类分析[J]. 中华中医药杂志, 2012, 27(5): 1445-1448. |
| [10] |
Isabella E, Flavia G, Marit R, et al. Interpretation, valida-tion and segmentation of preference mapping models[J]. Food Quality and Preference, 2014, 32: 302. |
| [11] |
窦婷, 欧阳慧子, 王兴蕊, 等. HPLC-MS/MS法测定大鼠血浆中麻黄碱、伪麻黄碱浓度及药动学研究[J]. 天津中医药大学学报, 2014, 33(6): 355-358. |
| [12] |
陈军辉, 谢明勇, 王凤美, 等. 聚类分析法用于西洋参样品分类研究[J]. 分析测试学报, 2006, 25(2): 20-24,28. DOI:10.3969/j.issn.1004-4957.2006.02.006 |
| [13] |
覃洁萍, 王智猛, 李梦龙. 化学计量学方法在中药鉴别及质量控制方面的应用[J]. 数理医药学杂志, 2004, 17(4): 351-355. DOI:10.3969/j.issn.1004-4337.2004.04.035 |
 2019, Vol. 38
2019, Vol. 38