文章信息
- 瞿璐, 王剑丽, 黄培建, 燕洁静, 王涛, 张祎
- QU Lu, WANG Jianli, HUANG Peijian, YAN Jiejing, WANG Tao, ZHANG Yi
- 莫哈韦丝兰化学成分的研究
- Study on the constituents of Yucca schidigera Roezl (Mojave)
- 天津中医药大学学报, 2019, 38(3): 279-283
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(3): 279-283
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.03.18
-
文章历史
收稿日期: 2019-02-03
莫哈韦丝兰[Yucca schidigera Roezl(Mojave),简称丝兰],为龙舌兰科(Agavaceae)丝兰属(Yucca)常绿灌木[1],主要分布于美国西南、墨西哥北方沙漠。该植物富含甾体皂苷及酚酸类化学成分[2]。因具有较强的生物活性及较好的安全性,丝兰提取物已通过美国食品药品监督管理局(FDA)认证。作为一种民间用药,印第安人称它为“生命之树”。现代药理学研究表明,丝兰提取物具有调节能量代谢和改善动物养殖环境等多种作用[3-4]。文献调研工作发现,该植物的化学成分研究缺乏系统性,极大程度上限制了它的进一步开发与利用。
本实验应用多种色谱技术,对丝兰70%乙醇提取物的化学成分进行了系统分离制备,并利用与文献类似的方法[5-6],鉴定了14个单体成分,分别为咖啡酸(1),β-羟基-3-甲氧基-4-羟基苯乙酮(2)、1-O-β-D-glucopyranosyl-2-hydroxy-4-allylbenzene(3)、2-O-(4-hydroxybenzoyl)-2,4,6-trihydroxyphenylacetic acid(4)、对羟基苯甲酸(5)、原儿茶酸(6)、4-羟基-3-甲氧基苯甲酸(7)、丁香酸(8)、对羟基苯甲醛(9)、原儿茶醛(10)、麦芽酚(11)、5-hydroxymaltol(12)、5-羟甲基糠醛(13)和4,4-二甲基-1,7-庚二酸(14)。其中,2~4、7~14为首次从丝兰属植物中分离得到的化合物,5、6为首次从该种植物中分离得到的化合物。
1 实验材料与仪器正相柱色谱用硅胶(48~75 μm,青岛海洋化工厂);薄层色谱硅胶预板、高效硅胶GF254(天津思利达科技有限公司);ODS(YMCGel ODS-A-HG,S~50 μm,日本YMC株式会社);Sephadex LH-20(瑞典Ge Healthcare Bio-Sciences AB公司);D101大孔吸附树脂(净品级,天津海光化工有限公司);氘代甲醇(北京崇熙科技孵化器公司);HPLC用分析柱/制备柱型号分别为Cosmosil 5C18-MS-Ⅱ(4.6 mm × 250 mm,5 μm/20 mm × 250 mm,5 μm,日本Nacalai Tesque公司);Wakopak Navi C30-5(4.6 mm × 250 mm,5 μm/7.5 mm × 250 mm,5 μm,日本Wako Pure Chemical公司)。
二氯甲烷、甲醇、乙腈、丙酮、冰醋酸等试剂(色谱纯或分析纯)购自天津康科德科技有限公司。
莫哈韦丝兰药材采自美国东南部弗罗里达州,由天津中医药大学李天祥教授鉴定为龙舌兰科丝兰属莫哈韦丝兰[Yucca schidigera Roezl(Mojave)]的干燥茎。
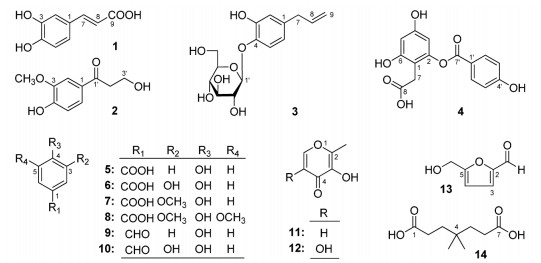
2 提取与分离丝兰干燥粉末(5.0 kg)经70%乙醇溶液依次加热回流提取,得浸膏800.0 g。上述浸膏(700.0 g)经D101大孔吸附树脂柱色谱分离(H2O→95% EtOH),得到H2O洗脱物(380.0 g)和95%乙醇洗脱物(310.0 g)。95%乙醇洗脱物(200.0 g)经硅胶柱色谱分离[CH2Cl2→CH2Cl2-MeOH(100:1→100:3→100:7→5:1→3:1→2:1→0:100),v/v],得到13个组分(Fr. 1~Fr. 13)。Fraction 3(7.5 g)经Sephadex LH-20凝胶柱色谱分离[CH2Cl2-MeOH(1:1,v/v)],得到8个组分(Fr. 3-1~Fr. 3-8)。Fraction 3-5(350.0 mg)经PHPLC分离制备[MeOH-H2O(40:60,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到6个组分(Fr. 3-5-1~Fr. 3-5-6)。Fraction 3-5-6(20.1 mg)经PHPLC分离制备[MeOH-H2O(40:60,v/v)+1% HAc,Wakopak Navi C30-5 column],得到β-羟基-3-甲氧基-4-羟基苯乙酮(2,5.0 mg)和4-羟基-3-甲氧基苯甲酸(7,8.2 mg)。Fraction 3-6(915.8 mg)经PHPLC分离制备[CH3CN-H2O(10:90,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到丁香酸(8,29.5 mg)、对羟基苯甲醛(9,21.0 mg)和5-羟甲基糠醛(13,66.9 mg)。Fraction 3-6-2(26.6 mg)经PHPLC分离制备[MeOH-H2O(15:85,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到麦芽酚(11,10.7 mg)和5-hydroxymaltol(12,6.0 mg)。Fraction 3-6-5(30.1 mg)经PHPLC分离制备[MeOH-H2O(40:60,v/v)+1% HAc,Wakopak Navi C30-5 column],得到β-羟基-3-甲氧基-4-羟基苯乙酮(2,2.5 mg)和4-羟基-3-甲氧基苯甲酸(7,2.2 mg)。Fraction 4(4.1 g)经Sephadex LH-20凝胶柱色谱分离[CH2Cl2-MeOH(1:1,v/v)],得到7个组分(Fr. 4-1~Fr. 4-7)。Fraction 4-3(1.4 g)经PHPLC分离制备[MeOH-H2O(40:60,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到7个组分(Fr. 4-3-1~Fr. 4-3-7)。Fraction 4-3-6(31.6 mg)经PHPLC分离制备[CH3CN-H2O(26:74,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到4,4-二甲基-1,7-庚二酸(14,14.7 mg)。Fraction 4-5(777.7 mg)经PHPLC分离制备[MeOH-H2O(25:75,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到4个组分(Fr. 4-5-1~Fr. 4-5-4)。其中Fraction 4-5-1经鉴定为5-hydroxymaltol(12,23.0 mg)。Fraction 4-5-2(20.0 mg)经PHPLC分离制备[CH3CN-H2O(14:86,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到原儿茶醛(10,10.0 mg)。Fraction 4-5-3(258.3 mg)经PHPLC分离制备[CH3CN-H2O(14:86,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到对羟基苯甲酸(5,180.3 mg)。Fraction 5(3.2 g)经ODS柱色谱分离[MeOH-H2O(10:90→20:80→30:70→40:60→50:50→60:40→70:30→80:20→100:0,v/v)],得到12个组分(Fr. 5-1~Fr. 5-12)。Fraction 5-2(116.4 mg)经Sephadex LH-20凝胶柱色谱分离(MeOH)以及PHPLC分离制备[MeOH-H2O(15:85,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到原儿茶酸(6,20.8 mg)。Fraction 5-4(228.6 mg)经Sephadex LH-20凝胶柱色谱分离(MeOH)及PHPLC分离制备[MeOH-H2O(30:70,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到咖啡酸(1,40.7 mg)。Fraction 6(12.0 g)经ODS柱色谱分离[MeOH-H2O(30:70→40:60→50:50→60:40→70:30→80:20→100:0,v/v)],得到14个组分(Fr. 6-1~Fr. 6-14)。Fraction 6-5(253.1 mg)经PHPLC分离制备[MeOH-H2O(35:65,v/v)+1% HAc,Cosmosil 5C18-MS-Ⅱ column],得到1-O-β-D-glucopyranosyl-2-hydroxy-4-allylbenzene(3,33.0 mg)和2-O-(4-hydroxybenzoyl)-2,4,6-trihydroxyphenylacetic acid(4,14.3 mg)。化合物结构如图 1。
|
| 图 1 化合物1-14的结构 |
化合物1:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 181.049 4[M+H]+(calcd for C9H9O4,181.049 5),确定其分子式为C9H8O4。1H NMR(CD3OD,500 MHz)δ:7.05(1H,d,J=2.0 Hz,H-2),6.79(1H,d,J=8.0 Hz,H-5),6.94(1H,dd,J=2.0、8.0 Hz,H-6),7.55(1H,d,J=16.0 Hz,H-7),6.23(1H,d,J=16.0 Hz,H-8)。13C NMR(CD3OD,125 MHz)δ:127.9(C-1),115.2(C-2),146.8(C-3),149.4(C-4),116.5(C-5),122.9(C-6),147.0(C-7),115.7(C-8),171.2(C-9)。其1H、13C NMR谱数据与文献[7]相对照,鉴定该化合物的结构为咖啡酸(caffeic acid)。
化合物2:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 197.081 0[M+H]+(calcd for C10H13O4,197.080 8),确定其分子式为C10H12O4。1H NMR(CD3OD,500 MHz)δ:7.55(1H,d,J=2.0 Hz,H-2),6.85(1H,d,J=8.0 Hz,H-5),7.57(1H,d,J=2.0、8.0 Hz,H-6),3.16(2H,t,J=6.0 Hz,H2-2′),3.94(2H,t,J=6.0 Hz,H2-3′),3.90(3H,s,3-OCH3)。13C NMR(CD3OD,125 MHz)δ:130.5(C-1),112.0(C-2),149.4(C-3),153.6(C-4),115.9(C-5),124.9(C-6),199.8(C-1′),41.7(C-2′),59.0(C-3′),56.4(3-OCH3)。其1H NMR谱数据与文献[8]相对照,鉴定该化合物的结构为β-羟基-3-甲氧基-4-羟基苯乙酮(β-hydroxypropiovanllone)。
化合物3:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 311.113 6[M-H]-(calcd for C15H19O7,311.113 6),确定其分子式为C15H20O7。1H NMR(CD3OD,500 MHz)δ:6.67(1H,d,J=2.0 Hz,H-3),6.60(1H,dd,J=2.0、8.0 Hz,H-5),7.09(1H,d,J=8.0 Hz,H-6),3.26(2H,br. d,ca. J=7 Hz,H2-7),5.91(1H,ddt,J=7.0、10.5、17.0 Hz,H-8),[5.01(1H,ddd,J=1.5、3.5、10.5 Hz),5.03(1H,ddd,J=1.5、3.5、17.0 Hz),H2-9],4.70(1H,d,J=7.5 Hz,H-1′),3.49(1H,dd,J=7.5、9.0 Hz,H-2′),3.47(1H,dd,J=7.5、9.0 Hz,H-3′),3.41(1H,m,overlapped,H-4′),3.41(1H,m,overlapped,H-5′),[3.71(1H,dd,J=5.0、12.0 Hz),3.89(1H,dd,J=2.0、12.0 Hz),H2-6′]。13C NMR(CD3OD,125 MHz)δ:145.2(C-1),148.4(C-2),117.3(C-3),137.2(C-4),121.0(C-5),119.0(C-6),40.6(C-7),139.1(C-8),115.8(C-9),104.7(C-1′),74.9(C-2′),77.6(C-3′),71.3(C-4′),78.3(C-5′),62.4(C-6′)。其1H、13C NMR谱数据与文献[9]相对照,鉴定该化合物的结构为1-O-β-D-glucopyranosyl-2-hydroxy-4-allylbenzene,并结合2D NMR谱的解析,对文献中C-3和C-6、C-3′和C-5′之间的化学位移值进行了调换。
化合物4:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 303.051 6[M-H]-(calcd for C15H11O7,303.051 0),确定其分子式为C15H12O7。1H NMR(CD3OD,500 MHz)δ:6.17(1H,d,J=2.5 Hz,H-3),6.26(1H,d,J=2.5 Hz,H-5),3.46(2H,s,H2-7),8.00(2H,d,J=8.5 Hz,H-2′,6′),6.88(2H,d,J=8.5 Hz,H-3′,5′)。13C NMR(CD3OD,125 MHz)δ:107.6(C-1),158.5(C-2),101.2(C-3),158.5(C-4),102.1(C-5),152.4(C-6),30.2(C-7),176.0(C-8),121.5(C-1′),133.5(C-2′,6′),116.5(C-3′,5′),164.2(C-4′),166.3(C-7′)。其1H、13C NMR谱数据与文献[10]相对照,鉴定该化合物的结构为2-O-(4-hydroxybenzoyl)-2,4,6-trihydroxyphenylacetic acid,并结合2D NMR谱的解析,对文献中H-3和H-5之间的化学位移值进行了调换。
化合物5:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 139.039 5[M+H]+(calcd for C7H7O3,139.039 0),确定其分子式为C7H6O3。1H NMR(CD3OD,500 MHz)δ:7.94(2H,d,J=9.0 Hz,H-2,6),6.87(2H,d,J=9.0 Hz,H-3,5)。13C NMR(CD3OD,125 MHz)δ:122.7(C-1),133.1(C-2,6),116.1(C-3,5),163.3(C-4),170.4(C-7)。其1H、13C NMR谱数据与文献[11]相对照,鉴定该化合物的结构为p-hydroxyl benzoic acid。
化合物6:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 155.034 1[M+H]+(calcd for C7H7O4,155.033 9),确定其分子式为C7H6O4。1H NMR(CD3OD,500 MHz)δ:7.44(1H,d,J=2.0 Hz,H-2),6.80(1H,d,J=8.0 Hz,H-5),7.43(1H,dd,J=2.0、8.0 Hz,H-6)。13C NMR(CD3OD,125 MHz)δ:123.3(C-1),117.8(C-2),146.1(C-3),151.6(C-4),115.8(C-5),123.9(C-6),170.4(C-7)。其1H、13C NMR谱数据与文献[12]相对照,鉴定该化合物的结构为原儿茶酸(protocatechuic acid)。
化合物7:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 169.049 9[M+H]+(calcd for C8H9O4,169.049 5),确定其分子式为C8H8O4。1H NMR(CD3OD,500 MHz)δ:7.56(1H,d,J=2.0 Hz,H-2),6.83(1H,d,J=8.5 Hz,H-5),7.55(1H,dd,J=2.0、8.5 Hz,H-6),3.89(3H,s,3-OCH3)13C NMR(CD3OD,125 MHz)δ:123.5(C-1),113.9(C-2),148.7(C-3),152.6(C-4),115.9(C-5),125.3(C-6),170.4(C-7),56.5(3-OCH3)。其1H、13C NMR谱数据与文献[13]相对照,鉴定该化合物的结构为4-羟基-3-甲氧基苯甲酸(4-hydroxy-3-methoxybenzoic acid)。
化合物8:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 199.060 1[M+H]+(calcd for C9H11O5,199.060 1),确定其分子式为C9H10O5。1H NMR(CD3OD,500 MHz)δ:7.33(2H,s,H-2,6),3.88(6H,s,3,5-OCH3)。13C NMR(CD3OD,125 MHz)δ:122.2(C-1),108.4(C-2,6),148.9(C-3,5),141.7(C-4),170.2(C-7),56.8(3,5-OCH3)。其1H、13C NMR谱数据与文献[14]相对照,鉴定该化合物的结构为丁香酸(syringic acid)。
化合物9:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 123.043 9[M+H]+(calcd for C7H7O2,123.044 1),确定其分子式为C7H6O2。1H NMR(CD3OD,500 MHz)δ:7.76(2H,d,J=8.5 Hz,H-2,6),6.91(2H,d,J=8.5 Hz,H-3,5),9.76(1H,s,H-7)。13C NMR(CD3OD,125 MHz)δ:130.2(C-1),133.5(C-2,6),117.0(C-3,5),165.5(C-4),192.8(C-7)。其1H、13C NMR谱数据与文献[15]相对照,鉴定该化合物的结构为对羟基苯甲醛(p-hydroxy-benzaldehyde)。
化合物10:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 139.039 2[M+H]+(calcd for C7H7O3,139.039 0),确定其分子式为C7H6O3。1H NMR(CD3OD,500 MHz)δ:7.30(1H,d,J=2.0 Hz,H-2),6.90(1H,d,J=8.0 Hz,H-5),7.31(1H,dd,J=2.0、8.0 Hz,H-6),9.69(1H,s,H-7)。13C NMR(CD3OD,125 MHz)δ:130.9(C-1),115.4(C-2),147.3(C-3),153.9(C-4),116.3(C-5),126.4(C-6),193.1(C-7)。其1H、13C NMR谱数据与文献[16]相对照,鉴定该化合物的结构为原儿茶醛(protocatechuic aldehyde),并结合2D NMR谱的解析,对文献中C-2和C-5之间的化学位移值进行了调换。
化合物11:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 127.039 1[M+H]+(calcd for C6H7O3,127.039 0),确定其分子式为C6H6O3。1H NMR(CD3OD,500 MHz)δ:6.38(1H,d,J=5.5 Hz,H-5),7.93(1H,d,J=5.5 Hz,H-6),2.34(3H,s,2-CH3)。13C NMR(CD3OD,125 MHz)δ:152.3(C-2),144.8(C-3),175.4(C-4),114.4(C-5),156.3(C-6),14.3(2-CH3)。其1H、13C NMR谱数据与文献[17]相对照,鉴定该化合物的结构为麦芽酚(maltol)。
化合物12:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 143.034 0[M+H]+(calcd for C6H7O4,143.033 9),确定其分子式为C6H6O4。1H NMR(CD3OD,500 MHz)δ:7.85(1H,s,H-6),2.31(3H,s,2-CH3)。13C NMR(CD3OD,125 MHz)δ:151.7(C-2),143.0(C-3),170.4(C-4),145.9(C-5),140.4(C-6),14.6(2-CH3)。其1H、13C NMR谱数据与文献[18]相对照,鉴定该化合物的结构为5-hydroxymaltol。
化合物13:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 127.038 6[M+H]+(calcd for C6H7O3,127.039 0),确定其分子式为C6H6O3。1H NMR(CD3OD,500 MHz)δ:7.38(1H,d,J=4.0 Hz,H-3),6.58(1H,d,J=4.0 Hz,H-4),9.53(1H,s,H-CHO),4.62(2H,s,5-CH2OH)。13C NMR(CD3OD,125 MHz)δ:153.9(C-2),124.9(C-3),110.9(C-4),163.2(C-5),179.5(2-CHO),57.7(5-CH2OH)。其1H、13C NMR谱数据与文献[19]相对照,鉴定该化合物的结构为5-羟甲基糠醛(5-hydroxy methyl furfura)。
化合物14:白色粉末。高分辨Q-TOF-ESI-MS给出其准分子离子峰m/z 189.111 7[M+H]+(calcd for C9H17O4,189.112 1),确定其分子式为C9H16O4。1H NMR(CD3OD,500 MHz)δ:2.28(4H,t,J=7.0 Hz,H2-2,6),1.60(4H,t,J=7.0 Hz,H2-3,5),1.35(6H,s,H3-8,9)。13C NMR(CD3OD,125 MHz)δ:177.8(C-1,7),35.0(C-2,6),30.1(C-3,5),26.1(C-4,8,9)。其1H、13C NMR谱数据与文献[20]相对照,鉴定该化合物的结构为4,4-二甲基-1,7-庚二酸(4,4-dimethyl-1,7-pimelic acid)。
4 结果与讨论丝兰在观赏、医药、饲料、净化环境等方面均有独特应用,但目前国内外对其物质基础研究尚不深入具体,限制了它的进一步开发及应用。本研究应用多种色谱及波谱学技术,对丝兰70%乙醇提取物的化学成分进行了系统分离制备及结构鉴定。首次从该植物中分离得到的化合物5、6及首次从丝兰属中分离得到的化合物2~4、7~14为该植物乃至丝兰属植物化学成分的研究进行了补充,也为丝兰的进一步研究与开发奠定了物质基础。
| [1] |
Sastre F, Ferreira F, Pedreschi F. A systematic approach for the chromatographic fractionation and purification of major steroid saponins in commercial extracts of Yucca schidigera Roezl[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2017, 1046: 235-242. DOI:10.1016/j.jchromb.2016.11.032 |
| [2] |
Cheeke PR. Actual and potential applications of Yucca schidigera and Quillaja saponaria saponins in human and animal nutrition[J]. J Anim Sci, 2000, 77(E-Suppl): 1-10. |
| [3] |
Kucukkurt I, Akkol EK, Karabag F, et al. Determination of the regulatory properties of Yucca schidigera, extracts on the biochemical parameters and plasma hormone levels as-sociated with obesity[J]. Rev Bras Farmacogn, 2016, 26(2): 246-250. DOI:10.1016/j.bjp.2015.12.005 |
| [4] |
Xu M, Rinker M, Mcleod KR, et al. Yucca schidigera ex-tract decreases in vitro methane production in a variety of forages and diets[J]. Anim Feed Sci Technol, 2010, 159(1-2): 18-26. DOI:10.1016/j.anifeedsci.2010.05.005 |
| [5] |
瞿璐, 刘艳霞, 李建良, 等. 祁菊叶化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2017, 36(1): 57-60. |
| [6] |
董勇喆, 史文中, 杨圣财, 等. 沙葱化学成分的分离与结构鉴定[J]. 天津中医药大学学报, 2016, 35(6): 404-408. |
| [7] |
欧徐涵, 况燚, 吴学谦, 等. 青钱柳叶子化学成分的研究[J]. 中草药, 2017, 48(23): 4480-4484. |
| [8] |
李锟, 郝志友, 张翠利, 等. 杜仲化学成分研究[J]. 中药材, 2016, 39(9): 2016-2018. |
| [9] |
Ly TN, Yamauchi R, Shimoyamada M, et al. Isolation and structural elucidation of some glycosides from the rhizomes of smaller galanga (Alpinia officinarum Hance)[J]. J Agric Food Chem, 2002, 50(17): 4919-4924. DOI:10.1021/jf025529p |
| [10] |
Hillenbrand M, Zapp J, Becker H. Depsides from the petals of Papaver rhoeas[J]. Planta Med, 2004, 70(4): 380-382. DOI:10.1055/s-2004-818956 |
| [11] |
陈斌, 蔡巍, 刘芳, 等. 脉络宁注射液的化学成分研究(Ⅰ)[J]. 中南药学, 2016, 14(3): 239-242. |
| [12] |
袁胜浩, 卞金辉, 谢珍, 等. 大半边莲中酚酸类成分与抑菌活性研究[J]. 中成药, 2013, 35(1): 170-172. |
| [13] |
马宁宁, 陈光英, 宋小平, 等. 匍匐滨藜的化学成分[J]. 中成药, 2013, 35(5): 982-985. DOI:10.3969/j.issn.1001-1528.2013.05.028 |
| [14] |
张艳军, 聂辉, 周德雄, 等. 桂野桐化学成分的研究[J]. 中草药, 2017, 48(11): 2172-2176. |
| [15] |
谭冰心, 彭光天, 于思, 等. 毛麝香的化学成分研究[J]. 中草药, 2017, 48(10): 2024-2027. DOI:10.7501/j.issn.0253-2670.2017.10.016 |
| [16] |
赵珊, 张宝, 熊丹丹, 等. 苗药黑骨藤的化学成分研究[J]. 中草药, 2017, 48(8): 1513-1518. |
| [17] |
孙朋悦, 徐颖, 文晔, 等. 朝鲜淫羊藿的化学成分Ⅱ[J]. 中国药物化学杂志, 1998, 8(4): 281-284. |
| [18] |
Shinoda Y, Murata M, Homma S, et al. Browning and de-composed products of model orange juice[J]. Biosci Biotechnol Biochem, 2004, 68(3): 529-536. DOI:10.1271/bbb.68.529 |
| [19] |
付丽娜, 陈兰英, 刘荣华, 等. 白茅根的化学成分及其抗补体活性[J]. 中药材, 2010, 33(12): 1871-1874. |
| [20] |
崔晓东, 梁侨丽, 孔丽娟, 等. 荆三棱块茎的化学成分研究[J]. 中国药学杂志, 2012, 47(24): 1987-1989. |
 2019, Vol. 38
2019, Vol. 38