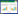文章信息
- 温利娟, 薛晓鸥, 米鑫, 谢伟
- WEN Lijuan, XUE Xiaoou, MI Xin, XIE Wei
- 清热利湿外治法对宫颈癌荷瘤裸鼠抗肿瘤作用与MARK信号通路的关系
- Relationship between anti-tumor effect and MARK signaling pathway in nude mice bearing cervical cancer treated with Qingre Lishi
- 天津中医药大学学报, 2019, 38(6): 578-582
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(6): 578-582
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.06.16
-
文章历史
收稿日期: 2019-08-28
2. 北京中医药大学东直门医院, 北京 100700
2. Dongzhimen Hospital of Beijing University of Chinese Medicine, Beijing 100700, China
宫颈癌是最常见的妇科恶性肿瘤,在女性恶性肿瘤中排名第三,且85%以上新发及死亡病例出现在发展中国家,中国是世界上宫颈癌高发国家,患病和死亡人数占全世界1/4[1]。目前,宫颈癌常用的西医治疗方法为手术治疗和放疗,辅助方法有化疗[2]。在宫颈癌治疗中,中医药治疗尚不能替代手术、放疗及化疗等治疗方法。但是在手术、放疗、化疗过程中,根据患者个体差异,采用望、闻、问、切四诊合参,辨证论治后用内服外用的中医治疗方法以扶正祛邪,能够稳定瘤体,有利于术后患者恢复,提升患者自身免疫力,提高生活质量,延长生存期,减轻患者在放化疗过程中的毒副作用,以利于治疗的顺利进行,有减毒增效之优势[3]。中医学中并无宫颈癌病名,根据其临床表现,归属于中医“癥瘕病”、“崩漏”、“带下”等病范畴。中医学认为本病的主要病机是正气虚弱,邪毒客于子门,瘀结胞中。“清热利湿外治法”前期临床及实验研究已经表明:能改善阴道局部免疫微环境,上调HLA-I和CD8分子的表达而增强机体对病毒免疫杀伤功能而起到抑制HR-HPV作用[4-9]。
ERK及P38是丝裂原活化蛋白激酶(MAPK)家族成员之一,ERK家族有5个亚族,包括ERK1-ERK5。其中ERK1及ERK2通路中的两个重要成员之一;主要参与并调节了细胞的生长、发育、分化、分裂及死亡等多种生理过程,并且在细胞的恶性转化中起着重要的作用。ERK及P38在肿瘤发生发展和防治中起着重要的作用,是目前肿瘤研究的重要热点。
本实验研究清热利湿法体外抗肿瘤作用及机制,测量肿瘤体积及体质量,计算抑瘤率,HE染色法观察肿瘤的形态学变化,并运用免疫组化方法,检测瘤体中p-ERK及p-p38蛋白表达水平,研究清热利湿外治法对宫颈癌荷瘤裸鼠的抑瘤作用,进一步揭示其抗肿瘤作用机制。
1 材料与方法 1.1 实验动物SPF级BALB/c(nu/nu)裸小鼠35只,雌性,5~6周龄,体质量SPF级BALB/cnu/nu,购于维通利华实验动物中心。饲养条件:SPF级BALB/c(nu/nu)裸小鼠均由实验动物中心SPF屏障系统的洁净层流架内,医学实验动物使用许可证编号:SCXK(京)2012-0001。实验室相对湿度为50%~70%,动物室温为(24±2)℃,采用12 h昼夜间断照明,水料自由饮用。
1.2 受试药物外用中药方由百川飞虹技术有限公司生产,注射用顺铂购自齐鲁制药有限公司,Anti-Human Papillomavirus 16(E7)antibody、Anti-ERK1+ERK2 antibody、Goat Anti-Rabbit IgG、Goat Anti-Mouse IgG、Anti-Human Papillomavirus 16(E6)+ 18(E6)antibody、Anti-Rb antibody、Anti-P53 antibody均购自abcam,免疫组化试剂盒购自北京中衫生物科技有限公司。
1.3 宫颈癌细胞株宫颈癌Siha细胞株,购自上海复祥生物科技有限公司。
1.4 主要仪器细胞培养箱(Thermo公司);酶标仪(Thermo公司);倒置显微镜(Nikon);生物洁净使用超净台(Opti MAIR);低速离心机(安徽中科中佳科学仪器有限公司);游标卡尺(SYNTEK);高精度电子称重天平(Ei)。
2 方法 2.1 宫颈癌Siha细胞悬液制备宫颈癌Siha细胞株复苏后行细胞培养。培养条件是含10%胎牛血清、100 mg/mL链霉素和100 IU/m青霉素的DMEM培养液,置于37 ℃、5% CO2饱和湿度培养箱内培养。取对数生长期细胞,用2.5%胰酶消化,离心,弃上清。培养基悬浮沉淀细胞,计数后调整细胞浓度2×107/mL。
2.2 动物与分组35只裸小鼠随机分为清热利湿外治法高剂量组、中剂量、低剂量、顺铂组、空白对照组。裸鼠购买后,预先在室内常规饲养,观察3天。每只裸鼠用0.5 mL注射器将0.2 mL浓度为2×107/mL的细胞悬液在无菌条件下皮下注射于裸鼠右前肢腋窝处皮下。在无特定病原体(SPF)环境饲养裸鼠,并观察裸鼠生长状态及肿瘤生长情况,以皮下结节直径>0.5 cm为成瘤标准。裸鼠成瘤后,将裸鼠称重,用随机数字表法分成5组,每组7只,进行给药。
2.3 各组给药方法① 外用中药方高剂量组:0.942 8 mg/kg;②中剂量组:0.471 4 mg/kg;③低剂量组:0.235 7 g/kg;④顺铂组:浓度为5 mg/kg,用量为0.5 mL,腹腔内注射,每4天1次;⑤空白对照组:不用药物观察。清热利湿外治法各组均使用无菌棉签将药物涂抹在裸鼠瘤体表面,每日一次。各组用药和观察时间均为4周。
2.4 观察指标每日观察裸鼠精神状态、活动力、反应、饮食、排便情况、皮下种植区外观及触感,每日用药前测量裸鼠瘤体的长径(a)和短径(b),测量裸鼠体质量。治疗过程中死亡裸鼠,均行解剖以明确死因。停药24小时后,用裸鼠颈椎脱臼法处死裸鼠,剥取瘤组织,并瘤组织称重、进行体积测量,计算抑瘤率。肿瘤体积(V)=ab2/2,抑瘤率=[(对照组平均瘤重-治疗组平均瘤重)÷对照组平均瘤重]×100%。
2.5 HE染色1)二甲苯2次去蜡处理,每次15 min。2)将切片进行清洗:100%乙醇5 min共2次,80%乙醇5 min 1次,蒸馏水5 min 1次。3)苏木精液染色5 min。4)流水冲洗5 min,1%盐酸乙醇30 sec,水洗30 sec,蒸馏水过洗5次。5)0.5%伊红液染色3 min,蒸馏水稍洗30 sec,80%乙醇稍洗30 sec,95%乙醇1 min 2次,无水乙醇3 min 2次,二甲苯3 min 2次。6)中性树胶封固。
2.6 免疫组化SP法第一天:将切片放入37 ℃烘培箱内30 min,取出后室温放置10 min;脱蜡:将切片放入纯二甲苯中脱蜡3次,每次15 min;将切片放入100%酒精2次,每次10 min;将切片放入90%酒精2次,每次10 min;将切片放入80%酒精1次,每次10 min;将切片放入70%酒精1次,每次10 min;将切片放入蒸馏水中3 min;将切片放入PBS中3次,每次3 min;灭活:双氧水直接滴加,室温内放置10 min;PBS洗3次,每次3 min;热修复抗原:将切片浸入枸橼酸盐缓冲液中,大火煮沸3 min;室温内静置2 h直至完全冷却,PBS洗3次,每次3 min;滴加5%BSA封闭液,室温放置20 min;滴加一抗,将切片放入湿盒中,4 ℃冷藏冰箱内过夜。第二天:将湿盒从冰箱内取出,PBS洗3次,每次2 min;滴加二抗,室温放置20 min,PBS洗3次,每次2 min;滴加SABC,室温放置20 min,PBS洗4次,每次5 min;DAB室温显色,蒸馏水洗涤中止反应,自来水冲洗30 min;⑤苏木素轻度复染,40~45 s,自来水流水冲洗30 min中止反应;将切片放入70%酒精1次10 min;80%酒精1次10 min;将切片放入90%酒精2次,每次10 min;将切片放入100%酒精2次,每次10 min;封片:中性树胶封片,要求胶少,无气泡。
2.7 结果判定标准免疫组化采用半定量法检测蛋白表达水平,是根据阳性细胞的比例和染色强度进行评分。阳性细胞比例:随机选择5个高倍视野,计算其中的阳性细胞比例,然后评分,<5%为0分,5%~25%为1分,25%-50%为2分;50%~75%为3分;>75%为4分。染色强度:无显色为0分,浅黄色或黄色为1分,棕黄色为2分,棕褐色为3分。蛋白表达水平=阳性细胞比例×染色强度。光镜下p-ERK和p-p38蛋白阳性细胞均表现为细胞浆或细胞膜呈棕黄色,而细胞核不着色。
2.8 统计方法用SPSS 19.0统计软件包进行数据处理,瘤体生长曲线采用重复测量方差分析,实验数据以均数±标准差(x±s)表示,不同组间比较采用One-way ANOVA分析,取P < 0.05作为显著性差异水平。
3 结果 3.1 裸鼠移植瘤的生长情况雌性裸鼠接种Siha细胞后,2 d种植区皮肤呈白色改变,3~4 d白色皮肤改变消失,5~6 d种植区皮下可触及2~3 mm瘤样结节,质地韧,7~8 d种植区皮下可触及直径5 mm瘤样结节,质地稍硬。本实验35只裸鼠成瘤率为100%。按裸鼠肿瘤体积大小随机分5组,每组7只,治疗前各组裸鼠平均体重无明显统计学差异(P>0.05)。

|
| 图 1 成瘤裸鼠 |
顺铂组裸鼠在用药后一周均出现活动量减少,厌食水,消瘦,皮肤干涩,其中2只裸鼠分别在用药第17、18天死亡,死亡裸鼠解剖其肝、肺、肾脏后未见明显异常,考虑为死亡为化疗后毒副作用所致。其余各组一般状况良好,未见药物不良反应。经过4周治疗后,各组裸鼠平均体重:清热利湿外治法高剂量组(18.83±0.76)g,清热利湿外治法中剂量组(18.45±0.65)g,清热利湿外治法低剂量组(18.72±0.82)g,顺铂组(13.51±0.31)g,对照组(19.26±0.82)g,顺铂组与其余各组相比,裸鼠体质量明显下降(P<0.05),清热利湿外治法3个剂量组与空白对照组体质量无明显变化(P>0.05),见表 1。
接种宫颈癌Siha细胞后各组肿瘤体积均逐渐增大,对照组肿瘤体积增长较快,各治疗组移植瘤体积均小于对照组,其中清热利湿外治法高、中剂量组及顺铂组与对照组相比差异具有统计学意义(P<0.05)。清热利湿外治法低剂量组肿瘤体积与对照组比较差异无统计学意义(P>0.05),见表 1。
3.4 各治疗组裸鼠瘤重及肿瘤生长抑制率的比较顺铂组肿瘤生长抑制率为75.82 3%,清热利湿外治法低、中、高剂量组抑制裸鼠Siha皮下移植瘤的抑制率分别为14.94%、31.24%、36.23%,见表 1。在治疗终点,顺铂组及紫柏凝胶高、中剂量组瘤重与对照组比较差异有统计学意义(P<0.05),而清热利湿外治法低剂量组瘤重与对照组比较无统计学意义(P>0. 05),见表 1。
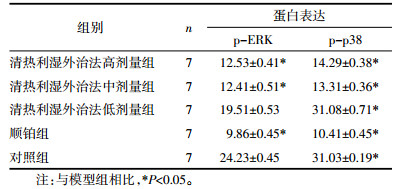
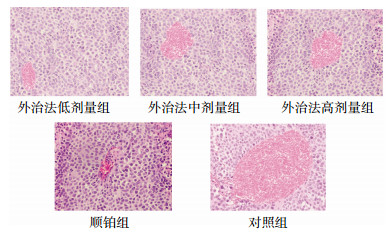
3.5 裸鼠移植瘤组织的病理学观察肉眼观察各组裸鼠移植瘤组织呈结节状,肿瘤组织血供明显、丰富,组织切面呈鱼肉样,可见局灶性坏死,以顺铂组及外用中药方高剂量治疗组明显。镜下见各组肿瘤细胞呈圆形或卵圆形,肿瘤细胞核大且清晰,可见病理性核分裂,肿瘤细胞呈漩涡、簇团状生长,瘤团间可见坏死病灶形成,呈均质红染色样,细胞变大,细胞核染色加深,见核固缩、溶解、碎裂。各治疗组的肿瘤组织坏死区域均有增大,其中顺铂组坏死区域增大较为明显。外用中药方用药组随着治疗剂量的增高,肿瘤组织坏死区域呈逐渐增大趋势。
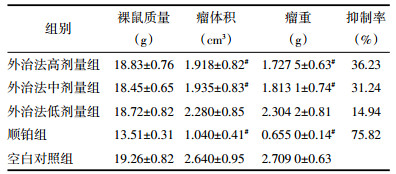
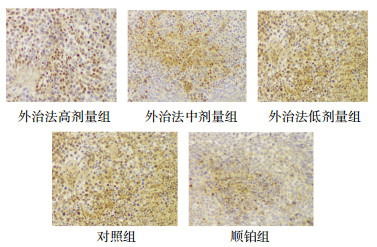
3.6 清热利湿外治法对p-ERK蛋白表达的影响从表 2可见,各用药治疗组与空白对照组相比较,p-ERK蛋白表达水平均有不同程度下降,其中外用中药方高剂量组、中剂量组及顺铂组与空白对照组相比较具有统计学差异(P<0.05)。提示外用中药方有下调p-ERK蛋白表达的作用。
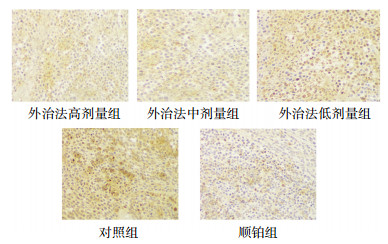
从表 2可见,各用药治疗组与空白对照组相比较,p-p38蛋白表达水平均有不同程度下降,其中外用中药方高剂量组、中剂量组及顺铂组与空白对照组相比较具有统计学差异(P<0.05)。提示外用中药方有下调p-p38蛋白表达的作用。

|
| 图 2 各组裸鼠大体情况 |
|
| 图 3 各组裸鼠移植瘤组织病理学观察(×200) |
|
| 图 4 各组裸鼠移植瘤组织p-ERK蛋白表达情况(×200) |
|
| 图 5 各组裸鼠移植瘤组织p-p38蛋白表达情况(×200) |
清热利湿外治法全方由紫草、金银花、苦参、黄柏、百部、莪术、白芨等药物组成,以上中药采用水提、醇提法提取后,加用卡波姆等基质制作而成,全方具有清热祛湿、解毒活血、敛疮生肌、杀虫止痒之功效。该方由东直门医院名老中医郭志强教授创立,该方经过前期部分临床观察,用于治疗宫颈高危型HPV感染,疗效甚佳。前期清热利湿体外实验研究结果亦证实此法能抑制宫颈癌Siha细胞的增殖和诱导其凋亡[10]。
本实验通过对人宫颈Siha细胞癌的动物研究,发现清热利湿外治法降低了人宫颈Siha细胞肿瘤的生长。我们通过建立人宫颈癌Siha细胞裸小鼠移植瘤模型,研究高、中、低剂量的清热利湿外治法治疗肿瘤效果,实验中采用模型组作为阴性对照,以细胞毒性药物顺铂作为阳性对照比较,结果显示清热利湿外治法对宫颈癌荷瘤裸鼠移植瘤生长有抑制作用。高、中、低浓度组的清热利湿外治法的肿瘤抑制率分别为36.23%、31.24%、14.94%,抑瘤效果呈剂量依赖性,随之外治法治疗剂量的增加,抑瘤效果增强。治疗期间荷瘤裸鼠无进食水量减少、消瘦、行动迟缓等副反应表现,显示外治方药物安全性高并无毒副作用。HE染色病理检查发现,随着外治方治疗剂量增加,瘤团间的坏死灶比例增大。本研究结果显示,外治法对宫颈癌裸鼠移植瘤的生长具有抑制作用。
ERK及P38是丝裂原活化蛋白激酶(MAPK)家族成员,参与并调节了细胞的生长、发育、分化、分裂及死亡等多种生理过程,并且在细胞的恶性转化中起着重要的作用。目前,ERK及P38是肿瘤发展和防治研究的重要热点。实验结果表明,清热利湿外治法在一定剂量范围内可以下调p-ERK及p- P38蛋白表达水平,说明清热利湿外治法可以通过下调ERK/P38 MAPK信号通路引起细胞周期阻滞进而阻滞宫颈癌细胞增殖,且清热利湿外治法对ERK/P38 MAPK信号通路的调节点应该在上游,具体调节点还需进一步实验证实。
| [1] |
程海荣, 陈杰. 年轻早期宫颈癌患者的诊治进展[J]. 现代肿瘤医学, 2016, 4: 678-680. DOI:10.3969/j.issn.1672-4992.2016.04.050 |
| [2] |
Mariani L, Preti M, Cristoforoni P, et al. Overview of thebenefits and potential issues of the nonavalent HPV vac-cine[J]. Int J Gynecol Obstet, 2017, 136(3): 1-8. |
| [3] |
Mariani L, Preti M, Cristoforoni P, et al. Overview of thebenefits and potential issues of the nonavalent HPV vac-cine[J]. Int J Gynecol Obstet, 2017, 136(3): 1-8. |
| [4] |
Joum EA, Giuliano AR, Iversen OE, et al. A 9-valentHPV vaccine against infection and intraepithelial neo-plasia in women[J]. N Engl J Med, 2015, 372(8): 711-723. DOI:10.1056/NEJMoa1405044 |
| [5] |
温利娟, 张云, 薛晓鸥. 中医治疗宫颈高危型人乳头瘤病毒感染临床研究进展[J]. 天津中医药大学学报, 2018, 37(5): 437-440. |
| [6] |
温利娟, 李娅, 薛晓鸥. 紫柏凝胶抑制宫颈癌Siha细胞增殖和诱导凋亡的实验研究[J]. 长春中医药大学学报, 2017, 33(6): 883-886. |
| [7] |
徐垲, 李健, 马秀丽, 等. 紫柏凝胶对宫颈癌SiHa细胞的影响[J]. 中国中医药信息杂志, 2015, 7: 60-62. |
| [8] |
徐垲, 马秀丽, 秦蕾. 紫柏凝胶外治方治疗宫颈高危型人乳头瘤病毒感染的临床观察[J]. 北京中医药大学学报, 2015, 8: 566-568+572. DOI:10.3969/j.issn.1006-2157.2015.08.013 |
| [9] |
马秀丽. "紫柏凝胶"治疗宫颈HR-HPV感染的临床研究及对宫颈组织HLA-I及CD8的影响[D].北京: 北京中医药大学, 2012.
|
| [10] |
开丽曼·阿不都巴热, 热伊拉·麦买提伊敏, 杨杰. 顺铂周疗联合放化疗在中晚期宫颈癌患者中的应用研究[J]. 检验医学与临床, 2016(20): 2955-2956. DOI:10.3969/j.issn.1672-9455.2016.20.044 |
 2019, Vol. 38
2019, Vol. 38