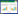文章信息
- 朱美娟, 李灵云, 杨君君, 杨静, 柴欣, 王跃飞
- ZHU Meijuan, LI Lingyun, YANG Junjun, YANG Jing, CHAI Xin, WANG Yuefei
- 基于差示浓度法的远志及其炮制品中三种成分的分析
- Analysis of three components in Radix Polygalae and its processed products by the method of differential concentration
- 天津中医药大学学报, 2019, 38(6): 598-602
- Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(6): 598-602
- http://dx.doi.org/10.11656/j.issn.1673-9043.2019.06.20
-
文章历史
收稿日期: 2019-09-09
 酮Ⅲ(PXⅢ)、3,6'-二芥子酰基蔗糖(DISS)、甘草酸(GA)的含量,以GA为标志物区分制远志与生远志、蜜远志。[方法] 采用超高效液相色谱法(UPLC),以甲醇-0.1%甲酸水为流动相,梯度洗脱,流速0.3 mL/min;柱温60℃;检测波长320、237 nm;进样量2 μL;测定高浓度供试品溶液中低含量成分(GA),测定低浓度供试品溶液中高含量成分(PXⅢ、DISS)。[结果] 差示浓度法能够分析远志及其炮制品中含量悬殊的PXⅢ、DISS和GA的含量。[结论] 该方法灵敏度高、准确性好,以GA为标志物能够区分制远志与生远志、蜜远志。
酮Ⅲ(PXⅢ)、3,6'-二芥子酰基蔗糖(DISS)、甘草酸(GA)的含量,以GA为标志物区分制远志与生远志、蜜远志。[方法] 采用超高效液相色谱法(UPLC),以甲醇-0.1%甲酸水为流动相,梯度洗脱,流速0.3 mL/min;柱温60℃;检测波长320、237 nm;进样量2 μL;测定高浓度供试品溶液中低含量成分(GA),测定低浓度供试品溶液中高含量成分(PXⅢ、DISS)。[结果] 差示浓度法能够分析远志及其炮制品中含量悬殊的PXⅢ、DISS和GA的含量。[结论] 该方法灵敏度高、准确性好,以GA为标志物能够区分制远志与生远志、蜜远志。 酮Ⅲ 3, 6'-二芥子酰基蔗糖 甘草酸
酮Ⅲ 3, 6'-二芥子酰基蔗糖 甘草酸 远志(Polygalae Radix)为远志科植物远志Polygala tenuifolia Willd.或卵叶远志Polygala sibirica L.的干燥根。中国植物志记载远志多产东北、华北、西北和华中以及四川,现主产于山西、陕西[1]。始载于《神农本草经》,是临床常用中药,性温, 味辛、苦, 归心、肾、脾经,具有安神益智[2-3]、祛痰[1]、消肿[4]等功效。文献报道远志生用有"戟人咽喉"的副作用,古籍有"若不去心,服之令人闷"的记载[5-6],口服易引起恶心、呕吐、眩晕等,因此远志多以炮制品入药,远志炮制后可减缓其毒副作用,增强安神益智之功效[7],临床常用制远志(甘草制)、蜜(炙)远志[8-10]。
远志及其炮制品中,蜜远志较生远志色泽深,表皮有光泽,略沾手,生、蜜远志性状差异较大易于区分。但制远志与生远志、蜜远志性状差异较小,外形上不易判别,易于混淆,所以构建制远志与生远志的鉴别方法对于临床用药的安全性和有效性意义重大[11-15]。远志主要化学成分为

中药中化学成分复杂,多个成分协同发挥疾病治疗作用,单一成分无法有效、准确的全面评价中药质量。但是,中药化学成分含量悬殊给中药多成分的质量评价带来困难,因此一般对中药中的微量、痕量成分进行富集以满足定量分析的要求。文献报道常采用柱切换程序进样技术解决含量悬殊成分的检测问题,通过控制进样量,在线富集含量较低的成分,选择性地将目标分析物通过富集后定量引入分析系统中, 尽可能去除中药中其他共存化合物的干扰,达到检测痕量、微量成分的目的[24]。但前处理净化富集操作复杂,柱切换技术对设备、流动相等提出更高要求,不利于推广应用。因此,需进一步开发更加简单、高效的含量悬殊成分同时测定方法,为中药多成分,特别是含量悬殊成分的测定提供方法支持。
本研究以PXⅢ、DISS、甘草酸(GA)为指标成分,针对制远志中的PXⅢ、DISS与甘草中的GA含量差别较大的特点,为提高检测准确性,构建了差示浓度分析法,制备高浓度供试品溶液以检测低含量成分(GA),高浓度样品稀释后获得低浓度供试品溶液以检测高含量成分(PXⅢ、DISS),通过“一样多测”有效解决了含量差别较大成分的同时检测问题。
1 仪器及试药 1.1 仪器超高效液相色谱仪:Waters ACQUITYTM UPLC系统(美国沃特世公司);XS 205型十万分之一电子天平(瑞士Mettler-Toledo公司),AL 204型电子天平(瑞士Mettler-Toledo公司);DHG-9145A型电热恒温鼓风干燥箱(上海一恒科技有限公司);SCIENTZ SB25-12DTN型超声波清洗器(宁波新芝生物有限公司,功率:500 W,频率:40 kHz);TGL-16C型高速台式离心机(上海安亭科学仪器厂);Milli-Q型超纯水系统(美国Millipore公司)。
1.2 药品与试剂甘草酸铵(110731-201619,购自中国食品药品检定研究院,纯度为98%),DISS(P04A7F18932,购自上海源叶生物科技有限公司,纯度为98%),PXⅢ(R02A8F41025,购自上海源叶生物科技有限公司,纯度92.0%);甲醇、甲酸均为色谱纯,水为实验室自制超纯水;远志生品(S1~S5)、制远志(Z1~Z10)、蜜远志(M1~M3)均购自亳州市药材市场。含量测定方法学研究用制远志(Z0)是参照2015年版《中华人民共和国药典》制远志炮制方法炮制,所用远志(S0)产地山西,经鉴定为远志科植物远志Polygala tenuifolia Willd.的干燥根,炮制所用的甘草、生远志均购自河北春开制药股份有限公司。
制远志的炮制:参照2015版《中华人民共和国药典》规定的制远志炮制方法。取生远志,按照远志:甘草(100:6)加入适量甘草水煎液,文火煮至吸尽汤汁,取出平铺,置烘箱干燥,放凉,即得。制远志中水分应 < 12%[17]。
2 方法与结果 2.1 色谱条件色谱柱:ACQUITY UPLC® BEH C18(2.1 mm×100 mm,1.7 μm);进样量2 μL;检测波长320、237 nm;柱温60 ℃;以甲醇(A)-0.1%甲酸水(B)为流动相梯度洗脱(0~6 min,5%~33%A;6~7 min,33%~33%A;7~7.5 min,33%~41%A;7.5~10 min,41%~46.7%A;10~11 min,46.7%~55%A;11~16 min,55%~70%A;16~20 min,70%~95%A),流速0.3 mL/min。
2.2 对照品溶液的制备取远志

取混合对照品溶液,用50%甲醇逐级稀释成2、4、8、16、32、64倍的一系列混合对照品溶液。
2.3 供试品溶液的制备取远志粉末0.5 g,精密称定,置25 mL容量瓶中,加75%甲醇适量,密塞,超声处理30 min,放冷,75%甲醇定容至刻度,摇匀,14000 rpm离心10 min,取上清液,备用,供检测GA用(高浓度)。
取上述供试品溶液1 mL于5 mL容量瓶中,加30%甲醇水溶液定容,摇匀,备用,供测定PXⅢ、DISS用(低浓度)。
2.4 方法学验证 2.4.1 线性关系考察按“2.1”项下色谱条件测定“2.2”项下系列混合对照品溶液(PXⅢ浓度为73.35、36.68、18.34、9.17、4.58、2.29、1.15 μg/mL;DISS浓度为258.02、129.01、64.51、32.25、16.13、8.06、4.03 μg/mL;GA浓度为157.07、78.53、39.27、19.63、9.82、4.91、2.45 μg/mL),平行进样2次,以对照品浓度x(μg/mL)为横坐标,以峰面积y为纵坐标,绘制标准曲线,以信噪比S/N=3为检测限(LOD)、S/N=10为定量限(LOQ),结果如表 1。远志中PXⅢ、DISS、GA在相应浓度范围内线性关系良好,其相关系数r均大于0.999。
按“2.3”项下方法制备制远志供试品溶液,以“2.1”项下色谱条件测定,重复进样6次,连续测定三天,计算其RSD值,考察该方法日内和日间精密度。结果表明,该方法的日内精密度RSD值均小于1.9%,日间精密度RSD均小于1.4%,该方法精密度良好。
2.4.3 重复性试验按“2.3”项下方法制备制远志供试品溶液,平行制备6份,采用“2.1”项下色谱条件测定,制远志中PXⅢ、DISS、GA含量分别为2.183 7、7.737 8、0.600 8 mg/g(RSD值均小于2.1%)。结果表明,该方法的重现性良好。
2.4.4 稳定性试验按“2.3”项下方法制备制远志供试品溶液,采用“2.1”项下色谱条件分别于0、2、4、6、8、10、12 h进样测定,指标成分RSD值均小于0.66%。结果表明,供试品溶液中PXⅢ、DISS、GA在12 h内稳定。
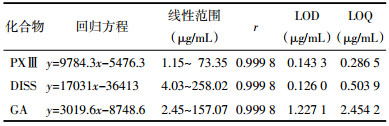
2.4.5 加样回收率试验取制远志粉末0.25 g,精密称定,准确加入与样品中各成分质量相当的指标成分的对照品溶液,按“2.3”项下方法制备制远志供试品溶液,平行6份,以“2.1”项下方法平行测定2次,PXⅢ、DISS、GA的加样回收率均值分别为103.2%、102.7%、97.5%,RSD均小于2.2%,结果如表 2所示,表明各化合物加样回收率良好,方法准确可行。
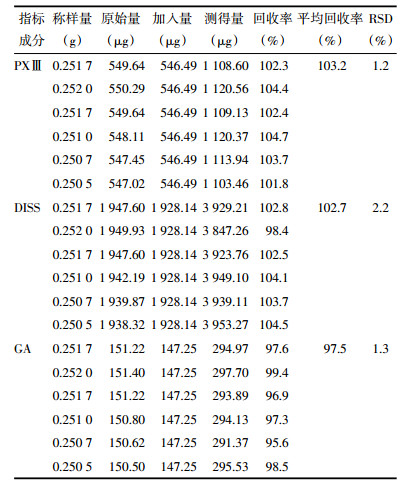
取不同批次的远志(S1~S5)、制远志(Z1~Z10)、蜜远志(M1~M3)饮片,粉碎,按“2.3”项下方法制备制远志供试品溶液,以“2.1”项下色谱条件检测,生远志、制远志、蜜远志的高低浓度供试品溶液色谱图如图 1所示。
|
| 图 1 制远志(A1低浓度,A2高浓度)、生远志(B1低浓度,B2高浓度)、蜜远志(C1低浓度,C2高浓度)、甘草汁(D)、混合对照品(E)色谱图 |
采用差示浓度法测定了不同批次的远志、制远志、蜜远志中PXⅢ、DISS、GA的含量,结果如图 2所示。生远志中PXⅢ和DISS含量分别为0.8131~1.7168、4.7333~6.4498 mg/g;生远志中未检测到GA。制远志中PXⅢ、DISS、GA含量分别为0.8122~1.9539、2.1834~6.5732、0.1210~0.4313 mg/g。蜜远志中PXⅢ、DISS含量分别为0.8104~0.8535、2.6710~6.5144 mg/g,未检测到GA。因此,GA可以作为标志物区分制远志与生远志、蜜远志。
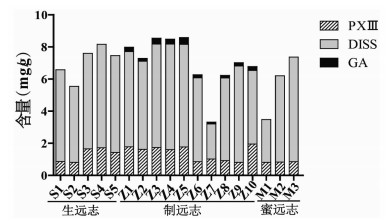
|
| 图 2 不同批次远志及其炮制品中PXⅢ、DISS、GA的含量 |
制远志供试品溶液制备方法的优化:以PXⅢ、DISS、GA含量为指标,系统考察了提取溶剂(50%甲醇水、75%甲醇水、甲醇)、提取时间(20 min、30 min、40 min)和料液比(1:25、1:50、1:100)对指标成分提取效率的影响,结果如图 3所示,超声提取30 min、40 min结果无明显差别,优于20 min的提取结果,为节约时间成本,选择超声处理30 min;料液比对制远志指标成分提取效率影响较小;75%甲醇水作为提取溶剂优于50%甲醇水和100%甲醇,提取效率略高。最终确定供试品溶液制备方法(如“2.3”项下供试品溶液的制备方法所示)。
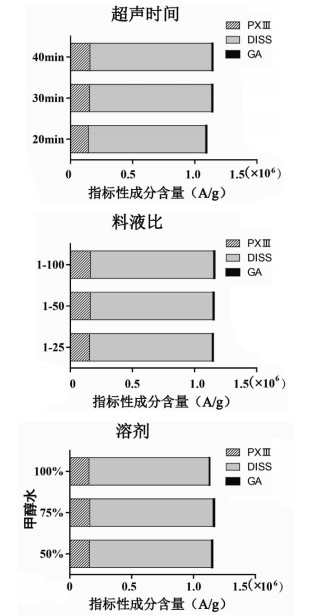
|
| 图 3 制远志供试品制备方法的优化结果 |
根据“2.5”项下各批次指标成分含量测定的结果,10批制远志中,制远志DISS含量约为GA含量的14.81~32.30倍,指标成分含量悬殊,难以同时测定,本研究构建的差示浓度法通过供试品溶液的梯度稀释,从而实现含量悬殊成分的同时检测,既可节省对照品,又能减少测定误差,验证了建立的“差示浓度法”的必要性、实用性。该方法具有操作简单、测定结果准确,可以根据样品含量的分布情况自主决定稀释倍数和稀释次数的优点,可以有效解决指标成分DISS、GA含量悬殊成分同时检测的问题。同时,GA作为标志物实现了制远志与生远志、蜜远志的区分。
| [1] |
苏晶, 陶慕珂, 陈晓虎, 等. 远志质量问题及中药材产地加工探讨[J]. 中国药事, 2018, 32(11): 1467-1472. |
| [2] |
罗虹, 王泽鹏, 郭亚菲, 等. 基于网络药理学探讨"远志-酸枣仁"药对安神作用机制[J]. 山西中医学院学报, 2019, 20(4): 254-258. |
| [3] |
Shin JW, Park H, Cho Y, et al. Reduced consolidation, reinstatement, and renewal of conditioned fear memory by repetitive treatment of Radix Polygalae in mice[J]. Front Psychiatry, 2017, 8: 97. DOI:10.3389/fpsyt.2017.00097 |
| [4] |
徐雪婷, 陈勤. 远志神经系统药理作用研究进展[J]. 现代中药研究与实践, 2015, 29(6): 77-82. |
| [5] |
蒲雅洁, 王丹丹, 张福生, 等. 远志的本草考证[J]. 中草药, 2017, 48(1): 211-218. |
| [6] |
刘艳芳, 彭东艳, 杨晓娟, 等. 去心与不去心远志药材的化学成分和药效学比较研究[J]. 中国药学杂志, 2012, 47(24): 1975-1979. |
| [7] |
郭常润. 远志不同炮制品对东莨菪碱模型小鼠模型学习记忆的影响[J]. 山东化工, 2015, 44(4): 10-12. DOI:10.3969/j.issn.1008-021X.2015.04.004 |
| [8] |
王瑞, 吴桐, 刘悦, 等. 远志和蜜远志对小鼠胃肠的急性毒性作用[J]. 中国中医药现代远程教育, 2018, 16(8): 88-90. DOI:10.3969/j.issn.1672-2779.2018.08.037 |
| [9] |
刁家葳, 王幼鹏, 张学兰, 等. 远志不同炮制品中3种寡糖酯类成分含量比较[J]. 辽宁中医杂志, 2018, 45(2): 346-349. |
| [10] |
郭琪, 程利娟, 雷虹, 等. 高效液相色谱法测定甘草远志合剂中甘草酸铵的含量[J]. 解放军医药杂志, 2013, 25(11): 76-80. DOI:10.3969/j.issn.2095-140X.2013.11.022 |
| [11] |
蒋冬霜. 不同炮制方法对远志药效的影响[J]. 中国处方药, 2016, 14(8): 26-27. DOI:10.3969/j.issn.1671-945X.2016.08.017 |
| [12] |
Wu D, He J, Jiang Y, et al. Quality analysis of Polygala tenuifolia root by ultrahigh performance liquid chromatography-tandem mass spectrometry and gas chromatography-mass spectrometry[J]. Journal of Food & Drug Analysis, 2015, 23(1): 144-151. |
| [13] |
祝之友. 远志鉴别要点[J]. 中国中医药现代远程教育, 2018, 16(20): 121. |
| [14] |
孟艳, 吴鹏, 张学兰, 等. 高效液相色谱-飞行时间质谱法快速鉴定远志生、制饮片的化学成分[J]. 中国实验方剂学杂志, 2015, 21(20): 17-20. |
| [15] |
张智华, 文莉, 陈海洋, 等. 远志常用配伍的实验研究进展[J]. 中国实验方剂学杂志, 2016, 22(12): 224-228. |
| [16] |
Feng GF, Liu S, Pi ZF, et al. Studies on the chemical and intestinal metabolic profiles of Polygalae Radix by using UHPLC-IT-MSn and UHPLC-Q-TOF-MS method coupled with intestinal bacteria incubation model in vitro[J]. Journal of Pharmaceutical and Biomedical Analysis, 2018, 148: 298-306. DOI:10.1016/j.jpba.2017.10.017 |
| [17] |
国家药典委员会.中华人民共和国药典[S].一部.北京: 中国医药科技出版社, 2015: 156-157.
|
| [18] |
陈静静, 王相, 连云岚, 等. 远志中远志  酮Ⅲ含量测定方法的改进[J]. 中国药房, 2016, 27(3): 397-399. 酮Ⅲ含量测定方法的改进[J]. 中国药房, 2016, 27(3): 397-399. |
| [19] |
徐保鑫, 刁家葳, 张学兰, 等. 远志炮制过程中6种寡糖酯类成分转化机制[J]. 中成药, 2018, 40(8): 1790-1794. DOI:10.3969/j.issn.1001-1528.2018.08.024 |
| [20] |
Xu R, Mao F, Zhao Y, et al. UPLC Quantitative Analysis of Multi-Components by Single Marker and Quality Evaluation of Polygala tenuifolia Wild. Extracts. Molecules, 2017, 22(12): 2276.
|
| [21] |
白钢钢, 袁斐, 叶慧, 等. 不同蜜炙方法对远志化学成分的影响[J]. 中药材, 2018(9): 1845-1848. |
| [22] |
梁晓, 张学兰, 李慧芬, 等. 甘草汁蒸制远志对远志皂苷B和细叶远志皂苷含有量的影响[J]. 中成药, 2015, 37(4): 824-827. DOI:10.3969/j.issn.1001-1528.2015.04.029 |
| [23] |
王丹丹, 闫艳, 张福生, 等. 远志药材UPLC指纹图谱及多指标性成分测定方法的建立[J]. 中草药, 2018, 49(5): 1150-1159. |
| [24] |
高晓筝. 中药制剂中含量悬殊成分的分析方法探讨[J]. 中国卫生标准管理, 2016, 7(11): 155-156. |
 2019, Vol. 38
2019, Vol. 38