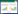文章信息
- 王新慧, 李敏, 柴欣, 王跃飞, 杨静
- WANG Xinhui, LI Min, CHAI Xin, WANG Yuefei, YANG Jing
- 小茴香饮片的粉末均匀化研究
- The study of powder homogenization of fennel
- 天津中医药大学学报, 2020, 39(1): 82-86
- Journal of Tianjin University of Traditional Chinese Medicine, 2020, 39(1): 82-86
- http://dx.doi.org/10.11656/j.issn.1673-9043.2020.01.18
-
文章历史
收稿日期: 2019-08-20
小茴香为伞形科植物茴香(Foeniculum vulgare Mill.)的干燥成熟果实,始载于《唐本草》,味辛,温,具有散寒、理气和胃的功效[1]。盐小茴香具有暖肾,散寒的功效,用于寒疝腹痛、睾丸偏坠、。现代药理研究证明,小茴香具有显著的抑菌、调节胃肠机能、利尿等作用,同时还具有利胆、保肝、促渗、抗癌、抗氧化抗突变及性激素样等作用[2-5]。
中药“标准饮片”作为中药提取物和中成药生产中的原料,可以全面的表征中药饮片特征属性,进而完整控制饮片中药效物质,更专属、更准确地分别评价生、制饮片质量,保障中药饮片的安全性、有效性、质量可控[6-7]。粉碎工艺的优化是标准饮片均匀化过程的重要环节,是后续一系列对于标准饮片内涵属性研究的基础。本实验以出粉率和紫丁香苷(SG)、槲皮素-3-O-葡萄糖醛酸苷(QG)的含量为指标,在此基础上设计L9(34)正交实验,采用“蛛网模式”[8-9]优选生小茴香和盐小茴香标准饮片均匀化工艺,为制定生小茴香和盐小茴香标准饮片均匀化技术规范提供参考依据。
1 仪器与试药 1.1 仪器ACQUITYTM UPLC system超高效液相色谱仪(美国沃特世公司);XS 205型十万分之一电子天平(瑞士Mettler-Toledo公司),AL 204型电子天平(瑞士Mettler-Toledo公司);DL 180E型智能超声波清洗器(上海之信仪器有限公司;功率:180W,频率:50 kHz);TGL-16C型高速台式离心机(上海安亭科学仪器厂);Milli-Q型超纯水系统(美国Millipore公司);HYC-940医用冷藏箱(青岛海尔特种电器有限公司);药筛:1~9号(上虞市冲压筛具厂);FW80型粉碎机(天津市泰斯特仪器有限公司)。微量进样器(平头10 μL,上海高鸽工贸有限公司),硅胶G板(200 mm×100 mm,青岛海洋化工分厂)。
1.2 试剂生小茴香购自河北春开制药股份有限公司,经天津中医药大学李天祥教授鉴定为伞形科植物茴香(Foeniculum Vulgaer Mill.)的干燥成熟果实。盐小茴香:严格按照2015版《中华人民共和国药典》盐炙法(通则0213)炮制。紫丁香苷(批号111574-201605)购自中国食品药品检定研究院,槲皮素-3-O-葡萄糖醛酸苷(批号R24S7F21842)购自上海源叶生物科技有限公司,HPLC分析纯度均≥95%。茴香醛(批号110838-201106)购自中国食品药品检定研究院。甲醇、甲酸均为色谱纯,水为超纯水。本文中小茴香是生小茴香和盐小茴香的统称;紫丁香苷简称为SG;槲皮素-3-O-葡萄糖醛酸苷简称为QG。
2 方法 2.1 色谱条件超高效液相色谱条件色谱柱ACQUITY UPLCⓇ BEH C18(2.1 mm×50 mm,1.7 μm);流动相:甲醇(B)- 0.1%甲酸水(A),梯度洗脱(0~7 min,95% → 63.5% A;7~12 min,63.5% → 15% A);柱温40 ℃;流速0.3 mL/min;检测波长:254 nm;进样量:2 μL[10]。
薄层色谱条件按照2015版《中华人民共和国药典》中薄层色谱法(通则0502)实验,吸取样品和对照品溶液各1~5 μL,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(17:2.5)为展开剂,展至8 cm,取出,晾干,喷以二硝基苯肼试液,日光下检视。
2.2 对照品溶液制备分别取SG、QG对照品适量,精密称定,制成质量浓度为1 mg/mL的对照品储备液,备用。分别取上述SG、QG对照品储备液500 μL、700 μL,置于5 mL容量瓶中,加50%甲醇定容至刻度,摇匀,制成质量浓度分别为99.30 mg/mL、123.8 mg/mL的混合对照品溶液,供定量分析用。
取茴香醛对照品,加乙醇制成每1 mL含1 μL的溶液,作为对照溶液,供薄层鉴别用。
2.3 供试品溶液的制备取小茴香粉末0.5 g,精密称定,置于25 mL的容量瓶中,加适量50%甲醇,密塞,超声处理(功率144 W,频率50 kHz)20 min,放冷,50%甲醇定容至刻度,摇匀,14 000 r/min离心10 min,取上清液,过滤,取续滤液1 mL,加1 mL蒸馏水,混匀,供定量分析用。
取小茴香粉末2 g,加乙醚20 mL,超声处理(功率144 W,频率50 kHz)10 min,滤过,滤液挥干,残渣加三氯甲烷1 mL使溶解,供薄层鉴别用。
2.4 不同目数的小茴香饮片粉末分布及对指标成分的影响研究取生小茴香和盐小茴香各100 g,粉碎机单次粉碎10 s,采用《中华人民共和国药典》规定的标准药筛制备不同粒度的粉末,称取不同药筛上未通过该药筛的样品粉末重量,分别计算其比例。按“2.3”项下方法处理样品A ~ H(生小茴香饮片粉末)和样品A' ~ H'(盐小茴香饮片粉末)制备含量测定和薄层鉴别样品,按“2.1”色谱条件测定供试品溶液中SG、QG的含量,薄层色谱条件鉴别不同粒度小茴香饮片粉末。
2.5 基于“蛛网模式”的小茴香饮片粉碎工艺正交实验研究以粉碎时间、粉碎次数、投料量(以投料药材占粉碎室的体积计)为因素,以出粉率、化合物含量为指标进行正交实验,借鉴本课题组研究的“蛛网模式”[11]原理,优选最佳粉碎工艺。Ga、G'a分别代表生小茴香和盐小茴香中出粉率,SG和QG的总量为Za和Z'a,其中a为不同粉碎方式(9个正交实验组,a为1~9)的小茴香饮片粉末样品。
为了消除不同指标取值范围差异对统计结果的影响,需对不同变量指标进行归一化处理。生小茴香和盐小茴香样品中最大出粉率为Ga(max)和G'a(max);SG和QG的最高总含量为Za(max)和Z'a(max)。将所得指标的数值分别除以其最大值,得到出粉率的归一化结果分别为Qa和Q'a,SG、QG总量的归一化结果分别为Ha和H'a。计算公式1、2如下所示。
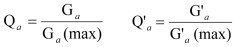
|
(1) |
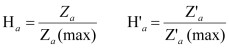
|
(2) |
通过计算Qa和Ha(Q'a和H'a)组成的阴影部分面积,优选生小茴香和盐小茴香饮片的最佳粉碎方式,其归一化面积分别为S和S',计算公式3、4如下所示。
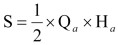
|
(3) |
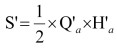
|
(4) |
取生小茴香和盐小茴香,以确定的小茴香最佳粉碎工艺制备小茴香标准饮片粉末,计算出粉率;按“2.3”项下方法制备小茴香饮片粉末供试品溶液,按“2.1”项下色谱条件测定供试品溶液中SG、QG的含量。
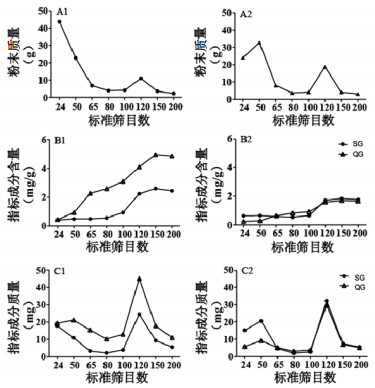
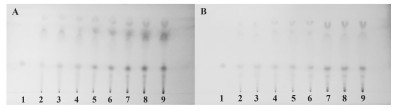
3 结果与讨论 3.1 不同目数的小茴香饮片粉末分布及对指标成分的影响研究由图 1所示,小茴香饮片粉末全部通过10目筛,生品中56.29%粉末通过24目筛,盐品粉末中75.99%通过24目筛;生品粉末中33.49%通过50目筛,盐品粉末中43.17%通过50目筛;生品盐品中均未有粉末通过200目筛。由结果可以看出经过高温炮制之后的小茴香饮片,质地更为疏松,更利于粉碎。SG和QG指标含量随标准筛目数增加,含量增加。薄层色谱结果显示生品盐品中茴香醛的含量随标准筛目数增加,斑点颜色加深。盐品中茴香醛斑点强度弱于生品中茴香醛强度,结果见图 2。
|
| 1生小茴香;2盐小茴香 图 1 不同目数小茴香饮片粉末质量(A)、指标成分含量(B)、指标成分质量(C)的折线图 |
|
| 1~9依次为茴香醛对照品、24目、50目、65目、80目、100目、120目、150目、200目标准筛上粉末的供试品溶液 图 2 不同生小茴香饮片粉末(A)、盐小茴香饮片粉末(B)薄层色谱图 |
结合小茴香饮片粉末目数分布的结果和2015版《中华人民共和国药典》小茴香项下的相关规定,采用中国药典规定的标准药筛三号筛制备小茴香标准饮片粉末,按“2.3”项下方法制备小茴香饮片粉末供试品溶液,按“2.1”项下色谱条件测定供试品溶液中指标成分的含量。以粉碎时间、粉碎次数、投料量(以投料药材占粉碎室的体积计)为因素,以出粉率、化合物含量为指标进行正交实验,优选最佳粉碎工艺,测定结果见表 1。
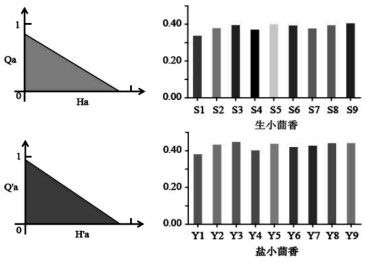
按“2.5”项下计算公式对小茴香粉末出粉率、化合物含量进行归一化处理,计算其归一化面积,结果见图 3。通过正交实验设计助手对实验数据进行分析,以归一化面积(S)为指标进行评价,考察因素对生小茴香饮片研究结果的归一化面积的影响为:粉碎次数 > 粉碎时间 > 投料量,最佳粉碎工艺为A3B3C3,即投料量为1/2粉碎室的体积,单次粉碎时间40 s,粉碎3次,过50目筛,即得。考察因素对盐小茴香饮片研究结果的归一化面积的影响为:粉碎次数 > 投料量 > 粉碎时间,最佳粉碎工艺为A3B2C3,即投料量为1/2粉碎室的体积,单次粉碎时间40 s,粉碎2次,过50目筛,即得。
|
| 图 3 基于“蛛网模式”对小茴香饮片粉碎工艺研究结果 |
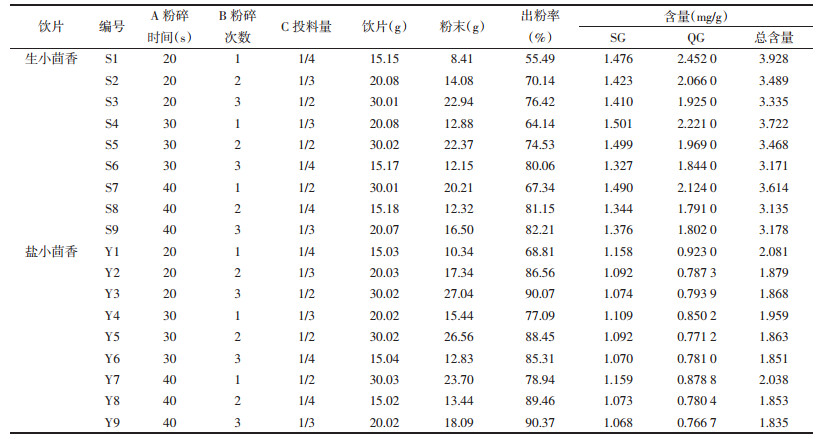
采用“2.6”项下方法,采用最佳粉碎工艺制备小茴香标准饮片粉末,计算出粉率及SG、QG的含量,结果见表 2。
综上可知,采用最佳粉碎工艺制备的生小茴香饮片的出粉率84.93%,RSD为1.44%(n=3);SG、QG的总含量为3.473 mg/g,RSD为1.01%(n=3),说明生小茴香最佳粉碎工艺稳定、可行。采用最佳粉碎工艺制备的盐小茴香饮片的出粉率92.01%,RSD为0.57%(n=3);SG、QG的总含量为1.740 mg/g,RSD为1.50%(n=3),说明盐小茴香最佳粉碎工艺稳定、可行。
4 结论实验利用“蛛网模式”的研究方法,通过出粉率、指标成分的总含量计算归一化面积(S),采用正交实验法以S为指标对小茴香进行粉末均匀化工艺研究。经粉碎工艺放大验证,该方法可行,为小茴香的标准饮片均匀化技术规范制定提供参考依据。
| [1] |
国家药典委员会.中华人民共和国药典[S].北京: 中国医药科技出版社, 2015: 47. National Commission of Chinese Pharmacopoeia. Pharmacopoeia of the People's Republic of China[J]. Beijing: Chinese Medical Science and Technology Press, 2015: 47. |
| [2] |
王建清, 杨艳, 金政伟, 等. 小茴香等7种植物蒸馏提取物的抑霉菌效果[J]. 天津科技大学学报, 2011(1): 10-13. WANG Y Q, YANG Y, JIN Z W, et al. Inhibition mould of distillation extracts from seven species of natural plants[J]. Journal of Tianjin University of Science & Technology, 2011(1): 10-13. DOI:10.3969/j.issn.1672-6510.2011.01.003 |
| [3] |
张泽高, 肖琳, 詹欣宇, 等. 维药小茴香抗肝纤维化作用及对TGF-β/smad信号转导通路的影响[J]. 中国肝脏病杂志(电子版), 2014(1): 32-37. ZHANG Z G, XIAO L, ZHAN X Y, et al. Effects of foeniculum vulgare mill of anti liver fifi brosis on TGF-β/smad signal pathways[J]. Chinese Journal of Liver Diseases (Electronic Version), 2014(1): 32-37. DOI:10.3969/j.issn.1674-7380.2014.01.008 |
| [4] |
孙亮, 杨欣欣, 包永睿, 等. 抗癌中药小茴香中无机元素的含量测定[J]. 中国药物评价, 2013, 30(3): 129-131. SUN L, YANG X X, BAO Y R, et al. Determination of inorganic elements in Foeniculi Fructus by ICP-MS[J]. Chinese Journal of Drug Evaluation, 2013, 30(3): 129-131. |
| [5] |
谢敏华, 陈丽. 小茴香抗菌与抗氧化作用研究进展[J]. 中国调味品, 2012, 37(10): 15-17. XIE M H, CHEN L. The research progress of antioxidant effect of Fennel[J]. China Condiment, 2012, 37(10): 15-17. |
| [6] |
肖永庆, 李丽, 刘颖. 构建中药饮片质量保障体系的关键问题[J]. 世界科学技术-中医药现代化, 2015, 17(1): 167-172. XIAO Y Q, LI L, LIU Y. Key problems of building Chinese herbal pieces quality guarantee system[J]. Modemization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2015, 17(1): 167-172. |
| [7] |
李丽, 刘颖, 肖永庆. 中药炮制与饮片领域科研回顾与展望[J]. 中华中医药杂志, 2015(9): 3053-3057. LI L, LIU Y, XIAO Y Q. Retrospect and prospect of scientific research in studying field of processing and pieces[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2015(9): 3053-3057. |
| [8] |
杨静, 江振作, 柴欣, 等. 中药注射液"Q-Markers"的辨析研究-丹红注射液研究实例[J]. 世界科学技术-中医药现代化, 2016, 18(12): 2056-2061. YANG J, JIANG Z Z, CHAI X, et al. Discriminant analysis of "Q-Markers" of traditional Chinese medical injections-taking Dan Hong injection as a model[J]. Modemization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2016, 18(12): 2056-2061. DOI:10.11842/wst.2016.12.005 |
| [9] |
江振作, 王跃飞. 基于"药材基原-物质基础-质量标志物-质控方法"层级递进的中药质量标准模式研究[J]. 中草药, 2016, 47(23): 4127-4133. JIANG Z Z, WANG Y F. A pattern of hierarchical progression for quality standard of Chinese materia medica based on "herbal origin-material basis-quality markers-quality control method"[J]. Chinese Traditional and Herbal Drugs, 2016, 47(23): 4127-4133. |
| [10] |
李敏, 窦志英, 柴欣, 等. 炮制对小茴香中黄酮成分的影响[J]. 天津中医药, 2019, 36(6): 612-614. LI M, DOU Z Y, CHAI X, et al. Effect of processing on flavonoids in Fennel[J]. Tianjin Journal of Traditional Chinese Medicine, 2019, 36(6): 612-614. |
| [11] |
YANG J J, YANG J, DU J, et al. General survey of Fructus Psoraleae from the different origins and chemical identification of the roasted from raw Fructus Psoraleae[J]. J Food Drug Anal, 2018, 2(26): 807-814. DOI:10.1016/j.jfda.2017.10.009 |
 2020, Vol. 39
2020, Vol. 39