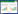文章信息
- 李宝辉, 李冬晖, 薛党党, 赵光
- LI Baohui, LI Donghui, XUE Dangdang, ZHAO Guang
- 中药益母草的化学指纹图谱及多组分定量分析方法的建立及应用研究
- The establishment and application of chemical fingerprint and multi-component quantitative analysis for Leonuri Herba
- 天津中医药大学学报, 2020, 39(3): 336-340
- Journal of Tianjin University of Traditional Chinese Medicine, 2020, 39(3): 336-340
- http://dx.doi.org/10.11656/j.issn.1673-9043.2020.03.19
-
文章历史
收稿日期: 2020-01-20
益母草(Leonuri Herba)是唇形科植物(Leonurus japonicus Houtt.)的新鲜或干燥地上部分[1], 主要药效成分为生物碱类、黄酮类、脂肪酸类、挥发油类化合物[2-3], 具有抗氧化、抗炎、抗血小板聚集等效用[4-5]。原料药的质量是药效发挥的重要保证。一些研究集中于定量分析益母草的已知成分来评价其质量[6-8], 事实上仍有部分重要化合物因未被确认而无法定量, 因此需要联用定量分析之外的其他技术来提升其质量控制的准确度和完整性。指纹图谱技术联合化学计量学可准确识别系统的微小差异, 被广泛用于复杂物质质量控制。已构建的益母草指纹图谱集中于制剂和配方[9-10], 原料药的指纹图谱仍属空白。本研究联合高效液相色谱(HPLC)指纹图谱技术和多组分定量分析研究不同产地益母草原料药。
1 实验部分 1.1 益母草采集和化学品准备研究共采集了本地区部分医院中药房和中药材零售店的110份益母草, 其中湖北2018年批次20份(#1~#20), 江西2018年批次25份(#21~#45), 河南2018年批次30份(#46-#75), 新疆2018年批次35份(#76-#110)。将样品打碎过40目筛后, 分装入塑料自封袋中, 20℃避光保存。
标准品:芦丁、芹菜素、槲皮素、山奈酚、盐酸益母草碱、盐酸水苏碱(色谱纯, 源叶生物科技有限公司, 上海); 其他化学品:甲醇(CH3OH)、乙醇(CH3CH2OH)、磷酸(H3PO4)、氢氧化钠(NaOH)(分析纯, 大茂化学试剂厂, 天津)。
1.2 HPLC试液制备及测量方法益母草提取物制备:逐份准确称取0.45 g益母草于50 mL锥形瓶中, 加入80%乙醇-水溶液25 mL, 用保鲜膜封口后置于BXP7200超声仪超声提取30 min (50℃, 40 kHz), 之后将提取物滤入25 mL容量瓶, 80%乙醇-水溶液定容。HPLC实验进样前, 将提取物过0.45 μm滤膜。
应用Agilent 1260 HPLC-DAD检测益母草提取物, 色谱柱为Agilent Zorbax Eclipse Plus-C18柱(4.6 mm×250 mm, 5 μm), 柱温20℃, 进样量20 μL, 流速1 mL/min, 流动相为甲醇(A)和0.1%磷酸-水溶液(B), 洗脱梯度:0~50 min, 95% B~20% B, 95% B平衡10 min, 检测波长270 nm。
应用Agilent 1260/6125 HPLC-MS鉴定益母草提取物的组成, 采用电喷雾离子源, 负离子检测模式, 毛细管电压3.0 kV, 锥孔电压30 V, 离子源温度110℃, 脱溶剂气温度350℃, 锥孔气流量50 L/h, 扫描范围50~850 m/z。
1.3 HPLC定量分析及方法学考察准确称取各标准品以制备梯度为800、400、80、40、10、0.1、0.01 μg/mL的标准品溶液, 其中芦丁、槲皮素、山奈酚的溶剂为甲醇, 芹菜素的溶剂为0.01 mol/L NaOH, 盐酸益母草碱的溶剂为超纯水。按"1.2"所述的HPLC方法检测, 5种标准品在梯度内线性良好(R>0.999), 见表 1。
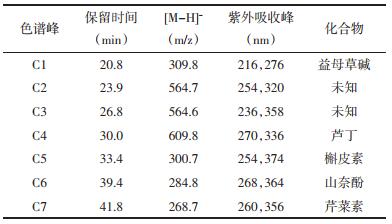
方法有效性验证:在HPLC批量检测前, 从4个产地药材中随机各取出1份(#2, #31, #66, #101)做重复性实验和中间精密度实验。重复性实验即同一份样品连续进样3次, 检测各组分峰面积的相对标准偏差(RSD); 中间精密度实验即同一份样品在当天3个时段(8:00-12:00, 14:00-18:00, 20:00-24:00)分别进样, 检测各组分峰面积的RSD。选取5个色谱峰(C1、C4、C5、C6、C7, 见图 1)做HPLC方法学考察。重复性实验的RSD为0.12%~0.44%, 中间精密度实验的RSD为0.21%~0.52%。
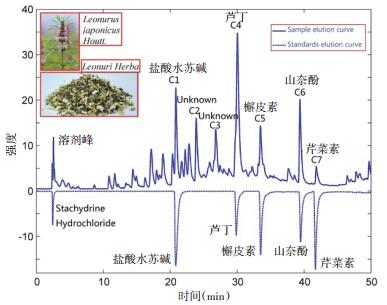
|
| 图 1 益母草提取物和标准品的HPLC流出曲线 |
应用化学计量学中经典的模式识别方法评价HPLC指纹图谱的效能, 包括无监督模式识别方法[主成分分析(PCA)]和有监督模式识别方法[线性判别分析(LDA), 最小二乘-支持向量机(LS-SVM), 径向基-神经网络(RBF-NN)][11-13]。本研究所有数据的统计学分析均在MATLAB 7.0平台完成。
2 结果 2.1 HPLC条件优化HPLC条件优化以益母草提取物的色谱峰(C1、C4、C5、C6、C7, 见图 1)为对象, 考查其理论塔板数、分离度、灵敏度和拖尾因子。应用正交实验设计方案[L 9(34)]优化实验条件, 最终选择检测波长为270 nm, 进样体积为20 μL, 流动相B构成为0.1%磷酸水溶液。经过反复流动相梯度优化, 获得基线平整、峰窄尖无拖尾、分离度高的HPLC流出曲线, 见图 1。
2.2 HPLC指纹图谱构建与评价本研究采集了4个产地110份益母草, 经HPLC检测后, 没有发现隶属于产地的特异色谱峰, 因此应用遗传-偏最小二乘法(GA-PLS)筛选特征变量[14], 获得7个与产地相关的特征峰(C1-C7, 见图 1), 并以此构建益母草的HPLC指纹图谱。
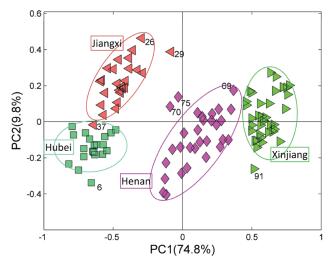
首先应用PCA探讨110份益母草之间的相似度关系, 结果见图 2。相同产地药材的相似度较高, 各自聚为一类, 湖北药材聚集在第3象限, 江西药材聚集在第2象限, 新疆药材聚集在PC1轴较正的1、4象限, 河南药材则处于其他3类样品中间区域; 但有少数样品与同产地其他药材相似度较低, 例如湖北#6、江西#29和#37、河南#70和#75、新疆#91。
|
| 图 2 4个产地110份益母草的HPLC特征峰的PCA图 |
为验证该HPLC指纹图谱的效能, 应用有监督模式识别方法评价其客观辨识度。首先用Kennard and Stone法将110份益母草分为两组:校正集(73份)和预报集(37份), 然后应用LDA、LS-SVM和RBF-NN分别构建学习模型并比较模型的辨识能力。LDA模型结果:校正集识别率95.9%, 预报集识别率94.6%;LS-SVM模型(γ=161.2, σ2=1.5)结果:校正集识别率97.3%, 预报集识别率94.6%;RBF-NN模型(隐藏神经元数7, 增加神经元数12, 均方根差10-4)结果:校正集识别率98.6%, 预报集识别率97.3%;3个模型均取得了较好的识别率, RBF-NN模型最优。
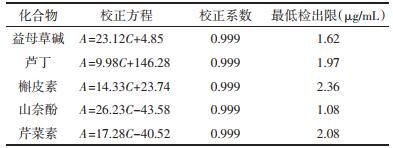
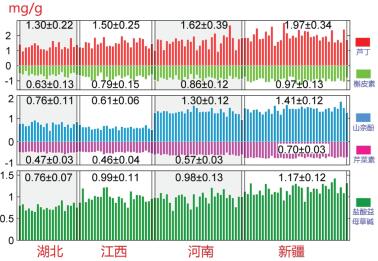
2.3 特征峰定性和定量分析与标准品HPLCDAD、MS数据比对后, 5个特征峰被准确鉴定, 分别是盐酸益母草碱(C1)、芦丁(C4)、槲皮素(C5)、山奈酚(C6)和芹菜素(C7), 见表 2。之后用HPLC外标法测定这5种特征组分的含量, 见图 3。
|
| 图 3 4种产地益母草的特征组分含量分布 |
湖北、河南和新疆益母草中4种黄酮类化合物含量呈现一致的分布, 即芦丁含量最高, 山奈酚次之, 之后是槲皮素, 芹菜素含量最低, 而江西产药材槲皮素的含量明显高于山奈酚(P < 0.001);新疆和河南产药材4种黄酮类化合物含量较高, 分别居第1、2名; 湖北、江西产药材的山奈酚、槲皮素、芹菜素含量较低; 江西和河南产药材芦丁的含量差异无统计学意义, 湖北和江西产药材芹菜素的含量差异无统计学意义。
110份益母草的盐酸益母草碱的含量范围是0.66~1.43 mg/g, 新疆产药材含量最高, 湖北产药材含量最低, 江西和河南产药材含量相近并居中。总之, 多组分定量分析发现新疆、河南益母草质量较好, 不同产地药材中部分化合物具有相近的含量。
3 讨论中药依赖其所含的多种化学成分共同发挥疗效, 有研究证实益母草的药效成分受环境、产地、种植方式、收割时间、原材料初加工方式等因素的影响较大[15-16], 其质量控制一直是个难题。相较于传统的经验鉴别和单组分分析, 色谱指纹图谱技术由于其整体性的特征备受青睐。事实上, 美国食品药品监督管理局、英国草药协会、加拿大药用与芳香植物协会以及德国药用植物协会均已批准将色谱指纹图谱作为中药的质量控制规范之一[17-19]。色谱指纹图谱的另外一个特征是模糊性, 强调准确的辨识, 也就是强调样品之间的相似度。本研究在指纹图谱相似度分析的基础上, 应用模式识别方法构建定性预报模型, 以评价HPLC指纹图谱的有效性和对未知样品的辨识度, 取得了较好的结果。然而, 指纹图谱无法在"量"上为待分析物提供质量保证, 而这正是多组分定量分析的优势。
《中华人民共和国药典》(简称药典)2015版规定益母草饮片盐酸水苏碱的含量不得低于0.40%, 盐酸益母草碱的含量不得低于0.04%[20]; 盐酸水苏碱具有兴奋子宫、抗炎、抗血栓等多种药理作用, 盐酸益母草碱主要发挥抗炎、抗凋亡、调节内环境Ca2+稳态等效用[2]。然而药典并未对益母草中黄酮类化合物的含量提出要求, 作为饮食中的非能量部分, 黄酮类化合物一直被认为对健康有促进作用, 尤其是可降低心脑血管疾病的病死率[21]。益母草中含量较高的黄酮类化合物包括芦丁、槲皮素、山奈酚、芹菜素等, 具有抗炎、抗氧化活性。
有效的制剂以及药效的发挥需要优质的原料药保证, 本研究探讨HPLC指纹图谱技术联合5组分定量分析在益母草原料药质量控制中的应用。首先应用HPLC检测4个产地110份益母草, 在变量筛选方法(GA-PLS)的帮助下得到7个特征峰, 并以此构建HPLC指纹图谱; 无监督/有监督模式识别模型均证实该指纹图谱具有很好的辨别度, 可准确鉴别不同产地的益母草, 以RBF-NN模型为最优(校正集识别率为98.6%, 预报集识别率为97.3%); 结合标准品的HPLC-DAD、MS数据, 其中5个特征峰被确定为益母草碱、芦丁、槲皮素、山奈酚和芹菜素; 最后应用HPLC外标法检测该5种特征组分的含量, 结果显示新疆和河南产药材的各组分含量较高, 河南、江西和湖北产药材的部分化合物具有相近的含量。总之, HPLC指纹图谱技术联合多组分定量分析, 可用于益母草的产地鉴别以及质量评价。
| [1] |
樊江波, 黄琳红. 益母草活性成分芫花素对小鼠凝血及抗炎作用的研究[J]. 西安交通大学学报(医学版), 2019, 40(1): 158-161. FAN J B, HUANG L H. Pharmacological effects of the active ingredient genkwanin in Leonurus on coagulation and anti-inflammation in mice[J]. Journal of Xi'an Jiaotong University(medical sciences), 2019, 40(1): 158-161. |
| [2] |
LIU X H, PAN L L, ZHU Y Z. Active chemical compounds of traditional Chinese medicine herba leonuri:implications for cardiovascular diseases[J]. Clinical & Experimental Pharmacology & Physiology, 2012, 39(3): 274-282. |
| [3] |
邓灿, 刘丽丽, 陈玥, 等. 益母草化学成分研究III[J]. 天津中医药大学学报, 2014, 33(6): 362-365. DENG C, LIU L L, CHEN Y, et al. Study on chemical constituents of Leonurus japonicus Houtt. Ⅲ[J]. Journal of Tianjin University of Traditional Chinese Medicine, 2014, 33(6): 362-365. |
| [4] |
乔晶晶, 吴啟南, 薛敏, 等. 益母草化学成分与药理作用研究进展[J]. 中草药, 2018, 49(23): 212-225. QIAO J J, WU Q N, XUE M, et al. Research progress on chemical components and pharmacological effects of Leonurus japonicas[J]. Chinese Traditional and Herbal Drugs, 2018, 49(23): 212-225. |
| [5] |
张雪, 宋玉琴, 杨雨婷, 等. 益母草活血化瘀化学成分与药理作用研究进展[J]. 药学评价研究, 2015, 38(2): 214-217. ZHANG X, SONG Y Q, YANG Y T, et al. Research progress on chemical components of Leonurus japonicas and their pharmacological effects of activating blood and resolving stasis[J]. Drug Evaluation Research, 2015, 38(2): 214-217. |
| [6] |
朱启亮, 黄玉梅, 高明, 等. 不同产地、部位和采收期益母草中药效成分研究[J]. 中药材, 2017, 40(12): 2828-2831. ZHU Q L, HUANG Y M, GAO M, et al. Study on pharmacodynamic components of Leonurus heterophylla from different places of origin and harvest period[J]. Journal of Chinese Medicinal Materials, 2017, 40(12): 2828-2831. |
| [7] |
DONG S Y, HE J, HOU H P, et al. Quality assessment of Herba Leonuri based on the analysis of multiple components using normal and reversed-phase chromatographic methods[J]. Journal of Separation Science, 2017, 40(23): 4482-4494. |
| [8] |
乔晶晶, 吴啟南, 许一鸣, 等. HPLC法同时测定益母草中4种成分[J]. 中成药, 2018, 40(11): 2467-2471. QIAO J J, WU Q N, XU Y M, et al. Simultaneous determination of four constituents in Leonurus japonicas[J]. Chinese Traditional Patent Medicine, 2018, 40(11): 2467-2471. |
| [9] |
杨超, 包小红, 耿超, 等. 益母草注射液指纹图谱的研究[J]. 药物分析杂志, 2016, 36(7): 1219-1224. YANG C, BAO X H, GENG C, et al. Fingerprint analysis of Leonurus japonicas injection[J]. Chinese Journal of Pharmaceutical Analysis, 2016, 36(7): 1219-1224. |
| [10] |
赵荣, 肖会敏, 何悦, 等. 调经益母片的高效液相色谱指纹图谱及成分定量研究[J]. 安徽医药, 2018, 22(7): 1263-1267. ZHAO R, XIAO H M, HE Y, et al. Study on fingerprint of Tiaojingyimu tablet and quantitative analysis of components by HPLC[J]. Anhui Medical and Pharmaceutical Journal, 2018, 22(7): 1263-1267. |
| [11] |
李宝辉, 李冬晖, 倪永年. 化学统计学在不同年份和不同产地郁金鉴别中的应用[J]. 分析科学学报, 2019, 35(1): 50-54. LI B H, LI D H, NI Y N. Discrimination of radix curcumae on the basis of their geographical origin and batches by chemometrics[J]. Journal of Analytical Science, 2019, 35(1): 50-54. |
| [12] |
Ferreiro-González M, ESTRELLA E B, Guillén-Cueto L, et al. Rapid quantification of honey adulteration by visible-near infrared spectroscopy combined with chemometrics[J]. Talanta, 2018(188): 288-292. |
| [13] |
DONG W J, NI Y N, KOKOT S. A novel near-infrared spectroscopy and chemmometrics method for rapid analysis of several chemical components and antioxidant activity of mint(Mentha haplocalyx Briq.) samples[J]. Applied Spectroscopy, 2014, 68(2): 245-254. |
| [14] |
YIN L H, ZHOU J M, CHEN D D, et al. A review of the application of near-infrared spectroscopy to rare traditional Chinese medicine[J]. Molecular and Biomolecular Spectroscopy, 2019(221): 117208-117216. |
| [15] |
晁志, 王厄舟, 周秀佳. 益母草药材中生物碱含量与产地生态环境的关系[J]. 第一军医大学学报, 2000, 20(6): 504-506. CHAO Z, WANG E Z, ZHOU X J. Relationship between alkaloid contents and growth environment of Yimu Cao(Herba Leonuri)[J]. Journal of First Military Medical University, 2000, 20(6): 504-506. |
| [16] |
谭亚杰, 濮宗进, 唐于平, 等. 基于UPLC-QTRAP®/MS2方法评价不同干燥方式对益母草中化学成分的影响[J]. 中草药, 2019, 50(7): 1576-1586. TAN Y J, PU Z J, TANG Y P, et al. Effects of different drying methods on multiple chemical components in Leonurus japonicas based on UPLC-QTRAP®/MS2[J]. Chinese Traditional and Herbal Drugs, 2019, 50(7): 1576-1586. |
| [17] |
ZHANG C, ZHENG X, NI H, et al. Discovery of quality control markers from traditional Chinese medicines by fingerprint-efficacy modeling:current status and future perspectives[J]. Journal of Pharmaceutical & Biomedical Analysis, 2018(159): 296-304. |
| [18] |
张兵, 张丽娜, 韩鹏军, 等. 白术中3种内酯成分的含量测定及指纹图谱研究[J]. 天津中医药大学学报, 2018, 37(5): 411-415. ZHANG B, ZHANG L N, HAN P J, et al. Determination of 3 atractylenolides in Atractylodes macrocephala Koidz. and the study of the fingerprint[J]. Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(5): 511-415. |
| [19] |
尹艳微, 贾琪, 马文娟, 等. 淫羊藿药材的UPLC指纹图谱研究[J]. 天津中医药大学学报, 2019, 38(5): 482-485. YIN Y W, JIA Q, MA W J, et al. UPLC fingerprint of Epimedium herbs[J]. Journal of Tianj in University of Traditional Chinese Medicine, 2019, 38(5): 482-485. |
| [20] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2015. National Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China[M]. Beijing: China Medical Science and Technology Publishing House, 2015. |
| [21] |
WOJTYNIAK K, SZYMANSKI M, MATLAWSKA I. Leonurus cardiaca L. (motherwort):a review of its phytochemistry and pharmacology[J]. Phytotherapy research, 2013, 27(8): 1115-1120. |
 2020, Vol. 39
2020, Vol. 39