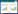文章信息
- 王宝剑, 高景华, 孙武, 高春雨, 魏戌, 杨克新, 张平, 冯敏山, 银河, 梁龙, 王源, 张静茹
- WANG Baojian, GAO Jinghua, SUN Wu, GAO Chunyu, WEI Xu, YANG Kexin, ZHANG Ping, FENG Minshan, YIN He, LIANG Long, WANG Yuan, ZHANG Jingru
- 退行性腰椎管狭窄症:NASS循证医学指南解读
- Degenerative lumbar spinal stenosis:interpretation of NASS guidelines for evidence-based medicine
- 天津中医药大学学报, 2020, 39(4): 398-402
- Journal of Tianjin University of Traditional Chinese Medicine, 2020, 39(4): 398-402
- http://dx.doi.org/10.11656/j.issn.1673-9043.2020.04.08
-
文章历史
收稿日期: 2020-01-20
2. 中医正骨技术北京市重点实验室, 北京 100102
2. Beijing Key Laboratory of Orthopedic Technology of Traditional Chinese Medicine, Beijing 100102, China
退行性椎管狭窄症(DLSS)是指由于后天退变等因素(如关节突关节增生、韧带增厚)造成椎管、神经根管狭窄,刺激或压迫神经根或马尾神经,出现以腰腿痛、间歇性跋行为主要特征的临床综合征[1]。其发病率与日益增,在一般人群中,腰椎椎管相对狭窄(椎管直径≤12 mm)的发病率占22.5%,绝对狭窄(椎管直径≤10 mm)的发病率占7.3%,而在≥60岁人群中,该发病率分别增至47.2%和19.4%[2]。本病已成为导致中老年人腰腿疼痛、活动功能受限的常见疾病,严重威胁中老年人群的生活质量和身心健康[3]。
目前,关于DLSS的诊断、治疗等方面还存在诸多争议,许多问题尚未取得共识,如DLSS的自然病程、非手术治疗的意义、手术治疗在减压的基础上是否需要融合等。2007年北美脊柱外科协会(NASS)制定了第1版循证临床实践指南,2011年完成了第2版《退变性腰椎管狭窄症诊疗指南》(以下简称《指南》)[4],根据循证学依据以问答的方式对本病进行了阐述,旨在为临床医师提供最佳的诊疗方案。笔者在充分研读最新版NASS《指南》的基础上,结合目前最新研究进展,对DLSS的临床诊治展开评述,以供临床医生参考。《指南》依然采用标准化证据推荐等级区分方法(表 1),以便读者理解证据等级和推荐强度。
《指南》予退DLSS的最佳定义:由于腰椎退变因素导致的椎管面积减少,压迫神经、血管等引起臀部或下肢疼痛、无力,伴或不伴有腰痛症状的临床综合征。其特点是如行走等直立体位会诱发神经源性跛行,而前屈弯腰、坐卧休息上述症状会缓解。
在缺乏可靠证据支持下,《指南》工作组专家共识为:临床中轻度及中度的DLSS患者占33%~50%,并且极少患者会出现快速进展的、灾难性的神经退变。由于绝大部分临床研究都排除了严重的神经损害患者,因此基于目前文献,不足以从临床或影像学角度定义DLSS的自然病程。
2 诊断 2.1 症状步行或直立后臀部或下肢症状加重,但坐位或前屈位上述症状又可以减轻。而步行或直立没有使疼痛加重的患者考虑该病的可能性较低,推荐等级:C级。另外,患者主诉的腰痛及下肢疼痛症状对该确诊该病的证据不足,推荐等级:Ⅰ级。
2.2 体征目前没有足够的证据支持或反对某一体格检查能有助于DLSS的诊断,这包括Romberg征阳性、大腿后伸时疼痛加重、感觉运动障碍、腿抽筋和跟腱反射异常,推荐等级:Ⅰ级。
但《指南》未提及老年患者的下肢疼痛症状可能是由血管病变所导致的血管源性疼痛[5]。Konno等[6]认为,诊断DLSS必须保证患者下肢血管系统检查的完整以排除血管源性跋行。这可以通过追溯患者病史、观察患者下肢皮肤色泽与温度、触诊足背动脉搏动、脚踏车运动试验、下肢血管彩超等检查来鉴别[7]。
2.3 影像学检查在符合DLSS病史及体格检查的患者中,磁共振成像(MRI)是最合适且无创的影像学检查方法,可以用来证实椎管的狭窄或神经的受压情况;对于有MRI禁忌症或者不能确定的患者,电子计算机扫描(CT)脊髓造影是最合适的替代检查;如果以上检查均为禁忌症或不能确定,可采用CT检查,推荐等级:B级。
目前为止,《指南》认为没有足够证据支持或反对DLSS的临床症状或活动功能与影像学(MRI、CT、CT脊髓造影)所表现的椎管狭窄的程度有相关性,推荐等级:Ⅰ级。在影像学表现与DLSS症状的相关性上,Sirvanci等[8]通过分析63名DLSS患者ODI(Oswestry Disability Index)与MRI表现的发现,其功能障碍与椎管狭窄程度之间的相关性较差。但Ogikubo等[9]通过研究80例中央椎管狭窄患者的典型症状体征与马尾神经最小横截面面积(mCSA)之间的关系,发现较小的mCSA与更重的腰腿疼痛、更短的行走距离以及更低的生活质量之间有直接相关关系。而Geisser等[10]通过50例患者的回顾性研究认为,椎管前后径与患者的疼痛程度、感觉功能以及步行能力之间没有相关性。
《指南》工作组专家认为影像学检查是一线的诊断方法。而关于F波、H反射、运动诱发电位(MEP)、运动神经传导研究、体感诱发电位(SSEP)、皮肤感觉诱发电位(DSEP)和下肢肌电图检查对DLSS诊断的确定没有足够的证据支持,推荐的等级:Ⅰ级。
此外,《指南》并没有提及DLSS的影像学分级的相关内容。目前国内外文献报道了一些基于MRI的影像学分级评分系统,但仍没有任何一个被广泛接受。如Song等[11]定义了一种以最狭窄节段蛛网膜下腔阻塞程度的3度分级法;Lee等[12]基于T2像轴位片上马尾神经的分离或聚拢程度将该病分为4级;Bartynski等[13]将侧隐窝狭窄程度分为4级。这些影像学分级基本上均围绕硬膜囊受压、神经根改变以及脑脊液流畅程度来进行描述,但其临床价值仍有待提高。
3 治疗 3.1 保守治疗本病的保守治疗方法主要包括药物、理疗、功能锻炼、手法推拿、健康宣教、辅助治疗(如支具、牵引、电刺激等)、硬膜外类固醇注射疗法以及综合保守治疗等方法。
1)《指南》提及的药物治疗有降钙素肌注、鲑鱼降钙素鼻喷、甲钴胺口服、脂化前列腺素E1静脉注射、前列腺素E1口服、加巴喷丁口服。但目前没有足够证据支持或反对药物治疗DLSS,推荐等级:Ⅰ级。
2)目前没有足够证据支持或反对单独使用物理治疗或运动锻炼治疗DLSS,推荐等级:Ⅰ级。但《指南》工作组专家基于临床经验达成的共识是理疗和运动作为综合保守治疗的一部分是有效的,可以积极使用。
3)目前没有足够证据支持或反对使用脊柱推拿手法治疗DLSS,推荐等级:Ⅰ级。
4)硬膜外类固醇注射(ESI)可以短期内改善间歇性跛行或神经根症状(2周~6个月),也有研究表明该疗法长期有效(21.5~24个月),推荐等级:B级。而对于该类患者,影像学引导下的经椎间孔多部位ESI或骶管注射有中期止痛效果(3~36个月),推荐等级:C级。另外,造影增强透视比常规X线透视更能提高给药的准确性,推荐等级:A级。
5)在辅助治疗中,没有足够证据支持或反对应用支具、牵引、针灸、电刺激或经皮电刺激治疗DLSS,推荐等级:Ⅰ级。而紧身腰围可以增加DLSS患者的步行距离并能改善疼痛,而一旦去除腰围后该疗效不能维持,推荐等级:B级。
6)药物等综合保守治疗:《指南》工作组专家推荐轻度DLSS患者考虑药物等综合保守治疗方案;而中度患者也适合采用综合保守方案,推荐等级:C级;另外,药物等综合保守治疗可以长期改善大部分患者预后(2~10年),推荐等级:C级。Amundsen等[14]报道了随访10年的前瞻性研究,提供的证据水平为4级,即护腰、健康宣教、理疗等初期的综合保守疗法适用于轻中度DLSS患者,效果不满意的患者可采用手术减压治疗,且手术疗效优于保守疗效。Simotas等[15]报道了一项病例系列研究,提供的证据水平为4级,通过综合保守治疗后(运动锻炼、口服止痛药、ESI),71%的DLSS患者在3年内症状无变化或得以改善,11%患者病情恶化,18%的患者已进展到需要手术治疗的程度。
3.2 手术治疗1)椎管减压术:对于中度及重度DLSS患者,椎板减压术可以改善预后,推荐等级:B级。Athiviraham等[16]报道了前瞻性对照试验,提供的治疗性证据水平为2级,其2年随访结果显示,椎管减压组、椎管减压加融合组和非手术治疗组Roland-Morris功能障碍问卷的评分平均改善值分别为6.9、6.1和1.2,同时手术治疗患者有一定的残余症状,但这也可能与症状较重的患者多数选择了手术治疗有关。Malmivaara等[17]的1项证据水平为2级的前瞻性随机对照试验发现,对于中度DLSS患者,手术减压组相较于药物等非手术治疗组的腰腿痛、腰椎功能的改善效果相更好,但行走能力的改善无差异。Weinstein等[18-19]纳入645例DLSS患者,其中289例行前瞻性随机对照研究,36例行前瞻性队列研究,结果显示手术治疗组早期的ODI和RMDQ评分(Roland Morris Disability Questionnaire)等指标改善情况明显优于非手术治疗组,该优势在随访2、4年时依然明显,而非手术治疗组仅为“轻微改善”,但同时手术组9%的患者出现了硬膜囊破裂,13%的患者需要再次手术,该研究的证据水平为2级。
另外《指南》提出,对于以下肢症状为主且不合并腰椎失稳的患者,建议只进行手术减压。推荐等级:B级。Grob等[20]报道的1项随机对照试验中,将45例相邻椎体前后位移小于5 mm的DLSS患者随机分为3组:椎板切开并内侧小关节切除减压组、减压并最狭窄节段融合组、减压并所有累及节段融合组,结果显示3组患者在行走能力及疼痛程度上均有改善,但差别无统计学意义。该研究的证据水平为2级,即在相邻椎体前后位移小于5 mm的DLSS患者中,单纯减压术与减压加融合术的疗效无差别。Yone等[21]报道了1项前瞻性对照研究,66例经保守治疗无效的DLSS患者中有33例合并腰椎失稳,其中19例行减压加融合术,14例行单纯减压术,而另外33[1]例不合并腰椎失稳的患者行单纯减压术。结果显示合并失稳的减压加融合组与不合并失稳的单纯减压组共80%患者取得了较好的疗效,而合并失稳单纯减压组只有43%患者有较好的疗效。该研究的证据水平为2级,即对于DLSS合并腰椎失稳的患者,减压加融合的手术疗效优于单纯减压。
2)棘突间撑开装置:目前尚缺乏充分证据支持或反对DLSS患者置入棘突间撑开装置,推荐级别:Ⅰ级。
棘突间撑开装置可以增加负重或伸直状态下的椎管容积,因而对椎管起到了间接的减压作用。Zucherman等[22]报道的1项前瞻性随机对照试验中,将191例轻中度DLSS患者随机分为植入X-Stop棘突间撑开器组(100例)和非手术治疗组(91例,包括健康宣教、运动锻炼、类固醇注射、口服非甾体类抗炎药、按摩、理疗等)。2年后随访发现,相较于基线水平,X-Stop组平均症状评分改善45.4%,对照组改善7.4%,X-Stop组平均功能评分改善44.3%,对照组为-0.4%。该研究提供的治疗性证据水平为1级,即在轻中度DLSS患者中X-Stop的疗效比非手术治疗更有优势。
然而,目前有文献系统评价表明[23],后路腰椎融合、Coflex、Wallis和X-stop装置在缓解疼痛、改善生活质量、恢复椎间盘高度和腰椎功能方面具有相同的效果,但3种棘突间装置可以降低邻近节段退变的发生率且手术节段的活动范围更大。Wu等[24]通过系统综述认为,棘突间装置对于DLSS患者在中短期有良好的治疗效果,且手术时间、估计失血量、住院时间均显著少于融合组患者,但其复发率、翻修率及手术成本较高,因而手术前应着重考虑各种棘突间装置的适应症及风险。
另外,《指南》提出高龄并不是DLSS的手术禁忌症,75岁及以上的患者仍建议手术减压治疗,其与65~74岁患者的手术疗效无差异,推荐等级:C级。
4 未来研究方向2011年版DLSS指南对于未来研究也提供了建议,其主要建议如下:
1)诊断方面:①建议进一步研究患者下肢疼痛或腰痛症状的对DLSS诊断的可靠性;②通过腰椎横断面影像的中央管、侧隐窝和椎间孔的狭窄面积,继续制定可靠和可重复的诊断标准。
2)保守治疗方面:①以大样本、双盲、长期随访的随机对照试验来研究降钙素治疗DLSS的潜在疗效;②在伦理具有可行性的前提下,设计一项将标准化手法、针灸、牵引或电刺激与未治疗自然病程的DLSS患者进行比较的对照试验;③建议将DLSS神经源性跛行患者分成两组(ESI组及生理盐水注射组),进行大样本、双盲、随机对照临床试验,并至少随访两年;④开展1项对软腰围、硬腰围与无腰围治疗DLSS进行对比的研究,评价指标采用视觉模拟评分法(VAS)评分、步行距离以及公认的生活质量量表如ODI、健康调查简表(SF-36)。
3)手术治疗方面:①开展大样本、多中心、随机对照试验研究,对比中度DLSS患者中减压手术组、药物等非手术治疗组、未治疗组的疗效差异;②开展大样本、多中心、随机对照试验研究,对比中度DLSS患者中棘突间撑开装置组、微创椎板减压组、药物等综合保守治疗组、未治疗自然病程组的疗效差异。
综上,笔者认为指南将重点放在手术方面,而在DLSS保守治疗方面,由于大部分治疗方案均缺乏循证医学证据,因而指南并未给出明确推荐的干预措施。但如手法、针灸、功能锻炼等中医药方案的治疗价值也应予以重视,因此建议在小样本随机对照试验(RCT)或病例观察等前期的研究基础上,适当开展前瞻性、大样本、多中心、长期随访的RCT以评价其疗效及安全性,为今后指南提供补充与替代医学方面的高等级证据支持。
| [1] |
HARTVIGSEN J, HANCOCK M J, KONGSTED A, et al. What low back pain is and why we need to pay attention[J]. Lancet, 2018(391): 2356-2367. |
| [2] |
KALICHMAN L, COLE R, KIM D H, et al. Spinal stenosis prevalence and association with symptoms:the framingham study[J]. Spine Journal, 2009(9): 545-550. |
| [3] |
AMMENDOLIA C, SCHNEIDER M, WILLIAMS K, et al. The physical and psychological impact of neurogenic claudication:the patients' perspectives[J]. The Journal of the Canadian Chiropractic Association, 2017, 61(1): 18-31. |
| [4] |
KREINER D S, SHAFFER W O, BAISDEN J L, et al. An evidence-based clinical guideline for the diagnosis and treatment of degenerative lumbar spinal stenosis (update)[J]. Spine Journal, 2013(13): 734-743. |
| [5] |
BACKSTROM K M, WHITMANJ M, Flynn T W. Lumbarspinalstenosisdiagnosisandmanagementoftheagingspine[J]. Manual Therapy, 2011, 16(4): 308-317. DOI:10.1016/j.math.2011.01.010 |
| [6] |
KONN O S, HAYASHINO Y, FUKUHARA S, et al. Development of a clinical diagnosis support tool to identify patients with lumbar spinal stenosis[J]. EuropeanU Spine Journal, 2007, 16(11): 1951-1957. DOI:10.1007/s00586-007-0402-2 |
| [7] |
FRITZ J M, ERHARD R E, DELLITTO A, et al. Preliminary results of the use of a two-stage treadmill test as a clinical diagnostic tool in the diferential diagnosis of lumbar spinal stenosis[J]. Journal of Spinal Disorders& Techniques, 1997, 10(5): 410-416. |
| [8] |
SIRVANC M, BHATIA M, GANIYUSUFOGLU K A, et al. Degenerative lumbar spinal stenosis:correlation with oswestry disability index and MR imaging[J]. European Spine Journal, 2008, 17(5): 679-685. DOI:10.1007/s00586-008-0646-5 |
| [9] |
OGIKUBO O, FORSBERG L, HANSSON T. The relationship between thecross-sectional area of the cauda equina and the preoperative symptoms in central lumbar spinal stenosis[J]. Spine, 2007, 32(13): 1423-1428. DOI:10.1097/BRS.0b013e318060a5f5 |
| [10] |
GEISSER M E, HAIG A J, TONG H C, et al. Spinal canal size and clinical symptoms among persons diagnosed with lumbar spinal stenosis[J]. Clinical Journalof Pain, 2007, 23(9): 780-785. DOI:10.1097/AJP.0b013e31815349bf |
| [11] |
SONG K S, JANG E C, JUNG H J, et al. Observer variability in the evaluation of multiple lumbar stenosis by routine MR——myelography and MRI[J]. Journal of Spinal Disorders& Techniques, 2008, 21(8): 569-574. |
| [12] |
LEE G Y, LEE J W, CHOI H S, et al. A new grading system of lumbar central canal stenosis on MRI:an easy and reliable method[J]. Skeletal Radiology, 2011, 40(8): 1033-1039. DOI:10.1007/s00256-011-1102-x |
| [13] |
BARTYNSKI W S, LIN L. Lumbar root compression in the lateral recess:MR imaging, conventional myelography, and CT myelography com parison with surgical confirmation[J]. American Journal of Neuroradiology, 2003, 24(3): 348-360. |
| [14] |
AMUNDSEN T, WEBER H, NORDAL H J, et al. Lumbar spinal stenosis:conservative or surgical management:A prospective 10-year study[J]. Spine, 2000, 25(11): 1424-1435. DOI:10.1097/00007632-200006010-00016 |
| [15] |
SIMOTAS A C. Nonoperative treatment for lumbar spinal stenosis[J]. Clinical Orthopaedics and Related Research, 2001(384): 153-161. |
| [16] |
ATHIVIRAHAM A, YEN D. Is spinal stenosis better treated surgically or nonsurgically[J]. Clinical Orthopaedics and Related Research, 2007(458): 90-93. |
| [17] |
MALMIVAARA A, SLLATIS P, HELIOVAARA M, et al. Surgical or nonoperative treatment for lumbar spinal stenosis a randomized controlled trial[J]. The Spine Journal, 2007, 32(1): 1-8. |
| [18] |
WEINSTEIN J N, TOSTESONTD, LURIEJD, et al. Surgical versus nonoperative treatment for lumbar spinal stenosis four-year results of the spine patient outcomes research trial[J]. The Spine Journal, 2010, 35(14): 1329-1338. DOI:10.1097/BRS.0b013e3181e0f04d |
| [19] |
WEINSTEIN J N, TOSTESON T D, LURIE J D, et al. Surgical versus nonsurgical therapy for lumbar spinal stenosis[J]. The New England Journal of Medicine, 2008, 358(8): 794-810. DOI:10.1056/NEJMoa0707136 |
| [20] |
GROB D, HUMKE T, DVORAK J. Degenerative lumbar spinal stenosis. Decompression with and without arthrodesis[J]. Journal of Bone and Joint Surgery-American, 1995, 77(7): 1036-1041. DOI:10.2106/00004623-199507000-00009 |
| [21] |
YONE K, SAKOU T. Usefulness of posner's defnition of spinal instability for selection of surgical treatment for lumbar spinal stenosis[J]. Journal of Spinal Disorders & Techniques, 1999, 12(1): 40-44. |
| [22] |
ZUCHERMANJ F, HSUK Y, HARTJEN CA, et al. A multicenter, prospective, randomized trial evaluating the X-STOP interspinous process decompression system for the treatment of neurogenic intermittent claudica-tion:two-year follow-up results[J]. The Spine Journal, 2005, 30(12): 1351-1358. DOI:10.1097/01.brs.0000166618.42749.d1 |
| [23] |
MO Z M, LI D, ZHANG R W, et al. Comparative effectiveness and safety of posterior lumbar interbody fusion, coflex, wallis, and X-stop for lumbar degenerative diseases:a systematic review and network meta-analysis[J]. Clinical Neurology and Neurosurgery, 2018(172): 74-81. |
| [24] |
WU A M, ZHOU Y, LI Q L, et al. Interspinous spacer versus traditional decompressive surgery for lumbar spinal stenosis:asystematic review and meta-analysis[J]. PLoS ONE, 2014, 9(5): e97142. DOI:10.1371/journal.pone.0097142 |
 2020, Vol. 39
2020, Vol. 39