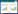文章信息
- 马旭彤, 刘羿廷, 张瀛, 张立强, 皮佳鑫, 刘志东
- MA Xutong, LIU Yiting, ZHANG Ying, ZHANG Liqiang, PI Jiaxin, LIU Zhidong
- 动物类中药材稳定性研究中适宜条件的选择-以水蛭、地龙为例
- Selection of suitable conditions in the stability study of animal Chinese medicinal materials:takinghirudoesand pheretimasas examples
- 天津中医药大学学报, 2020, 39(4): 459-463
- Journal of Tianjin University of Traditional Chinese Medicine, 2020, 39(4): 459-463
- http://dx.doi.org/10.11656/j.issn.1673-9043.2020.04.20
-
文章历史
收稿日期: 2020-01-14
2. 天津中医药大学中医药研究院, 天津 301617;
3. 天津中医药大学, 现代中药发现与制剂技术教育部工程中心, 天津 301617;
4. 牡丹江友搏药业有限责任公司, 牡丹江 157000
2. Institute of Traditional Chinese Medicale, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China;
3. Engineering Rescarch Cencer of Modern Chinese Medicine Discovery and preparation technique, Ministry of Education, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China;
4. Mudanjiang Youbo Pharmaceutical Limited Liability Company, Mudanjiang 157000, China
稳定性是药品必须具有的基本属性,是其质量可控性的主要内容之一。中药材质量问题较为复杂,除采收期和采收年限影响其质量外,在生产、贮存、使用过程中会导致药材发生变质,从而降低疗效或产生有毒物质。故稳定性也是直接影响中药材、中药饮片和中成药的临床疗效的重要环节之一。
动物类中药材,指来源于动物的干燥体、除去内脏的动物干燥体、部分器官、病理或生理产物等药用中药材,是中药材的重要组成部分,具有强心、镇静、抗血栓、抗惊厥等作用[1],体现独特的药用价值。目前,中药材稳定性多聚焦在植物药,通常以植物药中主要有效成分、特殊成分为依据,检测不同储存条件下有效成分的含量,通过比较含量变化得到药材稳定性结论。然而,动物类中药材稳定性研究基础薄弱,缺乏针对动物药易腐败变质特点的稳定性评价手段。因此,如何能结合动物类中药材温度敏感及湿度关联性大的特点,制定符合目前动物类中药材应用实际的稳定性实验方法与指标,是解决动物类中药材质量控制问题的关键。
水蛭和地龙是疏血通注射液的主要成分,也是临床常用的动物类中药材。课题组前期依据稳定性研究指导原则,进行了稳定性实验,发现常规条件下,水蛭和地龙药材在短时间内即出现发霉变质现象,导致稳定性实验无法进行。因此,文章对实验条件进行了优化,设定了更为温和的实验条件,进一步开展了水蛭、地龙药材稳定性补充研究,为动物类中药材选择适宜条件开展稳定性研究提供重要实验依据。
1 仪器与药品 1.1 仪器十万分之一天平(梅特勒托利多国际贸易有限公司,型号XP205);pH计(德国Sartorius公司,型号PB-10);离心机(赛默飞世尔科技公司,型号SORVALL ST 16R Centrifuge);电热恒温水浴锅(天津泰斯特仪器有限公司,型号DK-98-ⅡA);马弗炉(天津中环电炉股份有限公司,型号SX-G07123);电热鼓风干燥箱(上海博讯实业有限公司医疗设备厂,型号BG2-140);安捷伦高效液相色谱仪(美国安捷伦公司,Agient1260型高效液相色谱仪)。
1.2 试药和试剂水蛭(批号171207,181101,181202)、地龙(批号171015,171016,171017)药材由牡丹江友搏药业有限责任公司提供;乙酸乙酯(纯度:99.5%天津市康科德科技有限公司);硫酸(纯度:96%天津市大茂化学试剂厂);盐酸(纯度:38%天津市大茂化学试剂厂)均为分析纯;纤维蛋白原(北京索莱宝科技有限公司);凝血酶(北京索莱宝科技有限公司)为生物试剂。
2 方法与结果 2.1 实验条件的选择前期参考药典稳定性实验指导原则,进行了稳定性实验。但由于实验过程中水蛭地龙大量霉变,因此,依据药典稳定性指导原则中对温度特别敏感原料药物的(低温)实验条件以及包装在半透性容器中的药物制剂的(低湿)实验条件,对实验条件进行优化和改变,在更温和的条件下,继续实验。实验条件见表 1。
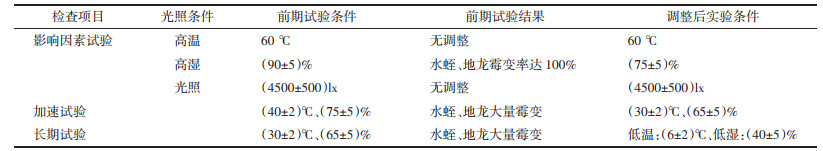
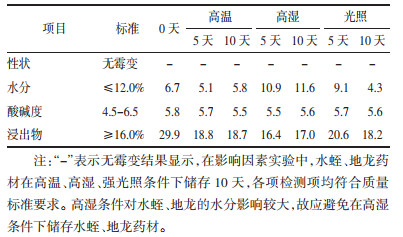
水蛭、地龙为《中华人民共和国药典》一部收载品种,水蛭检测项目包括鉴别、水分、含量测定等,地龙的检测项目包括鉴别、酸碱度、浸出物等,考察项目及标准见表 2。
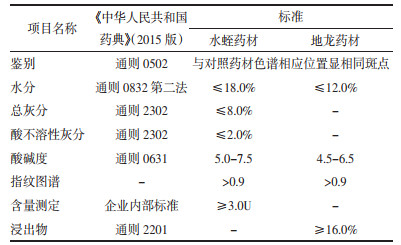
在高温实验(温度60 ℃),高湿实验(相对湿度(75±5)%)和强光照(4 500±500)lx)[2]条件下进行影响因素实验,水蛭结果见下表 3;地龙结果见下表 4。
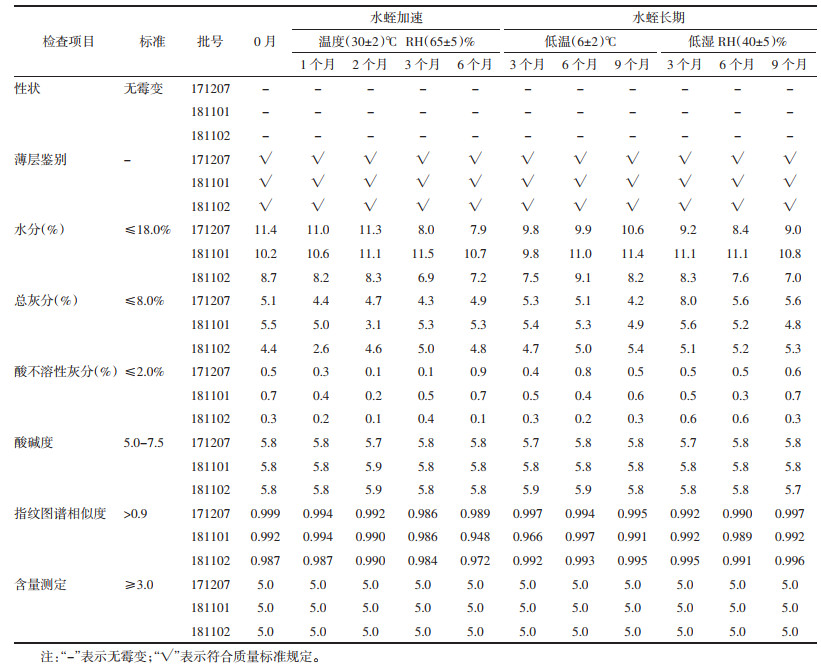
水蛭药材在(30±2)℃、相对湿度(65±5)%条件下进行加速实验,在低温条件(6±2)℃、低湿条件[(25±2)℃,相对湿度(40±5)%]下进行长期实验,实验结果如表 5。
结果显示,由于批间差异及质量变化,水蛭药材水分、总灰分、指纹图谱等稳定性实验结果数据存在波动情况。加速实验中,水蛭药材3批样品在温度(30±2)℃、(相对湿度65±5)%的条件下放置6个月,药材性状、薄层鉴别、水分、总灰分、酸不溶性灰分、指纹图谱以及含量均符合药材质量标准规定;长期实验中,在低温条件(6±2)℃和低湿条件(温度(25±2)℃,相对湿度(40±5)%)下进行长期实验,放置9个月,各项检验结果均符合水蛭药材质量标准规定。
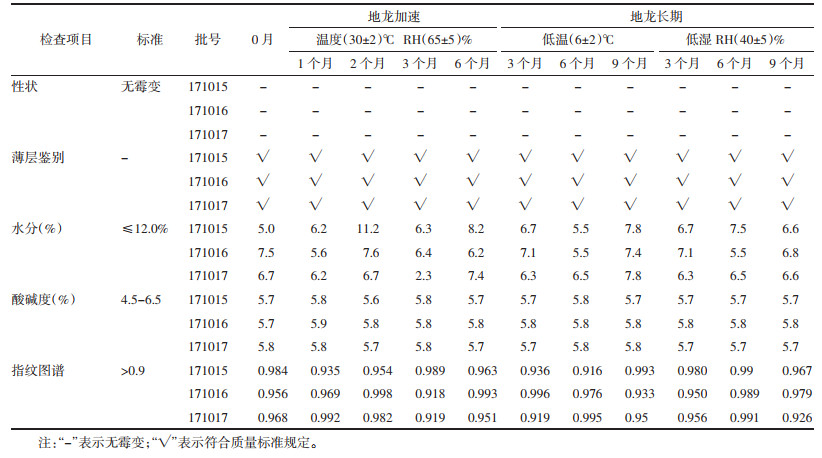
2.5 地龙加速及长期实验结果地龙药材在(30±2)℃、相对湿度(65±5)%条件下进行加速实验,在低温条件(6±2)℃、低湿条件[(25±2)℃,相对湿度(40±5)%]下进行长期实验,实验结果如表 6。
结果显示,由于批间差异及质量变化,地龙药材水分、总灰分、指纹图谱等稳定性实验结果数据存在波动情况。加速实验中,地龙药材在加速条件[温度(30±2)℃、相对湿度(65±5)%]下放置6个月,药材各项指标均符合质量标准规定;长期实验结果表明,在低温条件(温度(6±2)℃和低湿条件[温度(25±2)℃,相对湿度(40±5)%]下进行长期实验,放置9个月,各项检验结果均符合地龙药材质量标准规定。
3 讨论动物类中药材是中药材的重要组成部分。《中华人民共和国药典(2015版)》共收载102味动物类中药材,其中一部收载动物类中药材55味、提取物1种及含动物的药制剂458种,占全部品种的18%[3]。此外,《现代中药大辞典》收载740种动物类中药材,《中华本草》收载1051种动物类中药材[4]。
水蛭和地龙为《中国药典(2015版)》一部收载的品种。水蛭俗称蚂蟥,主要成分为水蛭素、组织胺等[5],有抗凝、抗血栓等作用[6];地龙是蚯蚓的干燥体,主要成分有蚯蚓素、地龙毒素,有抗凝血、降压等作用[7]。由于受到人工粗放式养殖,加工工艺落后及技术缺陷的限制,水蛭、地龙等动物类中药材质量存在诸多问题,因其对温湿度敏感,储存条件不佳会影响其临床疗效,故以之为例进行稳定性实验研究,可为动物类中药材选择适宜条件开展稳定性研究提供重要实验依据。
中国现行的稳定性实验指导原则为《中国药典(2015版)》第四部中《9001原料药物与制剂稳定性实验指导原则》,但是,现有稳定性研究实验条件与动物类中药材实际储存条件相差较大,同时,由于缺乏关于温湿度敏感的动物类中药材稳定性研究的指导原则、法规标准和相关数据,导致一些动物类中药材全生命周期的质量可控性差,严重影响其临床疗效及应用。因此,如何结合动物类中药材自身特点,选择适宜动物类中药材稳定性研究的条件,为该类药材的生产、包装、贮存、运输以及制定有效期提供科学依据,是深入研究动物类中药材的关键。
课题组前期进行了稳定性实验,考察了水蛭、地龙在药典规定的常规条件所下出现的质量波动和变化情况。影响因素实验中,在相对湿度90%的高湿条件下,水蛭、地龙霉变率达100%;加速实验条件,即在温度40 ℃±2 ℃、相对湿度(75±5)%的条件下放置6个月,水蛭、地龙药材从1个月开始出现霉变;此外,在温度30℃±2℃、相对湿度(65±5)%的条件下放置12个月,水蛭药材个别批次在3个月到9个月也会出现大量霉变。前期结果表明,高湿条件对水蛭地龙药材保存影响较大,常规实验条件不适宜开展水蛭、地龙的稳定性研究,应更改实验条件以保证药材质量。
根据前期结果,并参考指导原则中对温度特别敏感原料药物的(低温)实验条件以及包装在半透性容器中的药物制剂的(低湿)实验条件,对实验条件进行优化和改变,以期在更为温和的实验条件下,考察药材质量的稳定性。结果表明,在优化的实验条件下,水蛭、地龙未出现霉变及变质情况,且稳定性良好,质量可控,故可以此为基础,为动物类中药材选择适宜条件开展稳定性研究提供重要实验依据。
4 结论本文对水蛭、地龙药材开展稳定性研究。在实验条件下,水蛭地龙质量稳定可控。故可以采用在(30±2)℃,相对湿度(65±5)%的加速条件以及低温条件[(6±2)℃]、低湿条件[(25±2)℃,相对湿度(40±5)%]作为动物类中药材的稳定性研究条件。也可作为其他动物类中药材相关质量研究和稳定性研究的重要参考。
| [1] |
张静, 李晶峰, 杜延佳, 等. 近5年动物药药理研究新进展[J]. 吉林中医药, 2016, 36(11): 1136-1137, 1150. ZHANG J, LI Y F, DU Y J, et al. Recent advances in animal medicine pharmacology research in last five years[J]. Jilin Journal of Traditional Chinese Medicine, 2016, 36(11): 1136-1137, 1150. |
| [2] |
国家药典委员会.中华人民共和国药典[S].北京: 中国医药科技出版社, 2015. National Pharmacopoeia Commission. Pharmacopoeia of the People's Republicof China[S]. Beijing: China Medical Science and Technology Publishing House, 2015. |
| [3] |
罗亚虹, 张治军. 动物类中药材质量控制研究新进展[J]. 海峡药学, 2016, 28(8): 55-57. LUO Y H, ZHANG Z J. New progress in research on quality control of Animal Traditional Chinese Medicine[J]. Strait Pharmaceutical Journal, 2016, 28(8): 55-57. DOI:10.3969/j.issn.1006-3765.2016.08.019 |
| [4] |
陈衍会. 动物类中药的发展概况[J]. 中国民族民间医药, 2010, 19(17): 50-51. CHEN Y H. General situation of development of animal traditional Chinese medicine[J]. Chinese journal of ethnome-dicine and ethnophamacy, 2010, 19(17): 50-51. DOI:10.3969/j.issn.1007-8517.2010.17.034 |
| [5] |
刘璇, 高美风, 孔毅. 水蛭化学成分及药理作用的研究进展[J]. 药物生物技术, 2017, 24(0): 76-80. LIU X, GAO M F, KONG Y. Bioactive constituents and pharmacological effects of leech[J]. Pharmaceutical Biotechnology, 2017, 24(1): 76-80. |
| [6] |
刘贞丽, 潘继富, 董传海. 水蛭的药理作用及其临床应用[J]. 时珍国医国药, 2002(6): 376-378. LIU Z L, PAN J F, DONG C H. Pharmacological action and clinical application of leech[J]. Lishizhen Medicine and Materia MedicaResearch, 2002(6): 376-378. DOI:10.3969/j.issn.1008-0805.2002.06.047 |
| [7] |
唐鼎, 凃乾, 李娟, 等. 药用地龙的药理作用和临床研究进展[J]. 中国药师, 2015, 18(6): 1016-1019. TANG D, TU Q, LI J, et al. Progress in pharmacological effects and clinical research of Pheretima[J]. China Pharmacist, 2015, 18(6): 1016-1019. DOI:10.3969/j.issn.1008-049X.2015.06.044 |
 2020, Vol. 39
2020, Vol. 39