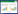文章信息
- 王小双, 魏文峰, 韩德强, 霍金海, 王伟明
- WANG Xiaoshuang, WEI Wenfeng, HAN Deqiang, HUO Jinhai, WANG Weiming
- 基于UPLC-Q-TOF/MS技术的橘皮竹茹汤血清药物化学初步研究
- Preliminary study on serum pharmacochemistry of Jupi Zhuru Decoction based on UPLC-Q-TOF/MS
- 天津中医药大学学报, 2022, 41(1): 108-117
- Journal of Tianjin University of Traditional Chinese Medicine, 2022, 41(1): 108-117
- http://dx.doi.org/10.11656/j.issn.1673-9043.2022.01.21
-
文章历史
收稿日期: 2021-09-25
橘皮竹茹汤源自张仲景的《金匮要略》,由橘皮、大枣、竹茹、人参、生姜、甘草组成。原文为: “哕逆者,橘皮竹茹汤主之。”后世医家以“胃虚有热,胃气上逆”“寒热相搏”“脾胃虚寒,胃失和降”等概括本方病因病机[1]。现代研究表明,橘皮竹茹汤已广泛应用于医治慢性胃炎、幽门水肿、幽门不全梗阻、消化性溃疡、消化功能不良引起的呕吐、反流性食管炎等疾病[2-4]。
超高效液相色谱-四级杆-飞行时间质谱联用(UPLC-Q-TOF/MS)技术是一种具有高分辨率、高灵敏度特点的质谱技术。目前大量研究报道了UPLC-Q-TOF/MS作为一种分析方法被应用于中药或中药复方的入血成分研究,且实验结果良好[5-6]。
中药成分复杂,想要确定中药入血后的有效成分并阐明其药效物质基础,通过现代化的分析手段对其给药后血清进行原型成分以及代谢产物分析是必不可少的。同时,尚未有橘皮竹茹汤入血成分研究的相关报道,所以本实验旨在采用UPLC-Q-TOF/MS技术推断或鉴定其入血成分。
1 材料与仪器 1.1 仪器实验用仪器具体情况见表 1。
对照品甘草酸(批号G-003-160330)、刺芒柄花素(批号C-018-160304)购于成都瑞芬思生物科技有限公司;柚皮苷(批号110722-201815)购自中国食品药品检定研究院。甲醇、乙腈(色谱纯,德国Merck公司);甲酸(色谱纯,美国Fisher公司);屈臣氏蒸馏水(广州屈臣氏食品饮料有限公司);甲醇(分析纯,天津市科密欧化学试剂有限公司);水合氯醛(批号20100827,天津市光复精细化工研究所);自制橘皮竹茹汤冻干粉(陈皮饮片购自湖北随州,批号17112111;竹茹饮片购自安徽岳西,批号1708311;大枣饮片购自河北安国,批号1709061;人参饮片购自吉林通化,批号180311;生姜饮片购自浙江磐安,批号ZJP2011165;甘草饮片购自甘肃陇西,批号17111411)。
1.3 实验动物健康雄性Wister大鼠,体质量(200±20) g,SPF级,由哈尔滨医科大学动物实验中心供给,许可证号: SYXK(黑)2016-008。大鼠于SPF级动物室饲养,室温20~25 ℃,湿度50%~70%。
2 实验方法 2.1 供试品溶液的制备取橘皮竹茹汤冻干粉1.0 g,精密称定,加甲醇25 mL,超声处理(功率300 W,频率40 KHz)30 min,放冷,补足甲醇,摇匀,滤过,取续滤液,13 000 r/min离心5 min(离心半径7 cm),取上清液,即得。
2.2 给药药液的制备取橘皮竹茹汤冻干粉,加适量蒸馏水超声溶解,制成0.108 g/mL药液供大鼠灌胃使用。
2.3 血清样本的制备Wister大鼠禁食12 h(自由饮水),给药组按照10.8 g/kg(相当于人体临床1 d剂量的10倍)灌胃橘皮竹茹汤冻干粉药液,空白组按照10.0 mL/kg灌胃蒸馏水。给药1 h后,腹腔注射5%水合氯醛麻醉,取腹主动脉血,离心(3 000 r/min,10 min,离心半径7 cm),取上清液,-80 ℃保存。
取大鼠空白血清及给药血清各400 μL,各加入10 μL磷酸,涡旋震荡(2 500 r/min),分别加入1.6 mL乙腈,涡旋震荡(2 500 r/min),离心(13 000 r/min,4 ℃,10 min,离心半径7 cm),取上清液,氮气流吹干,残渣用200 μL甲醇复溶,涡旋震荡(2 500 r/min,60 s),离心(13 000 r/min,4 ℃,10 min,离心半径7 cm),取上清液,供UPLC-Q-TOF/MS分析。
2.4 色谱条件Waters Acquity UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),ACQUITY UPLC BEH C18 VanGuard Pre-Column预柱(2.1 mm×5 mm,1.7 μm),柱温35 ℃,0.1%甲酸水为流动相A,0.1%甲酸乙腈为流动相B,梯度洗脱(0~3 min,0%~5%B;3~10 min,5%~50%B;10~18 min,50%~100%B;18~18.1 min,100%~5%B;18.1~20 min,5%B),流速0.3 mL/min,进样量5 μL。
2.5 质谱条件质谱条件设置见表 2。
将橘皮竹茹汤给药血清和空白血清导入Peakview软件,设置相关参数(Mass Errorr≤10;权重30%,Isotope≤10%;权重30%,Formula Finderscore>70%)扣除空白血清成分干扰,将检测到的其余离子与体外药材提取液所检测到化合物的保留时间、母离子精确质量数、同位素峰度比及二级质谱图进行比较,相同则确认为橘皮竹茹汤冻干粉中的原型成分[7]。
运用MetabolitePilot 2.0.4软件,导入前期推断或鉴定的橘皮竹茹汤化学成分的结构式和总离子流图,为每一个化学成分设置不同的Biotransformation parameters,选择所有可能的Ⅰ、Ⅱ相代谢途径,设置Generic ParametersPeak、Finding Strategy和Compound-Specific Parameters,给药血清的液质采集数据为sample,空白血清的液质采集数据为control进行分析[8-9],最后结合软件及相关文献给出代谢物的保留时间及二级碎片,推断可能的代谢物。
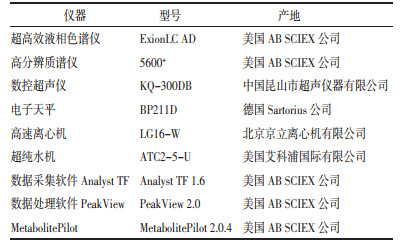
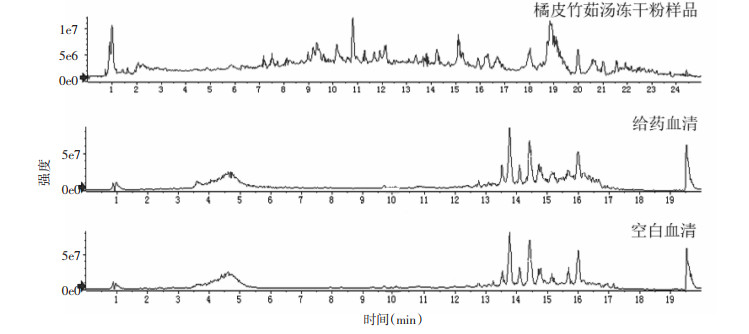
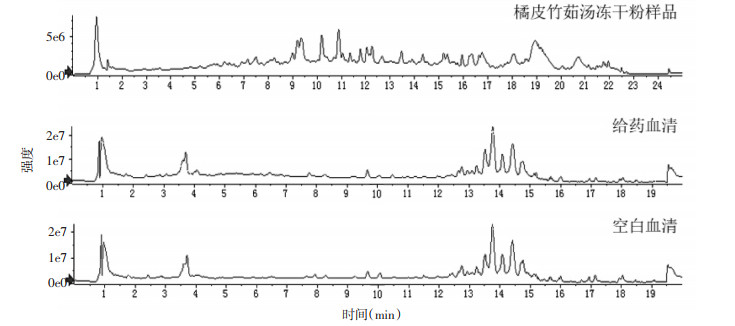
3 结果 3.1 橘皮竹茹汤UPLC-Q-TOF/MS色谱图的采集根据建立的橘皮竹茹汤血中移行成分分析方法,采用正、负离子模式采集橘皮竹茹汤冻干粉样品、给药血清和空白血清数据。正离子模式总离子流图见图 1,负离子模式总离子流图见图 2。
|
| 图 1 正离子模式下总离子流图 |
|
| 图 2 负离子模式下总离子流图 |
根据“2.6”项的分析方法,结合对照品比对及文献报道[10-15],鉴定出大鼠灌胃橘皮竹茹汤冻干粉后的血中移行成分41个,包括原型成分13个、代谢产物28个。见表 3。
本研究鉴定了原型成分13个,以化合物2和9说明推测过程。
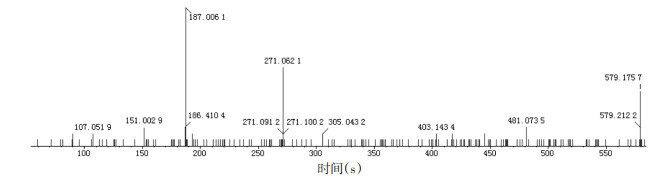
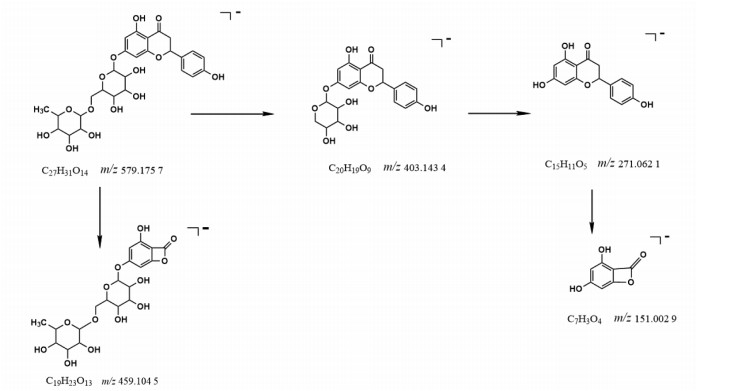
化合物2:负离子模式下,化合物2在含药血清总离子流图的柚皮苷保留时间与样品总离子流图一致,二级质谱碎片一致,准分子离子峰m/z 579.175 7相对丰度较强,拥有共同二级碎片m/z 403.143 4、271.062 1、151.002 9等。通过查询相关成分的文献[16],推断化合物2为柚皮苷。二级质谱图见图 3,其可能的裂解过程见图 4。
|
| 图 3 柚皮苷负离子模式下的质谱图 |
|
| 图 4 推测的柚皮苷裂解途径 |
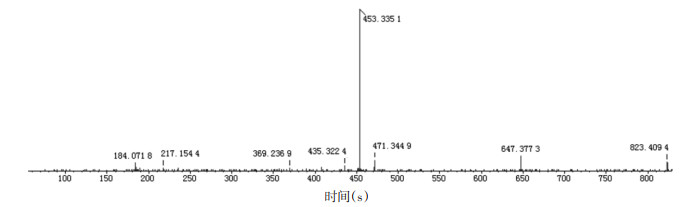
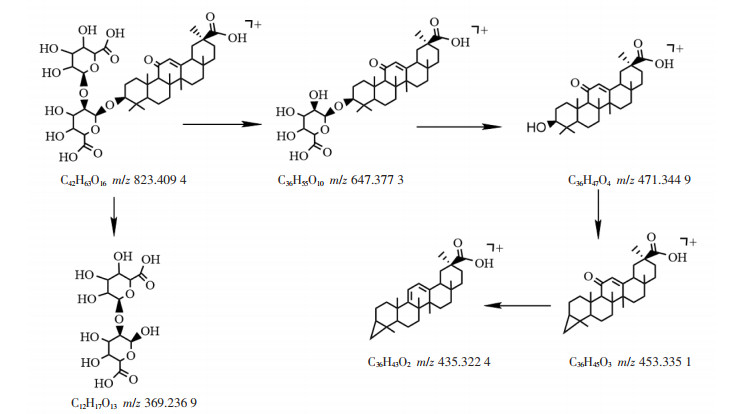
化合物9:正离子模式下,化合物9在含药血清总离子流图与样品总离子流图甘草酸的保留时间一致,二级质谱碎片一致,准分子离子峰m/z 823.409 4相对丰度较强,拥有共同二级碎片m/z 647.377 3、471.344 9、369.236 9等。通过查询相关成分的文献[17],推断化合物9为甘草酸。二级质谱图见图 5,其可能的裂解过程见图 6。
|
| 图 5 甘草酸正离子模式下的质谱图 |
|
| 图 6 推测的甘草酸裂解途径 |
本研究推测了28个代谢产物,以化合物20和化合物37为例说明鉴定过程。
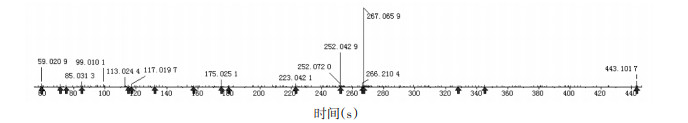
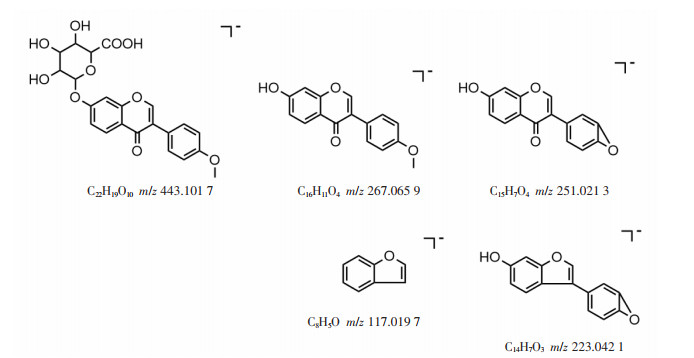
化合物20:刺芒柄花素是来自甘草的黄酮类成分,易发生Ⅱ相代谢反应。通过MetabolitePilot代谢软件分析发现,化合物20为刺芒柄花素A环7位发生葡萄糖醛酸化的产物。该产物在负离子模式下,准分子离子峰m/z 443.101 7[M-H]-,比刺芒柄花素准分子离子峰m/z 267.065 9[M-H]-多176.035 8,符合1分子葡萄糖醛酸的分子量。结合其特征碎片m/z 267.065 9、252.042 9、223.042 1等,与刺芒柄花素的二级碎片相一致,符合其葡萄糖醛酸化的过程。结合文献报道[18],芒柄花素-7-O-β-D-葡萄糖经Ⅰ相代谢水解反应后,转化为芒柄花素,易发生葡萄糖醛酸化反应。二级质谱图见图 7,其可能的裂解过程见图 8。
|
| 图 7 刺芒柄花素葡萄糖醛酸化产物负离子模式下的质谱图 |
|
| 图 8 推测的刺芒柄花素葡萄糖醛酸化产物裂解途径 |
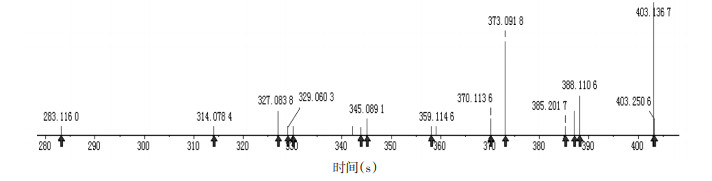
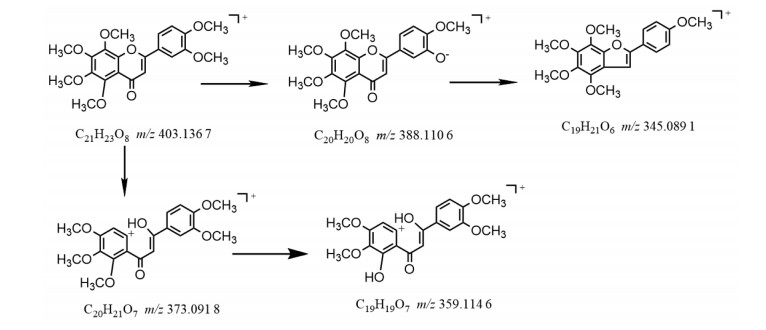
化合物37:柚皮黄素是陈皮中的黄酮类成分,易发生Ⅰ相代谢反应。通过MetabolitePilot代谢软件分析发现,化合物37为柚皮黄素C环3位脱羟基产物。在正离子模式下,准分子离子峰为m/z 403.136 7[M+H]+比柚皮黄素准分子离子峰m/z 419.148 2[M+H]+少16,提示失去1个氧原子,发生脱羟基。结合二级质谱碎片离子m/z 388.110 6、373.091 8、345.089 1等,与柚皮黄素的二级质谱碎片相比较,符合脱羟基过程。其准分子离子峰m/z 401.367 3丢失甲基产生m/z 388.110 6碎片离子,继续丢失C环上的1分子一氧化碳和1个氧原子产生m/z 345.089 1碎片离子。另一条裂解途径为A环甲氧基丢失,同时导致C环C-O键断裂产生m/z 373.091 8碎片离子,m/z 373.091 8碎片离子丢失亚甲基产生m/z 359.114 6碎片离子。根据文献报道[19],该柚皮黄素脱羟基产物与川陈皮素的裂解规律一致,所以推测柚皮黄素脱羟基产物为川陈皮素。二级质谱图见图 9,其可能的裂解过程见图 10。
|
| 图 9 柚皮黄素脱羟基产物正离子模式下的质谱图 |
|
| 图 10 推测的柚皮黄素脱羟基产物裂解途径 |
本实验考察了不同给药剂量(1、5和10倍),结果显示,10倍给药剂量的响应值最高,色谱峰最多,故10倍是最佳给药剂量。考察了4种血清处理方法(乙腈沉淀法、甲醇沉淀法、固相萃取-乙腈洗脱和固相萃取-甲醇洗脱),结果显示,乙腈沉淀法是血中移行成分最多的一种方法,故乙腈沉淀法是血清最佳处理方法。考察了8个不同采血时间节点(0、0.5、1、2、4、8、12、24 h),结果显示,给药1 h检测到的峰数目最多,故最佳采血时间节点为给药后1 h。
本实验对大鼠进行灌胃给予橘皮竹茹汤冻干粉的含药血清,推断了41个血中移行成分,其中原型成分13个、代谢产物28个,来自陈皮的主要是黄酮类成分,包括橙皮苷、柚皮黄素等,能够清除羟自由基、保护膜损伤、抑制幽门螺杆菌增殖、抗炎及增强幽门泵活动促进胃排空[20]。来自甘草的主要是黄酮类和三萜类成分,甘草中的甘草次酸能够抑制幽门螺杆菌感染后的胃黏膜上皮细胞凋亡,发挥抗炎作用[21]。来自生姜的主要是姜辣素类成分,包括6-姜酚、6-姜烯酚等,能够抑制胃黏膜上5-羟色胺3(5-HT3)和5-羟色胺4(5-HT4)受体发挥止吐作用[22]。结合各味药物的传统药效及药理作用,初步推测本实验得到的41个入血成分可能是其发挥药效的物质基础。
| [1] |
张波, 姜良铎, 张冬梅, 等. 《金匮要略》橘皮竹茹汤方证探微[J]. 天津中医药, 2010, 27(1): 34-36. ZHANG B, JIANG L D, ZHANG D M, et al. Research on prescription and syndrome of Jupi Zhuru Decoction in medical treasures of Golden Chamber[J]. Tianjin Journal of Traditional Chinese Medicine, 2010, 27(1): 34-36. |
| [2] |
张宵庆, 冯正权. 橘皮竹茹汤佐治化疗相关性呕吐30例[J]. 浙江中医杂志, 2019, 54(3): 210. ZHANG X Q, FENG Z Q. Jupi Zhuru Decoction for adjuvant treatment of 30 cases of chemotherapy-related vomiting[J]. Zhejiang Journal of Traditional Chinese Medicine, 2019, 54(3): 210. DOI:10.3969/j.issn.0411-8421.2019.03.041 |
| [3] |
马丽娟. 橘皮竹茹汤治疗胃轻瘫的理论探讨[J]. 中国中医药现代远程教育, 2017, 15(18): 57-59. MA L J. Study on the theory of Jupi Zhuru Decoction in the treatment of gastroparesis[J]. Chinese Medicine Modern Distance Education of China, 2017, 15(18): 57-59. DOI:10.3969/j.issn.1672-2779.2017.18.026 |
| [4] |
王长来. 济生橘皮竹茹汤为主治疗胃食管反流性呼吸并发症48例[J]. 山东中医杂志, 2009, 28(1): 26-27. WANG C L. Jisheng Jupi Zhuru Decoction for treating 48 cases of gastroesophageal reflux respiratory complications[J]. Shandong Journal of Traditional Chinese Medicine, 2009, 28(1): 26-27. |
| [5] |
胡晒平, 严建业, 伍红年, 等. 基于UPLC-Q-TOF-MS的西洋参提取物及入血成分分析[J]. 中南药学, 2019, 17(6): 825-830. HU S P, YAN J Y, WU H N, et al. Identification of chemical constituents and absorbed components of American ginseng by UPLC-Q-TOF-MS[J]. Central South Pharmacy, 2019, 17(6): 825-830. |
| [6] |
张珂, 许霞, 李婷, 等. 利用UHPLC-IT-TOF-MS分析陈皮的化学成分组[J]. 中国中药杂志, 2020, 45(4): 899-909. ZHANG K, XU X, LI T, et al. Chemome profiling of citri reticulatae pericarpium using UHPLC-IT-TOF-MS[J]. China Journal of Chinese Materia Medica, 2020, 45(4): 899-909. |
| [7] |
魏文峰, 陈宏昌, 刘烨, 等. 基于UPLC-Q-TOF-MS技术的刺五加叶血清药物化学初步研究[J]. 中草药, 2017, 48(7): 1306-1313. WEI W F, CHEN H C, LIU Y, et al. Preliminary study on serum pharmacochemistry of leaves of Acanthopanax senticosus base on UPLC-Q-TOF-MS[J]. Chinese Traditional and Herbal Drugs, 2017, 48(7): 1306-1313. |
| [8] |
王改丽, 程团, 霍金海, 等. 基于UPLC-Q-TOF/MS技术的北青龙衣大鼠肾组织化学成分分析[J]. 中草药, 2018, 49(16): 3763-3769. WANG G L, CHENG T, HUO J H, et al. Analysis on chemical constituents from rat kidney tissue of Juglans mandshurica based on UPLC-Q-TOF/MS[J]. Chinese Traditional and Herbal Drugs, 2018, 49(16): 3763-3769. DOI:10.7501/j.issn.0253-2670.2018.16.006 |
| [9] |
王改丽, 程团, 霍金海, 等. 北青龙衣醇提物在大鼠肝组织中的成分分布研究[J]. 中南药学, 2018, 16(4): 451-458. WANG G L, CHENG T, HUO J H, et al. Components distribution of Juglans mandshurica alcohol extract in rat liver tissue[J]. Central South Pharmacy, 2018, 16(4): 451-458. |
| [10] |
孙国东, 霍金海, 王改丽, 等. 基于UPLC-Q-TOF/MS技术的核桃楸皮成分分析[J]. 中草药, 2017, 48(4): 657-667. SUN G D, HUO J H, WANG G L, et al. Identification and characterization of chemical constituents in Cortex Juglandis Mandshuricae based on UPLC-Q-TOF/MS[J]. Chinese Traditional and Herbal Drugs, 2017, 48(4): 657-667. |
| [11] |
霍金海, 都晓伟, 孙国东, 等. 基于UPLC-Q-TOF/MS分析北青龙衣成分[J]. 中草药, 2016, 47(19): 3379-3388. HUO J H, DU X W, SUN G D, et al. Analysis on major chemical compounds in exocarp of Juglans mandshurica based on UPLC-Q-TOF/MS[J]. Chinese Traditional and Herbal Drugs, 2016, 47(19): 3379-3388. DOI:10.7501/j.issn.0253-2670.2016.19.006 |
| [12] |
魏文峰, 霍金海, 遆铁军, 等. 牛黄清感胶囊血中移行成分经时变化规律研究[J]. 中国中医药科技, 2018, 25(5): 677-680. WEI W F, HUO J H, TI T J, et al. Study on the time-dependent changes of blood migration components in Niuhuang Qinggan Capsule[J]. Chinese Journal of Traditional Medical Science and Technology, 2018, 25(5): 677-680. |
| [13] |
刘烨, 魏文峰, 霍金海, 等. 基于UPLC-Q-TOF-MS技术的芩百清肺浓缩丸血清药物化学初步研究[J]. 中国中药杂志, 2017, 42(3): 572-579. LIU Y, WEI W F, HUO J H, et al. Serum pharmacochemistry of Qinbai Qingfei concentrated pellets based on UPLC-Q-TOF-MS[J]. China Journal of Chinese Materia Medica, 2017, 42(3): 572-579. |
| [14] |
代吉瑞, 魏文峰, 霍金海, 等. 不同采收时期刺五加叶化学成分动态分析[J]. 中南药学, 2019, 17(4): 495-500. DAI J R, WEI W F, HUO J H, et al. Dynamic analysis of chemical constituents of leaves of Acanthopanax senticosus at different harvest time[J]. Central South Pharmacy, 2019, 17(4): 495-500. |
| [15] |
孙国东, 霍金海, 洪晓琴, 等. 基于UPLC-Q-TOF/MS技术的北青龙衣不同干燥方法对萘醌类成分影响研究[J]. 中药材, 2016, 39(11): 2501-2508. SUN G D, HUO J H, HONG X Q, et al. Influence of drying method on naphthoquinone components in Juglans mandshurica based on UPLC-Q-TOF/MS[J]. Journal of Chinese Medicinal Materials, 2016, 39(11): 2501-2508. |
| [16] |
赵艳敏, 刘素香, 张晨曦, 等. 基于HPLC-Q-TOF-MS技术的甘草化学成分分析[J]. 中草药, 2016, 47(12): 2061-2068. ZHAO Y M, LIU S X, ZHANG C X, et al. Analysis on chemical constituents from Glycyrrhizae Radix et Rhizoma by HPLC-Q-TOF-MS[J]. Chinese Traditional and Herbal Drugs, 2016, 47(12): 2061-2068. DOI:10.7501/j.issn.0253-2670.2016.12.007 |
| [17] |
史培颖. 中药四类成分质谱裂解规律及芪参益气方药代动力学研究[D]. 杭州: 浙江大学, 2010. SHI P Y. Studies on mass spectrometric fragmentation patterns of four categories of compounds in TCMs and pharmacokinetics of Qishen Yiqi Formula[D]. Hangzhou: Zhejiang University, 2010. |
| [18] |
郑单单, 魏文峰, 霍金海, 等. 基于UPLC-Q-TOF-MS技术的芪风固表颗粒血清药物化学研究[J]. 中草药, 2021, 52(3): 643-652. ZHENG D D, WEI W F, HUO J H, et al. Study on serum pharmacochemistry of Qifeng Gubiao Granules based on U-PLC-Q-TOF-MS[J]. Chinese Traditional and Herbal Drugs, 2021, 52(3): 643-652. |
| [19] |
叶晓岚. 广陈皮体外指纹谱及体内代谢谱研究[D]. 广州: 广东药学院, 2013. YE X L. The study on chemical fingerprint and metabolic profile of Citrus reticulate Chachi[D]. Guangzhou: Guangdong Pharmaceutical University, 2013. |
| [20] |
魏大军. 橙皮苷抗呼吸道炎症作用效果的实验研究[D]. 长春: 吉林大学, 2011. WEI D J. Experimental research on the effect of the effect of anti-airway inflammation by hesperidin[D]. Changchun: Jilin University, 2011. |
| [21] |
韩瑶聃, 王彬, 王政雨, 等. 甘草酸药理作用的研究进展[J]. 中国新药杂志, 2012, 21(21): 2499-2505. HAN Y D, WANG B, WANG Z Y, et al. Recent research progress in pharmacological effects of glycyrrhizic acid[J]. Chinese Journal of New Drugs, 2012, 21(21): 2499-2505. |
| [22] |
侯以森, 刘雅范, 张晓雨, 等. 6-姜烯酚药理作用的研究进展[J]. 吉林医药学院学报, 2020, 41(2): 132-135. HOU Y S, LIU Y F, ZHANG X Y, et al. Advances in pharmacological effects of 6-shogaol[J]. Journal of Jilin Medical University, 2020, 41(2): 132-135. |
 2022, Vol. 41
2022, Vol. 41