文章信息
- 薛子祥, 王颂瑞, 杨冬月, 赵露露, 欧阳慧子, 常艳旭, 何俊
- XUE Zixiang, WANG Songrui, YANG Dongyue, ZHAO Lulu, OUYANG Huizi, CHANG Yanxu, HE Jun
- 细辛水提物HPLC指纹图谱及化学模式识别的研究
- Study on HPLC fingerprint and chemical pattern recognition of Asarum water extract
- 天津中医药大学学报, 2022, 41(2): 243-249
- Journal of Tianjin University of Traditional Chinese Medicine, 2022, 41(2): 243-249
- http://dx.doi.org/10.11656/j.issn.1673-9043.2022.02.24
-
文章历史
收稿日期: 2021-11-20
2. 天津中医药大学第一附属医院, 天津 300193
2. First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300193, China
细辛为马兜铃科植物北细辛Asarum heterotropoides Fr. Schmidt var. mands huricum(Maxim.)Kitag.、汉城细辛Asarum sieboldii Miq. var. seoulense Nakai或华细辛Asarum sieboldii Miq.的干燥根和根茎。前两种习称“辽细辛”[1]。细辛气辛香、味温,入肺、肾、心经。细辛在中医药学上具有祛风散寒、止痛、通窍、温肺化饮等功效,临床上常用于治疗风寒头痛、鼻塞、牙痛、痰饮咳喘、关节痛等疾病[2]。近些年来对细辛的挥发性成分研究较多[3],但对于细辛水提物的研究相对较少[4]。Huang等[5]指出具有特异性的“马兜铃酸突变指纹”会被含有马兜铃酸的中药诱导从而诱发肝癌。细辛为马兜铃科植物,其非挥发性成分中含有马兜铃酸[6-7]。同时,中药材在临床上主要采用水煎煮的提取方法,在古代临床上早有“细辛不过钱”的说法[8]。从中药材细辛临床安全用药的角度考虑,需要建立一种高效、快速的分析检测方法完善对细辛药材水提物的质量评价。
1 材料 1.1 仪器Agilent 1100型高效液相色谱仪(Agilent,USA);Milli-Q IQ 7005超纯水制备仪(Millipore公司);5424R型高速离心机(德国Eppendorf公司);AS 60/220.R2型十万分之一天平(波兰RADWAG公司);G3KT18273型旋涡混合器(赛默飞世尔科技公司)。
1.2 试药对照品细辛脂素(批号:DST180425-014)、马兜铃酸A(批号:DST180413-021)、芝麻脂素(批号:MUST-1706301)、卡枯醇(批号:DST190325-028)、去甲乌药碱(批号:DST190402-154)、槲皮素(批号:DST180521-028)购于成都德思特生物科技有限公司;甲醇为色谱纯,购于美国Fisher公司;甲酸为色谱纯,购于美国ROE公司;超纯水由Milli-Q超纯水仪制备。
1.3 样品来源10批细辛药材分别来源于辽宁盘锦,辽宁丹东,辽宁本溪,辽宁沈阳,吉林白山,山西长治,云南本溪,辽宁锦州,吉林靖宇,辽宁新宾。经何俊研究员鉴定分别为马兜铃科植物北细辛、汉城细辛以及华细辛表 1为不同批次细辛的来源。
色谱柱:ZORBAX Eclipse Plus C18柱(4.6 mm×250 mm,5 μm);流动相:A相为0.1%甲酸水,B相为甲醇。梯度洗脱,洗脱梯度为:0~3 min,3% B;3~15 min,3%~50% B;15~20 min,50%~80% B。流速为1 mL/min,柱温:30 ℃,进样量:10 μL,检测波长285 nm。
2.2 对照品溶液的配制精密称定细辛脂素,马兜铃酸A,芝麻素,卡枯醇,去甲乌药碱,槲皮素5.00 mg,加入5 mL甲醇进行溶解,得到浓度为1 mg/mL的各对照品储备液,并置于4 ℃冰箱冷藏备用。
2.3 供试品溶液的配制分别称定10个不同批次的细辛5 g,加入纯水定容至50 mL,加热回流1 h,减压干燥得浸膏约0.45 g。精密称定浸膏5 mg,加水1 mL溶解,涡流振荡,14 000 r/min离心10 min,用0.22 μm的微孔滤膜过滤,得上清液,置于4 ℃冰箱冷藏备用。
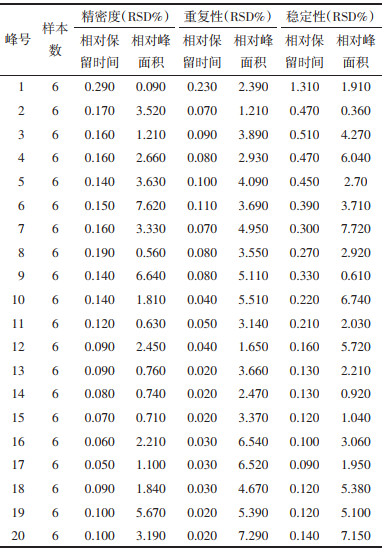
2.4 方法学考察 2.4.1 精密度实验取同一批细辛供试品溶液(S1),按“2.1”项色谱条件连续进样6次,测得各个共有色谱峰的峰面积和相对保留时间,计算RSD,结果见表 2,结果表明此方法的精密度良好。
精密称定细辛药材水提物(S1)6份,每份5 g,按照“2.3”项制备供试品溶液,按“2.1”项色谱条件进样,测得各共有色谱峰的峰面积和相对保留时间,计算RSD,结果见表 2,结果表明此方法的重复性良好。
2.4.3 稳定性实验取同一批细辛供试品溶液(S1),分别在时间点0、2、4、8、12、24 h下按“2.1”项色谱条件进样,测得各个共有色谱峰的峰面积和相对保留时间,计算RSD,结果见表 2,结果表明样品放置于室温24 h条件下稳定。
3 结果与分析 3.1 细辛HPLC指纹图谱建立和相似度分析采用中药色谱指纹图谱相似度评价软件(130723版,国家药典委员会,2012),对10批细辛药材水提物的实验结果和数据进行分析,采用多点校正法建立细辛药材水提物的指纹图谱,指纹图谱结果见图 1,共标定出20个共有峰,其中有6个特征峰,依次为6号峰(去甲乌药碱),16号峰(槲皮素),17号峰(卡枯醇),18号峰(马兜铃酸A),19号峰(芝麻素),20号峰(细辛脂素)。混合对照品图谱见图 2,10批细辛药材水提物的相似度分析结果见表 3。10批样品的相似度结果均在0.908以上,初步说明3种基源的细辛药材水提物质量相对均一稳定,推测这可能是北细辛、汉城细辛、华细辛3种基源的细辛均被药典收录的原因。

|
| 图 1 10批细辛药材水提物的叠加特征图谱 |

|
| 注:6.去甲乌药碱;16.槲皮素;17.卡枯醇;18.马兜铃酸A;19.芝麻素;20.细辛脂素。 图 2 混合对照品色谱图 |
为了对指纹图谱的结果进行补充,本研究以10批细辛指纹图谱中20个共有峰的相对峰面积为变量,导入SPSS 25.0软件,采用组间联接法,以欧氏距离为测度进行聚类分析[9]。聚类分析结果见图 3。结果表明,当距离刻度为15时,10批细辛药材水提物主要分为3类R1、R2、R3。R1中S6、S7、S8、S9均为北细辛,4批药材分别来源于山西长治、云南玉溪、辽宁锦州、吉林靖宇,4批药材的基源相同来源不同被分为了一类;R2中S4和S5均为北细辛,分别来源于辽宁沈阳和吉林白山;S1为华细辛,来源于辽宁盘锦;S10为汉城细辛,来源于辽宁新宾,4批药材中S4和S5与S1、S10的基源不同均来源于东北三省;R3中S2为北细辛,来源于辽宁丹东;S3为汉城细辛,来源于辽宁本溪。2批药材的基源不同均来源于辽宁省。10批细辛药材水提物的聚类结果表明不同产地及基源的细辛药材水提物间存在一定的质量差异。此外,聚类结果并不是按照药材的基源或者是药材的产地某单一变量作为划分,该结果为今后细辛药材水提物的质量研究提供参考。

|
| 图 3 10批细辛药材水提物聚类分析图 |
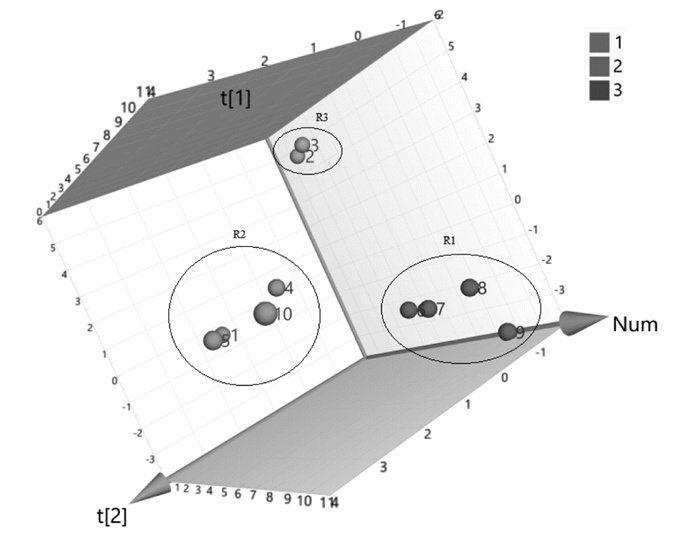
为了印证HCA的结果,本研究以指纹图谱中20个共有峰的峰面积为变量,构建20×10的原始数据矩阵,使用SIMCA14.1统计软件对10批细辛药材水提物进行无监督模式的PLS-DA,Par作为标度化方式,绘制出PLS-DA 3D分析图,见图 4。由图 4可知R1、R2、R3分别聚集在不同的区域,其分类结果与HCA结果一致,印证了HCA的结果。说明不同产地及基源的细辛药材水提物间存在一定的质量差异。
|
| 图 4 10批细辛药材水提物PLS-DA 3D图 |
为了进一步印证PLS-DA的结果,本研究以指纹图谱中20个共有峰的峰面积为变量,构建20×10的原始数据矩阵,使用SIMCA14.1统计软件对10批细辛药材水提物进行具有监督模式的OPLS-DA,见图 5。由模型分析验证参数可知,结实率参数R2X为0.807,区分参数R2Y为0.919,预测参数Q2为0.885,以上数据均大于0.5且原始数据矩阵中没有异常值,表明该模型稳定并且具有较好的预测准确性[10-13]。由图 5可知R1、R2、R3分别聚集在不同的区域,其分类结果与PLS-DA的结果一致,印证了PLS-DA的结果。进一步说明了不同产地及基源的细辛药材水提物间存在一定的质量差异。

|
| 图 5 10批细辛药材水提物的OPLS-DA散点图 |
为进一步评价不同基源和产地的细辛药材水提物的质量,本研究以10批细辛指纹图谱中20个共有峰的相对峰面积为变量,导入SPSS 25.0软件对10批细辛药材水提物进行PCA。结果将20个变量降维成5个主要成分,其方差累积贡献率为95.417%,综合了10批细辛药材水提物20个共有峰的大部分信息,相关矩阵的特征系数及方差贡献率见表 4。主成分综合得分和排序见表 5。结果对HCA、PLS-DA以及OPLS-DA的结果进行了补充。PCA结果表明10批细辛药材水提物中,S4得分最高,可初步认为来源于本溪的汉城细辛在10批细辛药材水提物中的质量相对较好,该结果为今后细辛药材水提物的质量研究提供参考。
得到的5个主成分的得分计算公式和综合得分计算公式如下

|
实验分别考察了甲醇-水、甲醇-0.1%甲酸水、乙腈-水、乙腈-0.1%甲酸水流动相体系对色谱峰的影响,发现甲醇-0.1%甲酸水为流动相时,色谱峰峰形及分离效果较好。故选择甲醇-0.1%甲酸水作为流动相体系;对样品溶液进行254 nm,285 nm,320 nm检测波长进行考察,结果发现当检测波长为285 nm时基线相对平稳,所有色谱峰响应相对较大,故选择285 nm作为检测波长。
中药指纹图谱技术是一种能够用于鉴别中药真伪、区分基源、评价优劣以及保证其稳定性和一致性的高效快速的分析检测方法[14]。但由于中药本身化学成分复杂,再加上产地不同、基源不同等影响因素,仅使用相似度评价系统并不能全面的、多层次的对中药材进行质量评价,需要结合其他分析方法对结果进行分析[15-16]。
化学模式识别是使用统计学或数学方法将化学体系的测量值与体系的整体建立联系,广泛应用于中药材的鉴定、表征、质量评价及质量控制等研究中[17]。化学模式识别分为无监督的模式识别和有监督的模式识别,在使用化学模式识别分析数据时,单独使用一种模式识别往往缺少科学性和代表性,因此常将两种模式结合起来相互验证、相互补充[18]。本实验采HPLC法建立细辛药材水提物的指纹图谱,并将HCA、PLS-DA、OPLS-DA和PCA联合使用,对所得指纹图谱进行综合分析,将多种分析方法联合使用使得分析结果较大程度地避免了人为因素所带来的误差[19]。几种分析结果相互验证相互补充,使得分析结果更加可靠[20]。本实验初步评价了不同基源和产地的细辛药材水提物的质量。这些结果较好地阐明了细辛水提物内在的质量特征,并进一步完善了对于细辛药材的质量评价。
| [1] |
国家药典委员会. 中华人民共和国药典(2015年版)[S]. 北京: 中国医药科技出版社, 2015: 135-136. National Pharmacopoeia Commission. Pharmacopoeia of the people' s republic of China (2015 edition)[S]. Beijing: China Medical Science and Technology Press, 2015: 135-136. |
| [2] |
朱跃兰, 侯秀娟, 赵凤毛. 细辛应用安全性的研究进展[J]. 中华中医药学刊, 2010, 28(6): 1175-1177. ZHU Y L, HOU X J, ZHAO F M. Research progress of Asarum application security use[J]. Chinese Archives of Traditional Chinese Medicine, 2010, 28(6): 1175-1177. |
| [3] |
段鹤君, 付朝晖. 细辛挥发油化学成分研究[J]. 中药材, 2010, 33(4): 562-565. DUAN H J, FU C H. Study on chemical constituents of volatile oil from Asarum[J]. Journal of Chinese Medicinal Materials, 2010, 33(4): 562-565. |
| [4] |
胡志祥, 彭崇胜, 刘忠. 华细辛根中非挥发性成分研究[C]. 中国化学会第八届天然有机化学学术研讨会论文集. 济南, 2010: 130. HU Z X, PENG C S, LIU Z. Study on non-volatile con- stituents from root of Asarum sinensis[A]. Proceedings of the 8th National Symposium on Natural Organic Chemistry, 2010: 130. |
| [5] |
NG A W T, POON S L, HUANG M N, et al. Aristolochic acids and their derivatives are widely implicated in liver cancers in Taiwan and throughout Asia[J]. Science Transla- tional Medicine, 2017, 9(412): eaan6446. DOI:10.1126/scitranslmed.aan6446 |
| [6] |
董玉启, 于华, 王春华, 等. 北细辛根化学成分研究[J]. 天津中医药, 2017, 34(12): 845-848. DONG Y Q, YU H, WANG C H, et al. Chemical con- stituents from the roots of Asarum heterotroprides var. mandshuricum[J]. Tianjin Journal of Traditional Chinese Medicine, 2017, 34(12): 845-848. DOI:10.11656/j.issn.1672-1519.2017.12.15 |
| [7] |
张翠英, 俞捷, 刘广学, 等. 3种马兜铃酸和2种马兜铃内酰胺在北细辛、华细辛及汉城细辛不同部位的分布及含量分析[J]. 世界科学技术-中医药现代化, 2019, 21(7): 1295-1305. ZHANG C Y, YU J, LIU G X, et al. Distribution and content of 3 aristolochic acids and 2 aristololactams in different parts of Asarum heterotropoides var. mandshuricum, A. sieboldii and A. sieboldii var. seoulense[J]. Modernization of Traditional Chinese Medicine and Materia Medica-World Science and Technology, 2019, 21(7): 1295-1305. |
| [8] |
王莉, 吴波, 王绍印. 正确认识"细辛不过钱"[J]. 天津中医药大学学报, 2018, 37(5): 366-368. WANG L, WU B, WANG S Y. Correct understanding of "Asarum' s dose can not exceed one Qian"[J]. Journal of Tianjin University of Traditional Chinese Medicine, 2018, 37(5): 366-368. |
| [9] |
康建, 周霖, 孙志, 等. 基于UPLC指纹图谱结合化学模式识别的冠心丹参胶囊质量控制研究[J]. 中草药, 2018, 49(17): 4051-4057. KANG J, ZHOU L, SUN Z, et al. Quality control research of Guanxin Danshen Capsule based on UPLC fingerprint combined with chemical pattern recognition[J]. Chinese Traditional and Herbal Drugs, 2018, 49(17): 4051-4057. DOI:10.7501/j.issn.0253-2670.2018.17.013 |
| [10] |
潘宏春, 阳勇, 秦伟瀚, 等. 基于多元统计学方法的亚香棒虫草与冬虫夏草化学差异研究[J]. 中草药, 2020, 51(16): 4316-4324. PAN H C, YANG Y, QIN W H, et al. Analysis of chemical differences between Cordyceps hawkesii and Cordyceps sinensis based on multivariate statistics[J]. Chinese Tradi- tional and Herbal Drugs, 2020, 51(16): 4316-4324. DOI:10.7501/j.issn.0253-2670.2020.16.028 |
| [11] |
林秀敏, 岳丽丹, 张振凌, 等. GC-IMS法比较不同方法炮制酒当归特异气味成分差异[J]. 中草药, 2020, 51(17): 4464-4472. LIN X M, YUE L D, ZHANG Z L, et al. Using GC-IMS to compare difference of specific odor components of Angeli-cae Sinensis Radix by different yellow wine processing methods[J]. Chinese Traditional and Herbal Drugs, 2020, 51(17): 4464-4472. DOI:10.7501/j.issn.0253-2670.2020.17.014 |
| [12] |
易博, 张旻, 胡引明, 等. 基于UPLC-Q-TOF-MS/MS技术的裸花紫珠不同部位化学成分分析[J]. 中国中药杂志, 2019, 44(21): 4661-4669. YI B, ZHANG M, HU Y M, et al. Analysis of constituents from different parts of Callicarpa nudiflora by UPLC-Q-TOF-MS/MS[J]. China Journal of Chinese Materia Medica, 2019, 44(21): 4661-4669. |
| [13] |
王璐, 刘然, 邢爽, 等. 草乌与生半夏、法半夏配伍UPLC/ Q-TOF-MS离子流图, OPLS-DA/PCS及差异化合物对比研究[J]. 四川中医, 2020, 38(1): 58-62. WANG L, LIU R, XING S, et al. Comparative study on UPLC/ Q-TOF-MS ion flow diagram, OPLS-DA/PCS and differential compounds between Radix polygoni and Rhizoma pinelliae and Pinellia ternata and Pinellia ternate[J]. Journal of Sichuan of Traditional Chinese Medicine, 2020, 38(1): 58-62. |
| [14] |
刘东方, 赵丽娜, 李银峰, 等. 中药指纹图谱技术的研究进展及应用[J]. 中草药, 2016, 47(22): 4085-4094. LIU D F, ZHAO L N, LI Y F, et al. Research progress and application in fingerprint technology on Chinese materia medica[J]. Chinese Traditional and Herbal Drugs, 2016, 47(22): 4085-4094. |
| [15] |
刘万仓, 孙磊, 于孟琦, 等. 中药指纹图谱模式识别研究进展[J]. 国际药学研究杂志, 2010, 37(6): 446-450. LIU W C, SUN L, YU M Q, et al. Advances in the pattern recognition research on fingerprint of Traditional Chinese Medicine[J]. Journal of International Pharmaceutical Re- search, 2010, 37(6): 446-450. |
| [16] |
褚延斌, 苏小琴, 周学谦, 等. 基于液质指纹图谱和化学模式识别的注射用益气复脉(冻干)质量综合评价研究[J]. 中草药, 2018, 49(10): 2410-2419. CHU Y B, SU X Q, ZHOU X Q, et al. Comprehensive evalu- ation of Yiqi Fumai Injection quality by UPLC-Q-TOF-MSE fingerprint and chemical pattern recognition[J]. Chinese Traditional and Herbal Drugs, 2018, 49(10): 2410-2419. DOI:10.7501/j.issn.0253-2670.2018.10.024 |
| [17] |
孙立丽, 王萌, 任晓亮. 化学模式识别方法在中药质量控制研究中的应用进展[J]. 中草药, 2017, 48(20): 4339-4345. SUN L L, WANG M, REN X L. Application progress on chemical pattern recognition in quality control of Chinese materia medica[J]. Chinese Traditional and Herbal Drugs, 2017, 48(20): 4339-4345. DOI:10.7501/j.issn.0253-2670.2017.20.031 |
| [18] |
顾志荣, 师富贵, 金岩. 化学模式识别在中药分析中的应用研究[J]. 甘肃中医学院学报, 2014, 31(3): 108-111. GU Z R, SHI F G, JIN Y. Application of chemical pattern recognition inanalysis of traditional Chinese medicine[J]. Journal of Gansu College of Traditional Chinese Medicine, 2014, 31(3): 108-111. |
| [19] |
毛睿, 刘亚男, 李丽红, 等. 麻黄饮片等级质量标准研究[J]. 天津中医药大学学报, 2019, 38(3): 274-278. MAO R, LIU Y N, LI L H, et al. Study on the grade quality standard of Ephedra Sinica[J]. Journal of Tianjin University of Traditional Chinese Medicine, 2019, 38(3): 274-278. |
| [20] |
李峰庆, 王福, 杨放晴, 等. 利用UHPLC-ESI-MS/MS法测定川陈皮与其混伪品中的黄酮类成分[J]. 天然产物研究与开发, 2020, 32(8): 1324-1330. LI F Q, WANG F, YANG F Q, et al. Analysis of flavonoids in Chuan Citrus reticulata pericarpium and its adulterant using UHPLC-ESI-MS/MS[J]. Natural Product Research and Development, 2020, 32(8): 1324-1330. |
 2022, Vol. 41
2022, Vol. 41