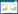文章信息
- 陈小存, 魏谭军, 陈飞, 肖成, 陈勇
- CHEN Xiaocun, WEI Tanjun, CHEN Fei, XIAO Cheng, CHEN Yong
- 高效液相一测多评法同时测定阴虚胃痛颗粒中8种成分含量
- Simultaneous determination of eight compounds in Yinxu Weitong Granules by HPLC-QAMS
- 天津中医药大学学报, 2022, 41(3): 361-367
- Journal of Tianjin University of Traditional Chinese Medicine, 2022, 41(3): 361-367
- http://dx.doi.org/10.11656/j.issn.1673-9043.2022.03.18
-
文章历史
收稿日期: 2021-12-20
2. 成都地奥集团天府药业有限公司, 达州 635027
2. Chengdu Diao Group Tianfu Pharmaceutical Co. Ltd., Dazhou 635027, China
阴虚胃痛颗粒由麦冬、北沙参、白芍等7味中药组成,具有养阴益胃、缓急止痛的功效,临床上主要用于胃阴不足及慢性胃炎引起的胃脘隐隐灼痛、口干舌燥、纳呆干呕等病症的治疗[1]。现代研究表明阴虚胃痛颗粒联合三联疗法对阴虚型慢性胃炎治疗效果显著,可明显改善患者临床症状,且不良反应较少[2]。
中药及其制剂,尤其是中成药复方制剂,由多味中药材按照中医基础理论配伍组方而来,具有多成分-多靶点-多途径的整体特点,不同成分的生物活性各异,方中药物所含化学成分相互协同、相互制约以达到临床治疗效果。《中华人民共和国药典》(2020年版)阴虚胃痛颗粒[1]项下仅对佐药白芍所含芍药苷进行定量测定,暂无对该制剂所含成分的文献报道,难以全面反映阴虚胃痛颗粒的整体质量。本研究参考中药质量标志物以君药所含成分为首选,兼顾臣、佐、使药成分的确认原则,选取君药北沙参所含活性成分法卡林二醇和人参炔醇、麦冬所含特征成分麦冬甲基黄烷酮A和甲基麦冬二氢高异黄酮B,以及佐药白芍所含主要成分氧化芍药苷、芍药内酯苷、芍药苷和苯甲酰芍药苷为定量控制指标成分,采用高效液相一测多评(HPLC-QAMS)法对上述成分含量同时进行测定,建立阴虚胃痛颗粒多指标成分质量控制模式,以期全面评价阴虚胃痛颗粒的整体质量,指导药品生产企业提升制剂的质量控制标准,完善制剂生产过程和原药材来源质量控制,为指导临床合理用药提供基础保障。
1 仪器与试药对照品芍药苷(批号110736-202044,质量分数96.8%)来源于中国食品药品检定研究院;对照品氧化芍药苷(批号PRF9040222,质量分数98.4%)、芍药内酯苷(批号PRF8101147,质量分数98.6%)、苯甲酰芍药苷(批号PRF8040621,质量分数97.2%)、麦冬甲基黄烷酮A(批号PRF8041122,质量分数99.9%)、甲基麦冬二氢高异黄酮B(批号PRF7102423,质量分数98.3%)、法卡林二醇(批号PRF9061222,质量分数99.4%)和人参炔醇(批号PRF8033144,质量分数98.5%)均来源于成都普瑞法科技开发有限公司;阴虚胃痛颗粒(规格:每袋装10 g,批号分别为20190501、20200221和20200309)来源于辽宁华润本溪三药有限公司;乙腈为色谱纯,其余试剂均为分析纯。Agilent 1260 Infinity Ⅱ型高效液相色谱仪(美国Agilent公司)、岛津LC-2030型高效液相色谱仪(日本岛津公司);Agilent HC C18、Kromasil C18和Xtimate C18色谱柱(规格250 mm×4.6 mm,5 μm);Quintix125D-1CN型十万分之一电子天平(德国赛多利斯公司);CSA-10BT型超声波发生器(上海沙鹰科学仪器有限公司)。
2 方法与结果 2.1 混合对照品溶液的配制各取氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇对照品适量,精密称定,用稀乙醇制成1 mL含氧化芍药苷0.454 mg、芍药内酯苷1.208 mg、芍药苷3.516 mg、苯甲酰芍药苷0.322 mg、麦冬甲基黄烷酮A 0.270 mg、甲基麦冬二氢高异黄酮B 0.138 mg、法卡林二醇0.212 mg和人参炔醇0.396 mg的混合对照品贮备液。精密吸取上述贮备液1.0 mL,用稀乙醇稀释至25 mL,制成混合对照品溶液(氧化芍药苷18.16 μg/mL、芍药内酯苷48.32 μg/mL、芍药苷140.64 μg/mL、苯甲酰芍药苷12.88 μg/mL、麦冬甲基黄烷酮A 10.80 μg/mL、甲基麦冬二氢高异黄酮B 5.52 μg/mL、法卡林二醇8.48 μg/mL和人参炔醇15.84 μg/mL)。
2.2 供试品溶液的配制取阴虚胃痛颗粒适量,精密称定研细后细粉2.0 g,加稀乙醇20 mL,对供试品超声处理30 min,放冷并用稀乙醇稀释至25 mL,摇匀,0.45 μm微孔滤膜过滤,续滤液作为阴虚胃痛颗粒供试品溶液。取按照阴虚胃痛颗粒质量标准处方比例和制法制备的缺白芍、缺麦冬、缺北沙参的阴性供试品各适量,按上述方法制得阴性供试品溶液。
2.3 色谱条件及系统适用性色谱柱为Agilent HC C18柱(250 mm×4.6 mm,5 μm),柱温30 ℃;检测波长分别为230 nm(0~25 min测定氧化芍药苷、芍药内酯苷、芍药苷和苯甲酰芍药苷)[3-5]、296 nm(25~34 min测定麦冬甲基黄烷酮A和甲基麦冬二氢高异黄酮B)[6-7]和254 nm(34~55 min,测定法卡林二醇和人参炔醇)[8-9];流动相为乙腈-0.1%磷酸,梯度洗脱(0~9 min,16.0%乙腈;9~25 min,16.0%→48.0%乙腈;25~34 min,48.0%A→55.0%乙腈;34~46 min,55.0%→78.0%乙腈;46~55 min,78.0%→16.0%乙腈),流速1.0 mL/min,进样量10 μL。理论塔板数按各成分色谱峰计均应≥4 500。
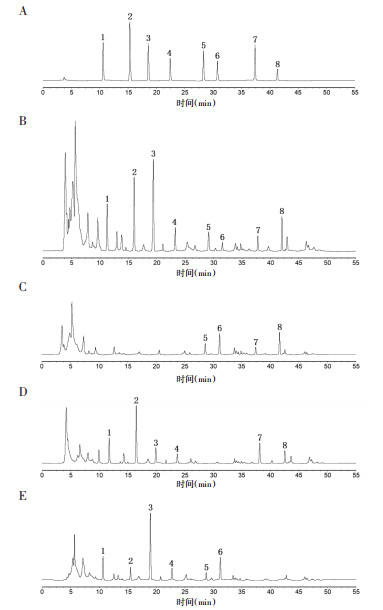
2.4 方法学考察 2.4.1 专属性精密吸取“2.1”项下混合对照品溶液及“2.2”项下溶液各10 μL,注入高效液相色谱仪中,记录所测色谱图,见图 1。结果显示阴虚胃痛颗粒供试品溶液中氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇与相邻色谱峰分离良好,分离度均>1.5;所测指标成分色谱峰峰形对称,拖尾因子符合《中华人民共和国药典》规定;阴性供试品对阴虚胃痛颗粒中氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的同时测定无干扰。
|
| 注:1.氧化芍药苷;2.芍药内酯苷;3.芍药苷;4.苯甲酰芍药苷;5.麦冬甲基黄烷酮A;6.甲基麦冬二氢高异黄酮B;7.法卡林二醇;8.人参炔醇;A.混合对照品;B.阴虚胃痛颗粒;C.白芍阴性供试品;D.麦冬阴性供试品;E.北沙参阴性供试品。 图 1 高效液相色谱图 |
精密吸取“2.1”项下氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇混合对照品贮备液0.1、0.5、1.0、1.5、2.0和2.5 mL,置于不同的20 mL容量瓶中,用稀乙醇稀释至20 mL配制成6个不同浓度的混合对照品溶液,各精密吸取10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,以质量浓度(μg/mL)为X轴,峰面积为Y轴进行线性回归分析,得回归方程及线性范围。见表 1。
精密吸取批号为20190501的阴虚胃痛颗粒同一份供试品溶液10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,重复操作6次,测得8种成分峰面积的RSD值分别为1.11%、0.86%、0.53%、1.07%、1.20%、1.13%、0.99%和0.85%,表明该方法日内精密度良好;连续3 d,每日重复进样3次进行日间精密度考察,结果8种成分峰面积的RSD值分别为1.05%、0.79%、0.63%、1.20%、1.16%、1.19%、0.92%和1.07%,表明该方法日间精密度良好。
2.4.4 重复性取批号为20190501的阴虚胃痛颗粒6份,按“2.2”项下方法制备供试品溶液,各精密吸取10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积并计算各成分含量,结果8种成分含量的RSD值分别为1.08%、0.91%、0.60%、1.15%、1.19%、1.07%、1.02%和0.96%。
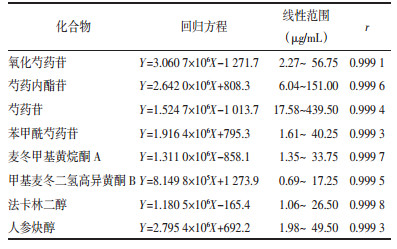
2.4.5 稳定性取批号为20190501的阴虚胃痛颗粒同一份供试品溶液,于0、2、4、8、16和24 h各精密吸取10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,结果阴虚胃痛颗粒供试品溶液24 h内稳定,8种成分峰面积的RSD值分别为1.82%、1.35%、0.96%、1.42%、1.80%、0.89%、1.74%和1.62%。
2.4.6 加样回收率取已知氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇含量的批号为20190501的阴虚胃痛颗粒细粉9份,每份1.0 g,精密称定,随机平分成3组,每组精密加入混合对照品溶液(氧化芍药苷0.242 mg/mL、芍药内酯苷0.752 mg/mL、芍药苷1.858 mg/mL、苯甲酰芍药苷0.174 mg/mL、麦冬甲基黄烷酮A 0.130 mg/mL、甲基麦冬二氢高异黄酮B 0.058 mg/mL、法卡林二醇0.114 mg/mL、人参炔醇0.218 mg/mL)0.8、1.0和1.2 mL,使加入量与所取阴虚胃痛颗粒中各目标成分含量之比约控制在0.8∶1、1∶1和1.2∶1,再按“2.2”项下方法制备成加样供试品溶液。各精密吸取10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积并计算各成分加样回收率及RSD值。结果表明阴虚胃痛颗粒中8种成分的平均加样回收率及RSD分别为98.90%(1.01%)、100.02%(0.94%)、99.52%(0.76%)、97.88%(1.35%)、99.14%(1.42%)、96.85%(0.65%)、97.83%(0.92%)和98.65%(1.24%)。
2.5 HPLC-QAMS法的质量评价模式建立 2.5.1 建立相对校正因子(RCF)精密吸取“2.4.2”项6个不同浓度的混合对照品溶液各10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,用质量浓度与峰面积之比计算各成分校对因子,将待测成分与内参物的校正因子之比计算为各成分的RCF,即RCFk/s=fk/fs=(Wk/Ak)/(Ws/As)=(Wk×As)/(Ws×Ak),f、W和A分别代表RCF、质量浓度和峰面积,k、s分别代表其他待测成分及内参物。以芍药苷为内参物,根据上述公式分别计算得芍药苷对氧化芍药苷、芍药内酯苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的RCF。见表 2。
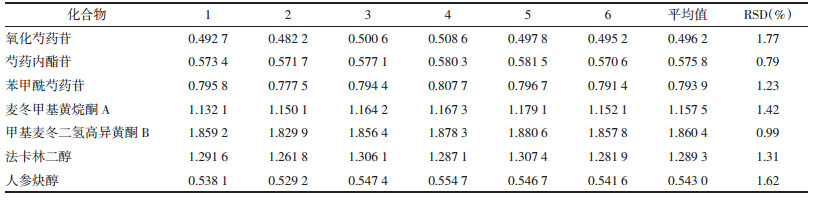
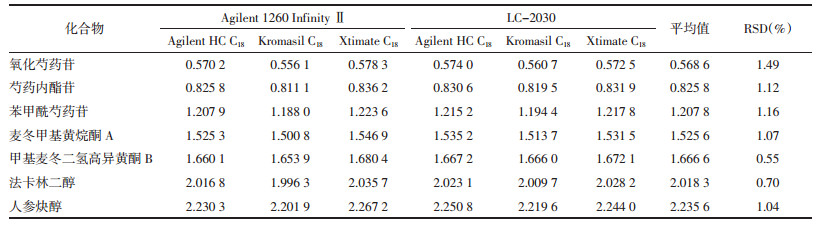
在不同仪器(Agilent 1260 Infinity Ⅱ型和岛津LC-2030型高效液相色谱仪)和色谱柱(Agilent HC C18、Kromasil C18和Xtimate C18柱)条件下,精密吸取“2.1”项下混合对照品溶液10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,计算得芍药苷对氧化芍药苷、芍药内酯苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的RCF。见表 3。
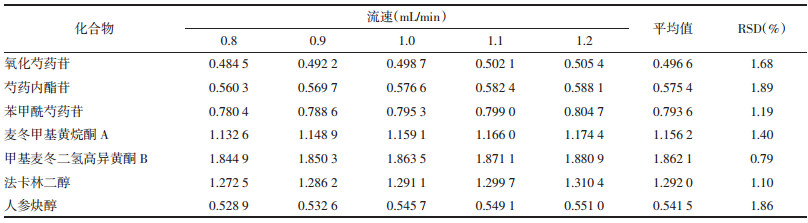
在不同流速(0.8、0.9、1.0、1.1和1.2 mL/min)条件下,精密吸取“2.1”项下混合对照品溶液10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,计算得芍药苷对氧化芍药苷、芍药内酯苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的RCF。见表 4。
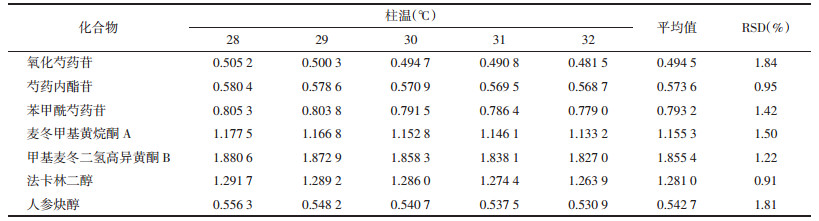
在不同柱温(28、29、30、31和32 ℃)条件下,精密吸取“2.1”项下混合对照品溶液10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,计算得芍药苷对氧化芍药苷、芍药内酯苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的RCF。见表 5。
待测物色谱峰的准确定位是HPLC-QAMS法可行性的基础,在不同仪器(Agilent 1260 Infinity Ⅱ型和岛津LC-2030型高效液相色谱仪)和色谱柱(Agilent HC C18、Kromasil C18和Xtimate C18柱)条件下,精密吸取“2.1”项下混合对照品溶液10 μL,注入高效液相色谱仪中进样检测,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇色谱峰的保留时间,将待测成分与内参物保留时间之比计算各成分的相对保留时间值(RRT),计算得芍药苷对氧化芍药苷、芍药内酯苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的RRT。见表 6。
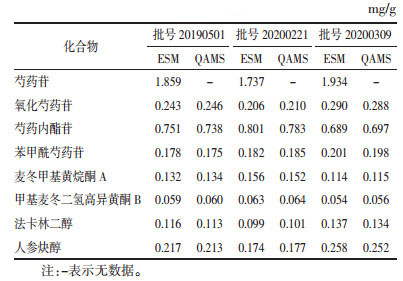
为验证所建立的HPLC-QAMS方法的准确性和可行性,各取3个批次的阴虚胃痛颗粒适量,按“2.2”项方法制备阴虚胃痛颗粒供试品溶液(每个批次平行制备3份),各精密吸取上述供试品溶液10 μL,注入高效液相色谱仪中,记录氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的峰面积,分别采用ESM和HPLC-QAMS法计算阴虚胃痛颗粒中氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的含量,并采用SPSS 26.0统计软件对两种方法检测结果进行分析,结果显示两种方法所得结果无统计学差异(P>0.05)。见表 7。
阴虚胃痛颗粒由白芍、麦冬、北沙参、石斛、玉竹、川楝子和炙甘草组方而来,北沙参养阴清肺、益胃生津,麦冬养阴生津、润肺清心,合为君药;石斛益胃生津、滋阴清热,玉竹养阴润燥、生津止渴,共为臣药;白芍养血敛阴、柔肝止痛,川楝子疏肝泄热、行气止痛,合为佐药;炙甘草补脾和胃、益气复脉、调和诸药,为使药。7味中药材所含化学成分相互协调、相互制约,共达养阴益胃、缓急止痛的临床功效。为全面评价阴虚胃痛颗粒的整体质量,本研究参考中药质量标志物的确认原则[10],以君药所含成分为首选,兼顾臣、佐、使药所含成分,选取君药北沙参活性成分法卡林二醇和人参炔醇、麦冬特征成分麦冬甲基黄烷酮A和甲基麦冬二氢高异黄酮B,以及佐药白芍主要成分氧化芍药苷、芍药内酯苷、芍药苷和苯甲酰芍药苷8种成分进行定量控制研究。内参物的选择对所建立HPLC-QAMS法的准确性和可行性至关重要,本研究选取成分较为稳定、样品中含量较高、价格低廉易得、出峰时间适中的芍药苷为内参物。
以阴虚胃痛颗粒中目标成分氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的分离效果为主要考察指标,兼顾分析检测用时、色谱图基线平稳等因素,考察了不同流动相洗脱系统,结果显示乙腈-水[6-7, 9]优于甲醇-水流动相洗脱,但目标成分氧化芍药苷、人参炔醇达不到有效分离。以乙腈为有机相,参考文献报道对乙腈-0.1%磷酸溶液[3-5]、乙腈-0.1%甲酸溶液[7-8]进行对比考察,选取乙腈-0.1%磷酸溶液为流动相,通过对流动相中有机相和水相比例的不断摸索,最终确定以“2.3”项下的梯度洗脱程序对阴虚胃痛颗粒中氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇含量同时进行检测。结果提示在此条件下,各成分分离效果较好,色谱图基线平稳,杂质对目标成分的测定干扰较小。本实验在处理阴虚胃痛颗粒供试品溶液时,依次考察了甲醇[6]、70%甲醇[7]、稀乙醇[3-5, 8]等提取溶剂以及超声[3-9]和加热回流提取两种提取方式,以氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇的综合提取率为首要指标,兼顾杂质干扰程度,最终确定以稀乙醇超声处理30 min对阴虚胃痛颗粒进行供试品制备。
4 结论自“2.6”项下氧化芍药苷、芍药内酯苷、芍药苷、苯甲酰芍药苷、麦冬甲基黄烷酮A、甲基麦冬二氢高异黄酮B、法卡林二醇和人参炔醇含量检测结果可以看出,HPLC-QAMS法的计算结果与外标法实测值之间无明显差异,表明本研究所建立的HPLC-QAMS法结果准确,可用于对阴虚胃痛颗粒中8种指标成分的同时测定,能够作为阴虚胃痛颗粒多指标成分的质量控制方法。同时也反映出8种目标成分存在一定的批间差异,尤其氧化芍药苷、麦冬甲基黄烷酮A、法卡林二醇和人参炔醇含量差异较为明显,表明多指标成分的质量控制对稳定阴虚胃痛颗粒产品质量、确保临床用药疗效一致性具有重要意义,有助于药品生产企业和监管部门不断提升阴虚胃痛颗粒的质量控制标准,建立健全该制剂原药材来源及内控质量标准,不断细化完善制剂生产过程的操作参数控制,以期保证阴虚胃痛颗粒产品质量稳定,为指导临床合理用药提供有效参考依据。
| [1] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2020. The National Pharmacopoeia Commission. Pharmacopoeia of People's Republic of China[M]. Beijing: China Medical Science and Technology Press, 2020. |
| [2] |
朱峰. 阴虚胃痛颗粒联合三联疗法治疗阴虚型慢性胃炎的疗效研究[J]. 中国医药指南, 2019, 17(30): 221. ZHU F. Study on the curative effect of Yinxu Weitong Granule combined with triple therapy on chronic gastritis of Yinxu typ[J]. Guide of China Medicine, 2019, 17(30): 221. |
| [3] |
成守玲, 王晓楠, 信文远, 等. 白芍药材、饮片、提取物及配方颗粒的HPLC特征图谱相关性研究[J]. 中华中医药杂志, 2020, 35(11): 5712-5715. CHENG S L, WANG X N, XIN W Y, et al. Correlation study on HPLC specific chromatogram of crude drug, decoction pieces, extractives, concentrated granules of Paeoniae Radix Alba[J]. China Journal of Traditional Chinese Medicine and Pharmacy, 2020, 35(11): 5712-5715. |
| [4] |
俞叶飞, 王盼, 陈子林, 等. 不同干燥方法对白芍药材初加工过程中品质的影响[J]. 浙江中医杂志, 2020, 55(12): 922-923. YU Y F, WANG P, CHEN Z L, et al. Effect of different drying methods on quality of Radix Paeoniae Alba in initial processing[J]. Zhejiang Journal of Traditional Chinese Medicine, 2020, 55(12): 922-923. DOI:10.3969/j.issn.0411-8421.2020.12.045 |
| [5] |
徐超, 林杰, 金传山, 等. HPLC指纹图谱结合化学计量学比较同株不同生长年限亳白芍化学成分差异[J]. 中草药, 2021, 52(8): 2408-2413. XU C, LIN J, JIN C S, et al. Comparison of chemical composition of Paeoniae Alba Radix in Bozhou with HPLC fingerprint and chemometrics in different growth years of same plant[J]. Chinese Traditional and Herbal Drugs, 2021, 52(8): 2408-2413. |
| [6] |
吴发明, 杨瑞山, 张思荻, 等. 高效液相色谱法同时测定麦冬中3个黄酮成分的含量[J]. 中国药学杂志, 2016, 51(8): 655-658. WU F M, YANG R S, ZHANG S D, et al. Simultaneous determination of three flavone constituents in ophiopogonis Radix by HPLC method[J]. Chinese Pharmaceutical Journal, 2016, 51(8): 655-658. |
| [7] |
谈梦霞, 陈佳丽, 邹立思, 等. 不同加工麦冬中多元活性成分的含量测定及多元统计分析[J]. 药物分析杂志, 2019, 39(6): 992-1002. TAN M X, CHEN J L, ZOU L S, et al. Determination of multiple bioactive constituents in Ophiopogonis Radix processed by different methods and multivariate statistical analysis[J]. Chinese Journal of Pharmaceutical Analysis, 2019, 39(6): 992-1002. |
| [8] |
利宇恒, 王鹏远, 刘超威, 等. 不同干燥方法对北沙参中5种香豆素及多糖含量的影响分析[J]. 广东化工, 2021, 48(2): 44-47. LI Y H, WANG P Y, LIU C W, et al. Analysis on the influence of different drying methods on the five kinds of cumarin and polysaccharide content in Radix glehniae[J]. Guangdong Chemical Industry, 2021, 48(2): 44-47. DOI:10.3969/j.issn.1007-1865.2021.02.020 |
| [9] |
冯子晋, 卢小玲, 张建鹏, 等. 北沙参中香豆素类与聚炔类成分的含量测定研究[J]. 中国海洋药物, 2014, 33(3): 20-26. FENG Z J, LU X L, ZHANG J P, et al. The study of the contents of coumarin and polyacetylene in Glehnia Littoralis[J]. Chinese Journal of Marine Drugs, 2014, 33(3): 20-26. |
| [10] |
刘昌孝, 陈士林, 肖小河, 等. 中药质量标志物(Q-Marker): 中药产品质量控制的新概念[J]. 中草药, 2016, 47(9): 1443-1457. LIU C X, CHEN S L, XIAO X H, et al. A new concept on quality marker of Chinese materia medica: quality control for Chinese medicinal products[J]. Chinese Traditional and Herbal Drugs, 2016, 47(9): 1443-1457. |
 2022, Vol. 41
2022, Vol. 41