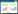文章信息
- 王敏, 薛志峰, 孙新茹, 李丹丹, 王志娟, 惠玉玉, 刘志东
- WANG Min, XUE Zhifeng, SUN Xinru, LI Dandan, WANG Zhijuan, HUI Yuyu, LIU Zhidong
- 羌活胜湿汤物质基准多指标成分含量测定及量值传递分析
- Analysis on the determination and quantity transfer of multi index components in Qianghuo Shengshi Decoction
- 天津中医药大学学报, 2024, 43(1): 15-21
- Journal of Tianjin University of Traditional Chinese Medicine, 2024, 43(1): 15-21
- http://dx.doi.org/10.11656/j.issn.1673-9043.2024.01.03
-
文章历史
收稿日期: 2023-08-30
2. 天津中医药大学, 组分中药国家重点实验室, 天津 301617;
3. 哈尔滨珍宝制药有限公司, 哈尔滨 150040
2. State Key Laboratory of Multi-fractions Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China;
3. Harbin Zhenbao Pharmaceutical Co., Ltd., Harbin 150040, China
羌活胜湿汤(QSD)出自金代医家李东垣所著《内外伤辨惑论》[1],由羌活、独活、藁本、防风、川芎、炙甘草、蔓荆子7味中药组成,具有祛风胜湿止痛之功,主治风湿在表之痹证,是临床祛风湿止痛的中药复方。现代临床研究表明本方主要用于关节炎、颈椎病、偏头痛、肩背疼痛等疾病的治疗[2]。经典名方是近年来的研究热点,其复方制剂是中药产品发展的重要途径[3],而经典名方物质基准更是其复方制剂研发和开展的核心内容,QSD被收录在国家中医药管理局发布的第1批古代经典名方目录中。目前,关于QSD的文献报道多集中于药理作用及临床应用领域,物质基准方面鲜有研究。本研究根据国家药品监督管理局发布的《古代经典名方关键信息考证原则》等相关指导原则,通过制备15批经典名方QSD物质基准冻干粉,采用高效液相(HPLC)法建立QSD多指标成分含量测定方法,测定其指标成分含量,进行饮片到物质基准之间的量值传递分析,为经典名方QSD后续的研究及相关制剂研发的质量控制提供依据。
1 仪器与材料 1.1 仪器1260型高效液相色谱仪,DAD检测器,美国Agilent公司;AX205型十万分之一天平,瑞士METTLER TOLEDO公司;FA124型万分之一天平,天津亿诺科学仪器有限公司;Milli-Q超纯水系统,美国Millipore公司;DZL煎药壶,潮州市潮安区康尔顺贸易有限公司;TDGC2-3KVA型接触式调压器,飘风电器有限公司;N-10000旋转蒸发仪,日本EYELA公司;DK-98-Ⅱ型电热恒温水浴槽,天津市泰斯特仪器有限公司;KQ-400B超声波清洗仪,昆山市超声仪器有限公司;FW100型万能粉碎机,天津市泰斯特仪器有限公司;B-290型喷雾干燥仪,瑞士Buchi公司;DZF-6090型真空干燥箱,上海新苗医疗器械制造有限公司;FDU-2100型冷冻干燥机,日本EYELA公司。
1.2 试药羌活醇(111820-201504,含量以99.9%计)、二氢欧山芹醇当归酸酯(111583-201605,含量以98.6%计)、5-O-甲基维斯阿米醇苷(111523-201610,含量以96.1%计)、蔓荆子黄素(111554-201705,含量以98.3%计)、异欧前胡素对照品(110827-201611,含量以99.4%计)、甘草酸铵对照品(110731-201619,含量以93.0%计)均购自中国食品药品鉴定研究所;甲醇(色谱级,赛默飞世尔科技有限公司),乙腈(色谱级,赛默飞世尔科技有限公司),磷酸(色谱级,批号130271,赛默飞世尔科技有限公司),实验室自制超纯水;QSD物质基准15批次,批号及所用饮片产地信息见表 1,由黑龙江珍宝岛药业股份有限公司提供,经过天津中医药大学祁东利副研究员鉴定羌活NOTOPTERYGⅡ RHIZOMA ET RADIX、独活ANGELICAE PUBESCENTIS RADIX、藁本LIGUSTICI RHIZOMA ET RADIX、防风SAPOSHNIKOVIAE RADIX、炙甘草GLYCYRRHIZAE RADIX ET RHIZOMA PRAEPARATA CUM MELLE、川芎CHUANX-IONG RHIZOMA、蔓荆子VITICIS FRUCTUS均符合《中华人民共和国药典》2020年版要求。
色谱条件:Agilent ZORBAX SB-C18色谱柱。流动相为乙腈-0.05%磷酸水。洗脱梯度:0~15 min,12%~15%乙腈;15~37 min,15%~19%乙腈;37~52 min,19%~24%乙腈;52~64 min,24%~27%乙腈;64~75 min,27%~37%乙腈;75~92 min,37%~50%乙腈;92~109 min,50%~58%乙腈;109~113 min,58%~90%乙腈;113~125 min,90%乙腈。柱温30 ℃。体积流量0.8 mL/min。进样量10 μL。检测波长:254(检测5-O-甲基维斯阿米醇苷和蔓荆子黄素)、310(检测羌活醇和异欧前胡素)、237(检测甘草酸铵)、330(检测二氢欧山芹醇当归酸酯)nm。
2.2 对照品溶液的制备精密称取5-O-甲基维斯阿米醇苷、蔓荆子黄素、羌活醇、异欧前胡素、甘草酸铵、二氢欧山芹醇当归酸酯对照品适量,加入甲醇制成1 mL含18.08 μg 5-O-甲基维斯阿米醇苷、4.47 μg蔓荆子黄素、44.7 μg羌活醇、8.016 μg异欧前胡素、504 μg甘草酸铵、4.29 μg二氢欧山芹醇当归酸酯的混合对照品溶液。
2.3 QSD物质基准冻干粉的制备采用随机数字表法,分别对方中各饮片进行随机组合,见表 1。《内外伤辨惑论》原文记载的QSD处方及制法为“羌活、独活各一钱,藁本、防风、甘草(炙)、川芎各五分,蔓荆子三分。上㕮咀,都作一服,水二盏,煎至一盏,去渣,大温服,空心食前”。经前期考证,确定处方剂量为羌活、独活各3.0 g,川芎、藁本、炙甘草、防风各1.5 g,蔓荆子0.9 g。取各饮片置于砂锅中,加入去离子水400 mL,浸泡30 min后煎煮至药液体积剩余约200 mL,使用两层纱布趁热过滤,置于室温冷却后,将标准汤剂旋转蒸发至流浸膏,预冻后冷冻干燥,即得15批QSD物质基准冻干粉,同法制备各阴性冻干粉。
2.4 供试品溶液的制备取“2.3”项下制备的QSD冻干粉0.2 g,精密称定,置于具塞锥形瓶中,精密移取60%甲醇(v/v)10 mL,称取质量,320 W、40 kHz超声处理45 min,放冷至室温,补足失去质量,摇匀,0.22 μm微孔滤膜滤过,取续滤液,即得。
2.5 含量测定方法学考察 2.5.1 专属性考察分别精密吸取按“2.2”项及“2.4”项下制备得到的各对照品溶液、供试品溶液及各阴性样品溶液,按“2.1”项下的色谱条件分别进样分析,记录色谱图,见图 1。结果显示,阴性对照图中显示对5-O-甲基维斯阿米醇苷、蔓荆子黄素、羌活醇、异欧前胡素、甘草酸铵、二氢欧山芹醇当归酸酯的测定无干扰。

|
| 注:A,完整色谱图;B,各指标成分放大色谱图;1,5-O-甲基维斯阿米醇苷;2,甘草酸铵;3,蔓荆子黄素;4,羌活醇;5,异欧前胡素;6,二氢欧山芹醇当归酸酯;a,对照品;b,QSD物质基准;c,甘草阴性;d,防风阴性;e,独活阴性;f,羌活阴性;g,蔓荆子阴性。 图 1 QSD专属性考察HPLC图 |
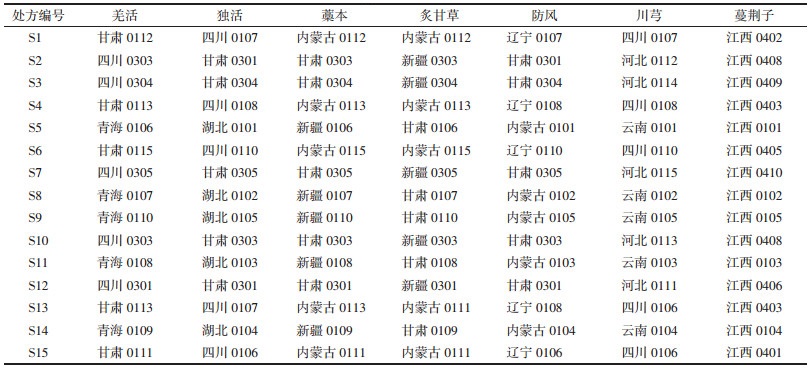
精密吸取按“2.2”项下制备的混合对照品溶液适量,用甲醇稀释成不同质量浓度的系列对照品溶液。按“2.1”项下的色谱条件进样分析,记录峰面积。以质量浓度为横坐标(X),峰面积为纵坐标(Y),进行线性回归,绘制标准曲线,如表 2所示。结果表明,各指标成分线性关系良好。
精密吸取一定浓度的混合对照品溶液,按“2.1”项下的含量测定色谱条件进样洗脱,连续进样6次,记录各指标成分峰面积,计算得到的峰面积RSD值均小于3.00%,结果表明该方法仪器精密度良好。
2.5.4 稳定性实验取同一批物质基准供试品溶液,按“2.1”项下色谱条件,分别于供试品溶液制备后0、2、4、8、12、24、36、48 h进样分析,记录峰面积,计算5-O-甲基维斯阿米醇苷、蔓荆子黄素、羌活醇、异欧前胡素、甘草酸铵、二氢欧山芹醇当归酸酯峰面积的RSD值分别为2.85%、1.91%、0.92%、2.53%、0.67%、2.01%,表明供试品溶液在48 h内稳定性良好。
2.5.5 重复性实验取同一批物质基准供试品溶液6份,按“2.1”项下的色谱条件进样分析,记录峰面积,计算5-O-甲基维斯阿米醇苷、蔓荆子黄素、羌活醇、异欧前胡素、甘草酸铵、二氢欧山芹醇当归酸酯含量的RSD值分别为2.86%、1.60%、0.76%、0.71%、0.81%、0.89%,表明该方法重复性良好。
2.5.6 加样回收率实验取上述重复性实验已测定各指标成分含量的同批次QSD物质基准冻干粉适量,精密称定,分别以指标成分含量的50%加入各指标成分对照品储备液各6份,按“2.4”项下的方法制备供试品溶液。按“2.1”项下的色谱条件进样测定,计算各指标成分的回收率。结果如表 1所示,各指标成分平均加样回收率均在95%~105%,RSD在0.77%~3.69%,结果表明加样回收率良好。
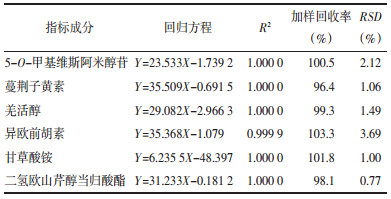
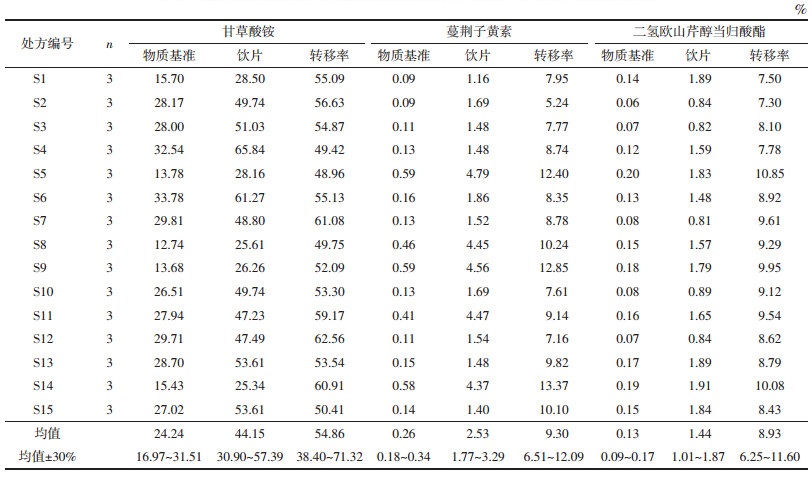
2.6 15批QSD物质基准指标成分含量及饮片-物质基准转移率测定采用“2.4”项下的方法分别制备15批物质基准供试品溶液,按“2.1”项下的色谱条件进样测定15批物质基准中各指标成分的含量,各饮片按照《中华人民共和国药典》2020年版进行含量测定[4],按公式“转移率(%)=[物质基准中指标成分含量(mg/g)]÷[对应批次饮片中指标成分含量(mg/g)]×100%”计算各指标成分饮片到物质基准的含量转移率,结果见表 3及表 4。
由表 3、表 4结果可知,15批物质基准中指标成分5-O-甲基维斯阿米醇苷含量为1.27~2.81 mg/g,平均转移率为77.60%,转移率均值的±30%为54.32%~100.88%;羌活醇含量为1.09~1.70 mg/g,平均转移率为16.82%,转移率均值的±30%为11.77%~21.87%;异欧前胡素含量为0.03~0.28 mg/g,平均转移率为1.44%,转移率均值的±30%为1.01%~1.87%;甘草酸铵含量为12.74~33.78 mg/g,平均转移率为54.86%,转移率均值的±30%为38.40%~71.32%;蔓荆子黄素含量为0.09~0.59 mg/g,平均转移率为9.30%,转移率均值的±30%为6.51%~12.09%;二氢欧山芹醇当归酸酯含量为0.06~0.20 mg/g,平均转移率为8.93%,转移率均值的±30%为6.25%~11.60%。
3 讨论 3.1 含量测定及指标成分的选择中药有效成分作为中药的药效物质基础,其选择及确定是中药复方及单味药材质量控制的重要过程,含量测定指标成分的选择不仅要符合《中华人民共和国药典》2020年版[4]的规定,还要确保其在相应的饮片、物质基准及复方能够实现可靠稳定的质量控制。本方选取的指标成分羌活醇、异欧前胡素、二氢欧山芹醇当归酸酯、甘草酸铵、蔓荆子黄素、5-O-甲基维斯阿米醇苷均为《中华人民共和国药典》2020年版[4]中羌活、独活、甘草、蔓荆子、防风药材的含量测定成分,均为专属性成分,且对于他们的药理作用有明确的文献报道[5-16]。独活、甘草在《中华人民共和国药典》2020年版中含量测定的成分还有蛇床子素、甘草苷,进行专属性实验时在独活阴性中有干扰;甘草苷出现峰形不好、不易分开等现象,故蛇床子素与甘草苷没有作为指标成分进行测定。《中华人民共和国药典》2020年版中藁本、川芎的含量测定成分均为阿魏酸,无法作为专属性指标成分,且藁本、川芎的化学成分相似[17-18],经实验研究,未在藁本、川芎中找到专属性成分。
3.2 色谱条件及样品处理方法的考察本实验前期对含量测定色谱条件的不同流速(0.7、0.8、0.9 mL/min)、不同柱温(30、35、40 ℃)、不同比例的流动相进行梯度洗脱,考察色谱图出峰个数、峰形及分离度情况。结果表明流速为0.8 mL/min、柱温为30 ℃时,各峰形较好,分离度较好,整体基线较平稳。对样品的处理方法考察了不同比例甲醇、乙腈和纯水的提取溶剂,不同超声功率及超声时间,以色谱图整体峰形及分离度结果确定了60%甲醇复溶、超声功率320 W、超声45 min的样品处理方法。
3.3 物质基准各指标成分的含量及量值传递分析根据《古代经典名方中药复方制剂的申报资料要求(征求意见稿)》中的指导建议,出膏率、指标性成分含量转移率应在均值±30%的波动范围内。结果提示15批物质基准的平均出膏率为31.86%,RSD为3.77%,均未出现离散数据(平均值的70%~130%以外)。指标成分5-O-甲基维斯阿米醇苷、甘草酸铵、二氢欧山芹醇当归酸酯转移率均在均值±30%内;异欧前胡素转移率中S5、S15批次超出范围;蔓荆子黄素转移率中S2、S5、S9、S14批次超出范围;羌活醇转移率中S1、S4、S9、S13、S14、S15批次超出范围。分析其原因发现不同批次饮片中羌活醇、异欧前胡素、蔓荆子黄素含量差异较大,导致多批次饮片-物质基准转移率超出范围;中药成分复杂,中药复方中各成分相互作用、相互影响也是造成指标成分转移率波动范围较大的原因之一;15批QSD物质基准各指标成分含量范围较大,组成QSD物质基准的饮片含量差异较大,15批QSD物质基准的原料来自不同产地,导致其各项指标成分含量差异较大。所以在以后的研究中,要确保选取药材的来源和质量稳定,进行药材道地产地和主产地之间指标含量等质量的差异分析,选择一定的含量范围,以此初步选定药材产地,除此之外投料的均一性也是保证含量稳定的重要条件[19]。建议剔除离散程度较大的批次数值,后续研究增加物质基准研究批次,严格控制饮片的质量波动,以保证不同批次物质基准的质量相对稳定,降低离散值的影响,以期建立更加具有代表性的物质基准相关质量标准。
4 结论本实验通过制备15批QSD物质基准冻干粉,建立其含量测定方法,测定专属成分羌活醇、异欧前胡素、二氢欧山芹醇当归酸酯、甘草酸铵、蔓荆子黄素、5-O-甲基维斯阿米醇苷含量并进行饮片到物质基准量值传递分析,建议在后续的研究中严格把控投料饮片的质量情况,以期为经典名方QSD后续物质基准与制剂研发的一致性和稳定性提供依据。
| [1] |
李东垣. 内外伤辨惑论[M]. 田翠时, 校注. 北京: 中国医药科技出版社, 2011: 21-22.
|
| [2] |
李影, 刘红宁, 邓晓霞, 等. 试述羌活胜湿汤的临床应用现状[J]. 江西中医药大学学报, 2017, 29(3): 113-114, 124. |
| [3] |
张鹏, 刘安, 邬兰, 等. 经典名方概述与开发探讨[J]. 中国实验方剂学杂志, 2020, 26(15): 183-194. |
| [4] |
国家药典委员会. 中华人民共和国药典[M]. 北京: 中国医药科技出版社, 2020: 42, 88, 156, 190, 274, 379, 397.
|
| [5] |
郭培, 郎拥军, 张国桃. 羌活化学成分及药理活性研究进展[J]. 中成药, 2019, 41(10): 2445-2459. |
| [6] |
马丽梅, 杨军丽. 羌活药材的化学成分和药理活性研究进展[J]. 中草药, 2021, 52(19): 6111-6120. |
| [7] |
WANG Q, ZHOU X, YANG L, et al. The natural compound notopterol binds and targets JAK2/3 to ameliorate inflammation and arthritis[J]. Cell Reports, 2020, 32(11): 108-128. |
| [8] |
WU S B, PANG F, WEN Y, et al. Antiproliferative and apoptotic activities of linear furocoumarins from Notopterygium incisum on cancer cell lines[J]. Planta Medica, 2010, 76(1): 82-85. DOI:10.1055/s-0029-1185971 |
| [9] |
OUYANG J Y, JIANG H J, FANG H, et al. Isoimperatorin ameliorates osteoarthritis by downregulating the mammalian target of rapamycin C1 signaling pathway[J]. Molecular Medicine Reports, 2017, 16(6): 9636-9644. DOI:10.3892/mmr.2017.7777 |
| [10] |
LIU J, HE L, HU J, et al. Isoimperatorin induces apoptosis of nasopharyngeal carcinoma cells via the MAPK/ERK1/2 signaling pathway[J]. Evidence-Based Complementary and Alternative Medicine, 2020, 20(11): 213-218. |
| [11] |
LAI Y N, HAN T T, ZHAN S F, et al. Antiviral activity of isoimperatorin against influenza A virus in vitro and its inhibition of neuraminidase[J]. Frontiers in Pharmacology, 2021, 12(3): 657-667. |
| [12] |
周璐丽, 曾建国. 独活化学成分及药理活性研究进展[J]. 中国现代中药, 2019, 21(12): 1739-1748. |
| [13] |
曹思思, 史磊, 孙佳琳, 等. 防风的化学成分及药理作用研究进展[J]. 现代中药研究与实践, 2021, 35(1): 95-102. |
| [14] |
邓桃妹, 彭灿, 彭代银, 等. 甘草化学成分和药理作用研究进展及质量标志物的探讨[J]. 中国中药杂志, 2021, 46(11): 2660-2676. |
| [15] |
田华, 杜婷, 黄开合, 等. 蔓荆子的药理作用研究进展[J]. 中国医药导报, 2013, 10(9): 29-30. |
| [16] |
官扬, 胡慧明, 潘婷, 等. 蔓荆子的药理作用及其临床应用研究进展[J]. 江西中医药, 2013, 44(4): 72-73. |
| [17] |
张晓娟, 张燕丽, 左冬冬. 川芎的化学成分和药理作用研究进展[J]. 中医药信息, 2020, 37(6): 128-133. |
| [18] |
李兴博, 齐耀东, 刘海涛, 等. 新疆藁本化学成分的研究[J]. 中国中药杂志, 2013, 38(10): 1543-1547. |
| [19] |
黄仕文, 颜媛媛, 嵇晶, 等. 经典名方质量研究及其量值传递关键技术[J]. 南京中医药大学学报, 2021, 37(3): 446-449. |
 2024, Vol. 43
2024, Vol. 43