文章信息
- 夏宁, 张孝莹, 成丽媛, 张玥, 周昆
- XIA Ning, ZHANG Xiaoying, CHENG Liyuan, ZHANG Yue, ZHOU Kun
- UHPLC-MS/MS法同时测定补骨脂药材中17种成分的含量
- Simultaneous quantification of 17 components in psoraleae fructus by UHPLC-MS/MS method
- 天津中医药大学学报, 2024, 43(11): 971-977
- Journal of Tianjin University of Traditional Chinese Medicine, 2024, 43(11): 971-977
- http://dx.doi.org/10.11656/j.issn.1673-9043.2024.11.03
-
文章历史
收稿日期: 2024-05-02
2. 天津中医药大学中医药研究院, 天津 301617;
3. 省部共建组分中药国家重点实验室, 天津 301617
2. Institute of Traditional Chinese Medicine, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China;
3. State Key Laboratory of Component-based Chinese Medicine, Tianjin 301617, China
补骨脂(Psoraleae Fructus,PF) 是豆科植物补骨脂(Psoraleacorylifolia L.)的干燥成熟果实,具有温肾助阳、温脾止泻等功效[1],临床上常用于治疗因肾阳不足引起的骨质疏松症[2]。目前已经从补骨脂中分离鉴定了90余种化合物[3],其主要活性成分包括香豆素类、黄酮类和单萜酚类[4]。作为一种广泛分布的物种,补骨脂的种植遍布全球,其药材来源不仅包括中国的四川、广西等地,在国际市场上,如缅甸、越南等国家的进口药材也占有一定比例[5]。由于环境等因素的差异性,不同来源的补骨脂药材中活性成分的含量存在显著差异。目前对补骨脂药材的研究多集中于化学成分及药理活性,对其质量控制的研究报道相对较少。药材含量测定的主要方法是高效液相色谱法[6-8],所测定的成分也主要针对补骨脂素、异补骨脂素[9-10]等少数成分,具有局限性。
因此,本研究采用超高效液相色谱串联质谱(UHPLC-MS/MS)技术,以不同产地,不同批次的补骨脂药材为研究对象,同时测定补骨脂药材中补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮和Corylifol A 17种成分的含量,并结合聚类方法进行差异分析,旨在揭示不同批次补骨脂药材中各成分含量的差异性,为进一步的质量控制和药效评价提供科学依据。
1 仪器与试药 1.1 仪器三重四极杆串联质谱仪AB 4500 Qtrap,超高效液相ExionLC(美国AB SCIEX);Vortex-Genie2涡旋仪(美国Scientific Industries);LEGED MICRO 21 R低温高速离心机(美国Thermo);MS 205 DU电子分析天平(瑞士METTLER TOLEDO);低温离心浓缩仪(日本EYELA);UC-6100超声清洗仪(Ameritech Scientific);超纯水机(美国Millipore)。
1.2 试药25批次不同产地的补骨脂药材,购自河北光明饮片有限公司,信息详见表 1。由天津中医药大学李天祥教授鉴定为补骨脂。对照品补骨脂素、异补骨脂素、补骨脂酚、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、Corylifol A,均购自成都普菲德生物技术有限公司;补骨脂二氢黄酮甲醚、补骨脂宁,均购自大连美仑生物技术有限公司;5-甲氧基补骨脂素购自美国Sigma-Aldrich试剂公司;4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮和巴库查尔酮,均由河南大学康文艺教授课题组提供;以上对照品纯度均≥98.0%。甲醇(色谱纯),购自德国Merck公司;乙腈(色谱纯),购自德国Merck公司;异丙醇(色谱纯),购自美国Thermo Fisher公司。
采用Thermo Fisher Scientific Hypersil GOLD C18色谱柱(2.1×100 mm,1.9 μm),以水(A)-乙腈(B)为流动相,梯度洗脱(0~2 min,5%~12% B;2~3 min,12%~24% B;3~7 min,24%~32% B;7~9 min,32% B;9~11 min,32%~58% B;11~15 min,58%~78% B;15~16 min,78% B;16~16.1 min,78%~5% B;16.1~20 min,5% B),流速0.2 mL·min-1,柱温40 ℃,进样量3.0 μL。
2.1.2 质谱条件离子源为电喷雾离子源(ESI),质谱多反应检测(MRM)模式及正负离子快速切换模式;气帘气、离子源GasⅠ、加热器GasⅡ均为N2,压力分别为10、40、50 psi;喷射源电压分别为4500 V和-4500 V;离子源温度为500℃。17种成分的母离子、子离子的m/z、去簇电压(DP)和碰撞能量(CE)详见表 2。
分别精密称取17种对照品适量,用甲醇溶解定容,得到质量浓度为1.0 mg/mL的对照品储备液,4 ℃储存备用。
2.2.2 供试品溶液的制备取补骨脂药材粉末(过三号筛)约0.25 g,精密称定,置于25 mL量瓶中,加入体积分数为60%的甲醇至刻度,密封后称重,超声提取45 min后,放冷至室温,再次称重,用甲醇补足减失的重量,摇匀,于0.22 μm滤膜滤过,即得供试品溶液。共计25批,4 ℃储存备用。
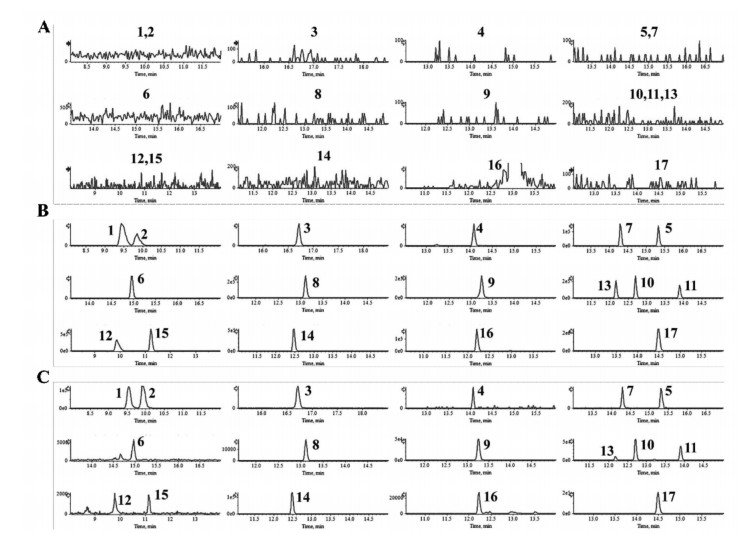
2.3 方法学考察 2.3.1 专属性精密吸取甲醇(空白溶液)、混合对照品溶液和补骨脂供试品溶液(S5)各100 μL,按“2.1.1”项和“2.1.2”项下的条件进样检测,分别得到甲醇(空白溶液)、混合对照品溶液和补骨脂供试品溶液的色谱图,见图 1,经考察,各成分在相应保留时间内无干扰,即空白溶剂对供试品溶液测试不存在干扰,表明所建立的方法专属性良好。
|
| 注:A,空白甲醇(Blank methanol)色谱图;B,混合对照品溶液(Mixed control solution)色谱图C,补骨脂供试品溶液(Test solution of PF)色谱图;1,补骨脂素;2,异补骨脂素;3,补骨脂酚;4,4,5-去氢异补骨脂定;5,补骨脂查尔酮;6,异补骨脂色烯查尔酮;7,补骨脂二氢黄酮甲醚;8,补骨脂宁;9,补骨脂定;10,补骨脂甲素;11,补骨脂乙素;12,8-甲氧基补骨脂素;13,异补骨脂二氢黄酮;14,新补骨脂异黄酮;15,5-甲氧基补骨脂素;16,巴库查尔酮;17,Corylifol A 图 1 补骨脂药材专属性色谱图 |
精密吸取“2.2.1”项下各成分的系列工作液各50 μL混匀,得到17种成分均在内的一系列混合工作液,即混合标曲溶液。精密吸取各浓度混合标曲溶液各100 μL,在“2.1.1”项和“2.1.2”项下的条件进样检测。以色谱峰峰面积为纵坐标(y),对照品浓度为横坐标(x),权重系数设为1/x2,以各成分与其周围基线噪音的比值(S/N)计算出检测限(LOD,S/N=3)和定量下限(LLOQ,S/N=10),计算各成分标准曲线方程。结果显示,17种成分在相应线性范围内线性关系良好(r≥0.991),各成分的线性方程,相关系数,线性范围及定量下限详见表 3。
精密吸取供试品溶液(S5) 100 μL,在“2.1.1”项和“2.1.2”项下的条件连续进样6次,记录各成分峰面积,计算RSD值。补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮、Corylifol A的RSD值(n=6) 分别为1.34%、0.36%、0.38%、1.35%、0.37%、1.22%、0.43%、0.64%、1.64%、0.84%、2.03%、0.00%、0.41%、1.05%、0.00%、0.87%、1.06%。表明该方法精密度良好。
2.3.4 重复性考查取同一批次(S5)补骨脂药材,依据“2.2.2”所述方法,平行制备6份,按“2.1.1”项和“2.1.2”项下的条件进样检测,记录各成分峰面积,计算RSD值。补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮、Corylifol A的RSD值(n=6)分别为0.96%、1.15%、0.34%、0.90%、0.43%、0.44%、0.87%、0.78%、0.87%、1.32%、1.28%、1.12%、1.31%、0.61%、0.79%、0.77%、1.12%。表明所建立的方法重复性良好。
2.3.5 稳定性考察取同一批次(S5)补骨脂药材,依据“2.2.2”所述方法,平行制备6份,按“2.1.1”项和“2.1.2”项下的条件,分别在样品处理完毕的第0、6、24 h进样检测,记录各成分峰面积,计算样品在不同时间的RSD值。补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮、Corylifol A的RSD值范围(n=6) 分别为0.3%~0.8%、0.54%~1.12%、0.37%~2.14%、0.68%~2.2%、0.22%~0.67%、0.41%~2.04%、0.41%~1.38%、0.33%~1.38%、1.91%~2.5%、0.79%~1.69%、0.37%~1.79%、1.07%~1.97%、0.41%~2.57%、0.64%~0.72%、1.73%~2.21%、0.48%~1.66%、0.63%~1.67%。表明补骨脂供试品溶液在24 h内稳定性良好。
2.3.6 加样回收率考察精密称取同一批次(S5)已知含量的样品6份,每份0.25g,精密加入等量已知浓度的对照品溶液,按“2.2.2”项下方法制备供试品溶液,在“2.1.1”项和“2.1.2”项条件下进样测定,计算各成分的加样回收率和RSD值。补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮、Corylifol A的平均加样回收率(n=6) 分别为99.09%、99.48%、99.63%、99.85%、100.28%、99.85%、100.36%、101.38%、98.99%、99.24%、99.25%、98.00%、98.44%、95.66%、100.37%、97.36%、99.72%。RSD值(n=6) 分别为1.67%、1.05%、1.40%、2.40%、1.01%、1.66%、0.77%、0.77%、3.04%、1.22%、1.08%、2.63%、1.24%、1.23%、1.79%、2.70%、2.39%。
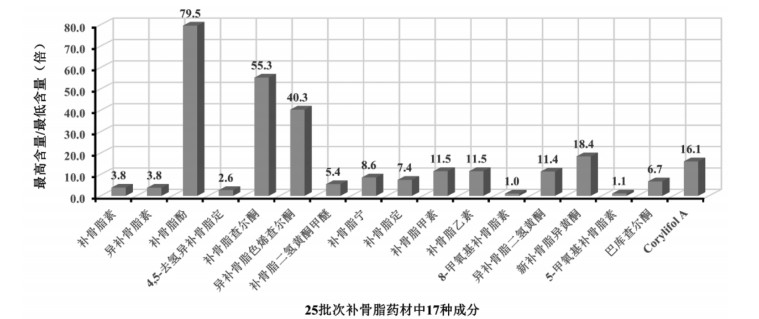
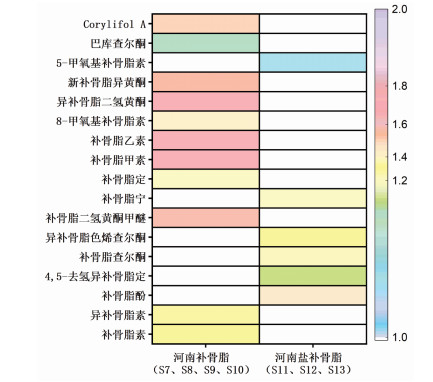
2.4 不同批次补骨脂中多成分的含量测定结果对25批次补骨脂药材中17种成分进行含量检测,结果以“均值(mean)”表示,详见表 4。根据检测结果,进一步统计17种成分在25批次药材中测得的最高含量与最低含量的倍数关系,而因为4,5-去氢异补骨脂定、8-甲氧基补骨脂素和5-甲氧基补骨脂素在某些批次中未被检测到,因此在统计时排除含量为0的结果。如图 2所示,补骨脂酚的含量差异最为显著,相差倍数最高,为79.5倍,其次为补骨脂查尔酮和异补骨脂色烯查尔酮(55.3倍)。通过热图对补骨脂炮制前后各成分含量的相对变化趋势进行展示,如图 3,发现炮制前后,补骨脂素和异补骨脂素含量降低,补骨脂酚含量升高。
|
| 图 2 25批次补骨脂药材中17种成分最高含量与最低含量的倍数比较 |
|
| 图 3 补骨脂药材炮制前后17种成分的含量相对变化 |
将25批次的药材中的17种成分的含量测定结果,通过Origin 2019统计软件进行系统聚类分析。如图 4,可以分为四类,第一类:S1,产自安徽,其成分含量相对较低,其中有11种成分相比其他批次均为最低。第二类:S4、S13、S6、S8、S9、S17,除S17为越南产地外,其余均为河南和河北产地。第三类:S2、21、15、20、18、22、23、14、3、7、19、12、5、10、11、24、16,产自广西、河北、河南、越南、四川、山西,展现了较大的多样性,但主要集中在南方地区。第四类:S25,产自新疆,具有独特性。

|
| 图 4 25批次补骨脂药材中17种成分的聚类分析 |
本研究成功建立了高效、简易、灵敏的UHPLC-MS/MS方法,可在20分钟内同时检测补骨脂药材中补骨脂素、异补骨脂素、补骨脂酚、4,5-去氢异补骨脂定、补骨脂查尔酮、异补骨脂色烯查尔酮、补骨脂二氢黄酮甲醚、补骨脂宁、补骨脂定、补骨脂甲素、补骨脂乙素、8-甲氧基补骨脂素、异补骨脂二氢黄酮、新补骨脂异黄酮、5-甲氧基补骨脂素、巴库查尔酮、Corylifol A 17种成分。经方法学验证,专属性、线性和定量下限、精密度、重复性、稳定性及加样回收率均符合标准,线性关系良好,相关系数r均大于0.99。
就产地来源分析来看,安徽S1批次的补骨脂多数成分含量低于其他产地;而进口于越南的补骨脂与来自新疆的补骨脂则显示出较高的成分含量。同种成分(如补骨脂酚)在不同产地之间的含量差异可达79.5倍。广西产地的S2批次中有3种成分未被检测到,而河北、河南产地的S4~S10批次中的17种成分均被检测到。进一步聚类分析发现越南产地的补骨脂差异较大。越南与中国广西、云南接壤,其地理环境和气候多样,具有明显的干湿两季变化[11],这可能是造成越南产地补骨脂成分含量差异的一个重要因素。值得注意的是,目前我国从越南进口的补骨脂多为野生采集[12]。野生药材的采集时间受到季节和气候等因素的影响,进而可能会导致药材品质的不稳定性。新疆产地的S25批次补骨脂中黄酮类成分和补骨脂酚含量明显高于其他批次。相关研究指出,紫外线辐射能够诱导植物体内酚类和黄酮类化合物的产生,新疆位于中国西部,紫外线辐射较强,因此不同产地的补骨脂药材在质量上可能存在显著差异,可能与气候、土壤和生长条件等因素有关,需进一步研究和监测。
盐制是补骨脂药材沿用至今的传统炮制方法,可缓和补骨脂的燥性。本研究发现,盐制后香豆素类化合物的含量略有降低;黄酮类化合物如补骨脂甲素、补骨脂乙素等也有所降低;而补骨脂酚的含量略有升高。这些变化与已有研究[13]的结果相似,可能与盐制过程中的高温作用导致香豆素类化合物开环以及种皮破碎使得活性成分更易于溶出有关[14]。而炮制后的一些活性成分含量降低,是否与“缓和燥性”有关,仍需深一步研究探讨。
香豆素类化合物补骨脂素和异补骨脂素,是补骨脂药材的指标性成分。25批次中,S17批次含量最高,S12批次含量最低。Corylifol A的含量相较于其他黄酮类成分更高,含量范围为4.6~73.5 mg/g,其次为补骨脂二氢黄酮甲醚,含量范围为5.0~27.1 mg/g。此外,单萜酚类化合物补骨脂酚的含量远高于其他成分,范围在5.8~460.6 mg/g。中医临床治疗讲究辨证论治,药物剂量的调整和药材批次间活性成分的差异,可能导致临床疗效的差异。鉴于补骨脂的肝毒性风险,其药效与安全性评估需谨慎对待,以确保临床用药的安全性。
综上所述,本研究成功建立了一种高效的UHPLC-MS/MS分析方法,全面定性和定量分析了补骨脂药材中的17种成分,揭示了不同产地补骨脂药材的质量差异,为补骨脂的质量控制提供了新的参考。
| [1] |
曹金一, 刘京晶, 黄文华, 等. 补骨脂药理作用与临床应用研究进展[J]. 中药药理与临床, 2008, 24(6): 89-92. |
| [2] |
ZHANG R, SHI W, LI L, et al. Biological activity and health promoting effects of psoralidin[J]. Die Pharmazie, 2019, 74(2): 67-72. |
| [3] |
ZHANG X N, ZHAO W W, WANG Y, et al. The chemical constituents and bioactivities of Psoralea corylifolia linn.: A review[J]. The American Journal of Chinese Medicine, 2016, 44(1): 35-60. DOI:10.1142/S0192415X16500038 |
| [4] |
张莹, 吕惠子. 补骨脂的化学成分和药理作用研究进展[J]. 临床医药文献电子杂志, 2020, 7(30): 195. |
| [5] |
王山, 孙莉, 吴杰, 等. 补骨脂全球适宜性区划研究[J]. 世界科学技术-中医药现代化, 2016, 18(8): 1272-1279. |
| [6] |
张彦东, 贾宜军, 王丽菊. 高效液相色谱法测定补骨脂中补骨脂素和异补骨脂素的含量[J]. 时珍国医国药, 2006, 17(8): 1465. |
| [7] |
赵陆华, 黄剑, 邹巧根, 等. 高效液相色谱法测定补骨脂中三种黄酮类成分的含量[J]. 中国药科大学学报, 2002, 33(2): 131-133. |
| [8] |
刘松青, 马文秀, 唐先哲, 等. 高效液相色谱法测定药材及中成药中补骨脂素与异补骨脂素含量[J]. 中草药, 1994, 25(7): 355-356, 358, 391. |
| [9] |
丁家欣, 张秋海, 张玲. 不同产地补骨脂中补骨脂素和异补骨脂素的含量测定[J]. 中药材, 2004, 27(11): 817-818. |
| [10] |
许勇, 李乐道, 熊志立, 等. 高效液相色谱法测定中药材补骨脂中补骨脂素和异补骨脂素的含量[J]. 色谱, 2003, 21(4): 385-387. |
| [11] |
彭伟, 罗勇军, 杨晓红. 越南医学地理特点及卫勤保障策略[J]. 国外医学(医学地理分册), 2016, 37(4): 295-297. |
| [12] |
张亚中, 刘军玲, 程世云, 等. 补骨脂药材的质量变化规律和标准探讨[J]. 中国现代中药, 2022, 24(2): 294-297. |
| [13] |
杨滨, 姚三桃, 崔淑莲. 补骨脂古今主要炮制方法的比较[J]. 中国中药杂志, 1996, 21(9): 25-27, 63. |
| [14] |
颜翠萍, 吴育, 翁泽斌, 等. 盐制对补骨脂中主要化学成分的影响[J]. 中成药, 2013, 35(11): 2470-2474. |
 2024, Vol. 43
2024, Vol. 43








