文章信息
- 朱征, 邹佳涵, 金鑫瑶, 赵霞, 王可仪, 张雅姿, 杨丰文
- ZHU Zheng, ZOU Jiahan, JIN Xinyao, ZHAO Xia, WANG Keyi, ZHANG Yazi, YANG Fengwen
- 金芪降糖片治疗2型糖尿病改善胰岛功能的系统评价
- Jinqi Jiangtang tablets improve islet function in the treatment of type 2 diabetes mellitus: a systematic review
- 天津中医药大学学报, 2024, 43(2): 150-159
- Journal of Tianjin University of Traditional Chinese Medicine, 2024, 43(2): 150-159
- http://dx.doi.org/10.11656/j.issn.1673-9043.2024.02.09
-
文章历史
收稿日期: 2023-10-09
2. 天津市滨海新区中医医院, 天津 300450;
3. 天津中医药大学循证医学中心, 天津 301617;
4. 河北省中医院, 石家庄 050000
2. Binhai New Area Hospital of Traditional Chinese Medicine, Tianjin, Tianjin 300450, China;
3. Evidence-based Medicine Center, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China;
4. Hebei Provincial Hospital of Traditional Chinese Medicine, Shijiazhuang 050000, China
糖尿病是胰岛素的产生与作用障碍,以代谢状态紊乱为主要表现的慢性代谢性疾病[1]。2021年国际糖尿病联盟(IDF)发布的《全球糖尿病地图》显示,截至2021年全球成年糖尿病患者数为5.37亿,到2045年患者人数预计将达到7.84亿[2]。中国过去10年间(2011—2021年),糖尿病患者人数由9000万增加至1亿4 000万,增幅达56%。预计2030年糖尿病患病总数将增加至1.64亿,2045年将增加至1.75亿[2]。中国2型糖尿病患者约占所有糖尿病患者的90%以上[1],其发病机制主要包括胰岛β细胞功能异常和胰岛素抵抗[3]。2型糖尿病的早期治疗以口服降糖药为主,多基于纠正导致人类血糖升高的两个主要病理生理改变,即胰岛素抵抗和胰岛素分泌受损。口服降糖药可分为主要以促进胰岛素分泌为主要作用的药物和通过其他机制降低血糖的药物,前者主要包括磺脲类、格列奈类、二肽基肽酶Ⅳ抑制剂(DPP-4i),而通过其他机制降低血糖的药物主要包括双胍类、噻唑烷二酮类(TZDs)等[4]。其中磺脲类(SUs)的主要作用机制为刺激胰岛β细胞分泌胰岛素;噻唑烷二酮类(TZDs)被称为胰岛素增敏剂,可明显减轻胰岛素抵抗;双胍类降糖药可抑制肝葡萄糖输出、改善外周组织对胰岛素的敏感性[5]。2型糖尿病患者口服降糖药物失效或有禁忌症时,则需考虑使用胰岛素制剂[2]。虽然现有西药降糖作用确切,但在改善胰岛抵抗方面仍面临很多困境。
金芪降糖片是中国第一个通过《新药审批办法》的治疗糖尿病的新型中成药,其组成通过现代药理筛选评价产生,包括黄芪、金银花、黄连三味中药,具有清热益气的作用。现代研究显示金芪降糖片具有改善糖代谢、改善脂代谢、改善胰岛素抵抗及增强免疫功能的作用[6-7]。1995年中法联合设计的评价金芪降糖片与格列苯脲治疗2型糖尿病患者的多中心双盲临床观察,显示金芪降糖片与格列苯脲在降低血糖方面具有协同作用,并且安全性良好[8]。另一项金芪降糖片用于治疗糖尿病前期的有效性和安全性的多中心随机对照试验的注册研究,纳入患者400例,观察糖尿病的发病率,显示金芪降糖片与安慰剂对比可有效降低糖尿病发病率[9-10]。基础研究显示金芪降糖片含多种中药活性成分,其可通过糖脂代谢减轻高脂饲养小鼠胰岛素抵抗,通过激活AMPK信号通路增加胰岛素敏感性,进而增加胰岛β细胞功能[11-12],进一步研究发现金芪降糖片可清除氧自由基,抑制α葡萄糖苷酶、醛糖还原酶和脂肪酶[13]。金芪降糖片能否改善胰岛素抵抗、增加胰岛素敏感性,及与西药降糖药联用的安全性如何,尚需进一步研究。本研究对相关临床试验进行系统评价,以期为临床应用提供证据支持。
1 方法 1.1 纳入与排除标准 1.1.1 研究类型随机平行对照临床试验(RCTs),是否使用盲法不限。
1.1.2 研究对象2型糖尿病无严重并发症患者,年龄、病程不限。
1.1.3 干预措施试验组采用金芪降糖片或金芪降糖片联合降糖西药;对照组采用西医常规用药或安慰剂。
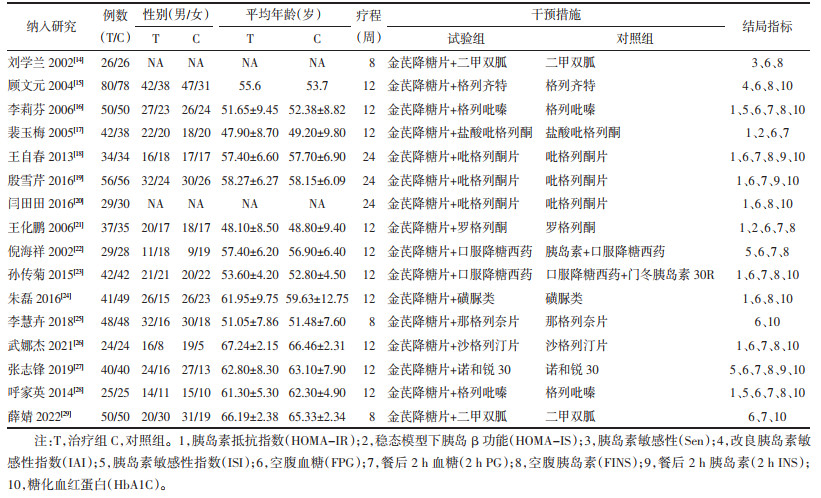
1.1.4 结局指标主要指标包括胰岛素抵抗指数(HOMA-IR)、稳态模型下胰岛β功能(HOMA-IS)、胰岛素敏感性(Sen)、改良胰岛素敏感性指数(IAI)、胰岛素敏感性指数(ISI);次要结局指标包括空腹血糖(FPG)、餐后2 h血糖(2 h PG)、空腹胰岛素(FINS)、餐后2 h胰岛素(2 h INS)、糖化血红蛋白(HbA1c)。
1.1.5 排除标准试验组或对照组使用金芪降糖片以外的其他中药;试验组与对照组基础用药不一致;重复发表的研究。
1.2 文献检索计算机检索CNKI、WanFang Data、SinoMed、PubMed、Embase、Cochrane library数据库,检索时间均从建库至2023年6月。以金芪降糖片、糖尿病、消渴等为主题词进行检索。
1.3 文献筛选及资料提取根据纳入排除标准,通过阅读标题和摘要对文献进行初筛,排除明显不相关文献。获取初筛文献后仔细阅读全文,确定最终纳入文献。由两位研究者独立进行文献筛选和资料提取,并进行交叉核对,如遇分歧,则讨论解决。重要数据缺失争取与原作者进行联系予以补充。
1.4 偏倚风险评价使用Cochrane Handbook 5.3.0推荐的偏倚风险评价工具评价纳入研究质量,从随机分配方法、分配方案隐藏、盲法、结果数据的完整性、选择性报告结果以及其他偏倚等六方面对纳入研究的偏倚风险进行评价。方法使用正确,评为“低风险”;方法使用错误,评为“高风险”;仅提及但未具体描述者评为“不明风险”。
1.5 统计分析采用RevMan 5.3.0软件进行统计分析。计量资料采用均数差(MD)及其95%CI为效应统计量,计数资料采用相对危险度(RR)及其95%CI为效应统计量。纳入研究结果间的异质性分析采用卡方检验(检验水准设为α=0.05),并结合I2定量判断异质性的大小。若各研究结果间统计学异质性较小(P>0.1,I2 < 50%),则采用固定效应模型合并效应量;若各研究结果间统计学异质性较大,则首先查找异质性来源,并根据异质性来源进行亚组分析及敏感性分析。
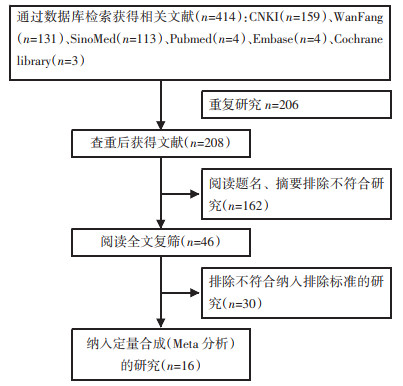
2 结果初检出相关文献414篇,排除重复文献206篇,经过阅读全文,符合纳入标准的文章共16篇。文献筛选流程及结果见图 1。
|
| 图 1 文献筛选流程图 |
研究对象:纳入的16个研究均为中国开展的研究,共纳入1306例2型糖尿病患者,其中试验组653例,对照组653例。
诊断标准:16个研究均报告了纳入和排除标准。1个研究的诊断标准参考1985年WHO糖尿病标准,1个研究参考1998年ADA制定的糖尿病诊断标准,1个研究参考1998年WHO糖尿病诊断标准,7个研究参考1999年WHO糖尿病诊断标准,1个研究提到参考WHO诊断标准未提及标准年份,1个研究参考2010年中华医学会糖尿病学分会制定的中国2型糖尿病防治指南,1个研究参考2013年中华医学会糖尿病学分会制定的中国2型糖尿病防治指南,1个研究参考2017年中华医学会糖尿病学分会制定的中国2型糖尿病防治指南,2个研究未明确所参考的诊断标准。
干预措施:16个研究均为金芪降糖片联合西药对比降糖西药,疗程最短为8周,最长为24周。
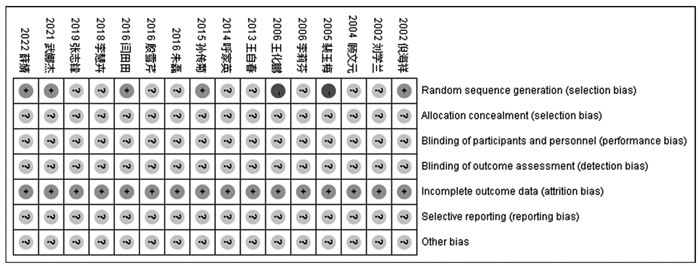
2.2 纳入研究的方法学质量纳入16个研究中所有试验均提到随机,其中2个试验按就诊顺序随机[16, 20],评为高风险,3个试验采用随机数字表法[19, 22, 28],1个试验采用投币法[21],1个试验采用抽签法[25],评为低风险,余9个试验未明确指出随机方法,评为不明风险;16个试验均未明确提出使用分配隐藏评为不明风险;16个试验均未明确提出盲法的使用,评为不明风险;16个试验均未提到结果评估采用盲法,评为不明风险;16个研究均有病例数据,评为低风险;16个研究均未注册研究方案,无法判断有无选择性报告,评为不明风险;16个研究无法判断其他偏倚来源,均评为不明风险。见图 2。
|
| 图 2 偏倚风险评估 |
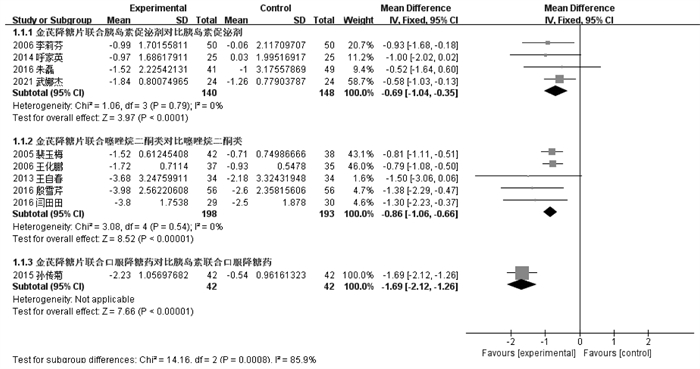
共10个RCT报告了治疗前后HOMA-IR的变化[16-21, 23-24, 26, 28]。根据对照组降糖药物种类进行亚组分析。结果提示金芪降糖片联合胰岛素促泌剂优于胰岛素促泌剂单用,组间比较差异有统计学意义[MD=-0.69,95%CI(-1.04,-0.35)]。在TZDs基础上加用金芪降糖片优于TZDs单用,组间比较差异有统计学意义[MD=-0.86,95%CI(-1.06,-0.66)]。金芪降糖片联合口服降糖药优于胰岛素联合口服降糖药,组间比较差异有统计学意义[MD=-1.69,95%CI(-2.12,-1.26)]。见图 3。
|
| 图 3 金芪降糖片治疗2型糖尿病HOMA-IR变化的Meta分析森林图 |
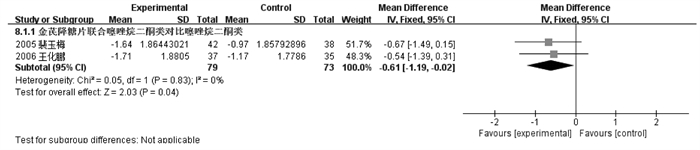
纳入2个RCT[17, 21]报告HOMA-IS,在TZDs基础上加用金芪降糖片优于TZDs单用,差异有统计学意义[MD=-0.61,95%CI(-1.99,-0.02)]。见图 4。
|
| 图 4 金芪降糖片治疗2型糖尿病HOMA-IS变化的Meta分析森林图 |
1个RCT[14]报告Sen,金芪降糖片联合二甲双胍优于单用二甲双胍,差异有统计学意义[MD=0.45,95%CI(0.19,0.71)]。1个RCT[15]报告IAI,金芪降糖片联合格列齐特优于单用格列齐特,组间比较差异有统计学意义[MD=2.00,95%CI(1.28,2.72)]。
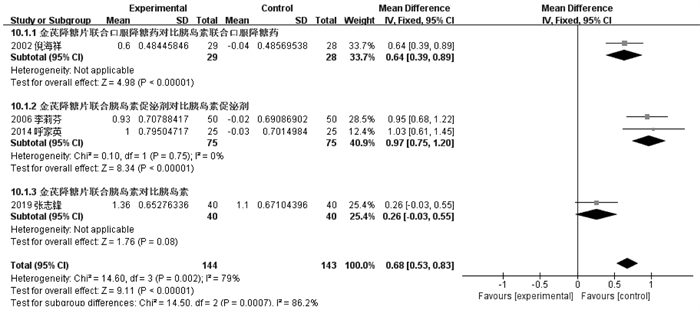
4个RCT[16, 22, 27-28]报告ISI,根据不同对照方案分亚组进行数据分析。金芪降糖片联合口服降糖药优于胰岛素联合口服降糖药,差异有统计学意义[MD=0.64,95%CI(0.39,0.89)]。金芪降糖片联合胰岛素促泌剂优于单用胰岛素促泌剂,组间比较差异有统计学意义[MD=0.97,95%CI(0.75,1.20)]。金芪降糖片联合胰岛素对比单用胰岛素,差异无统计学意义。见图 5。
|
| 图 5 金芪降糖片治疗2型糖尿病ISI变化的Meta分析森林图 |
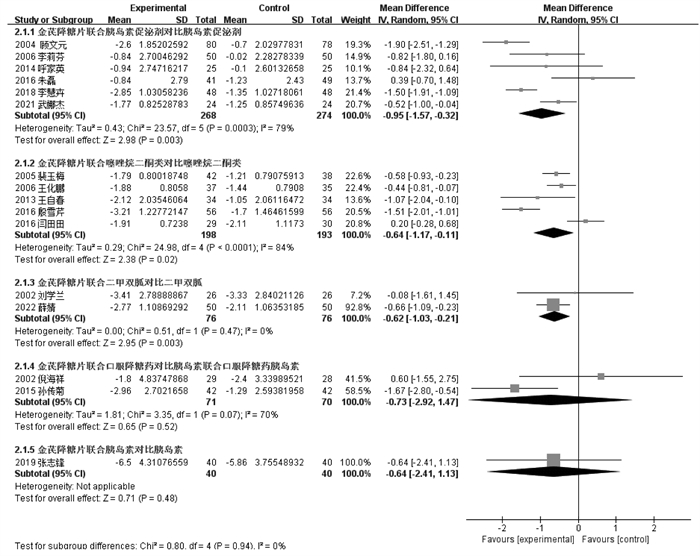
16个RCT[14-29]均报告了FPG,根据不同对照方案分亚组进行数据分析。金芪降糖片联用胰岛素促泌剂优于胰岛素促泌剂单用,差异有统计学意义[MD=-0.95,95%CI(-1.57,-0.32)]。金芪降糖片联用TZDs优于TZDs单用,差异有统计学意义[MD=-0.64,95%CI(-1.17,-0.11)]。金芪降糖片联合二甲双胍优于单用二甲双胍,组间差异有统计学意义[MD=-0.62,95%CI(-1.03,-0.21)]。金芪降糖联合口服降糖药与胰岛素联合口服降糖药比较,差异无统计学意义[MD=-0.73,95%CI(-2.92,1.47)]。金芪降糖联合胰岛素与胰岛素单用比较,差异无统计学意义[MD=-0.64,95%CI(-2.41,1.13)]。见图 6。
|
| 图 6 金芪降糖片治疗2型糖尿病FPG变化的Meta分析森林图 |
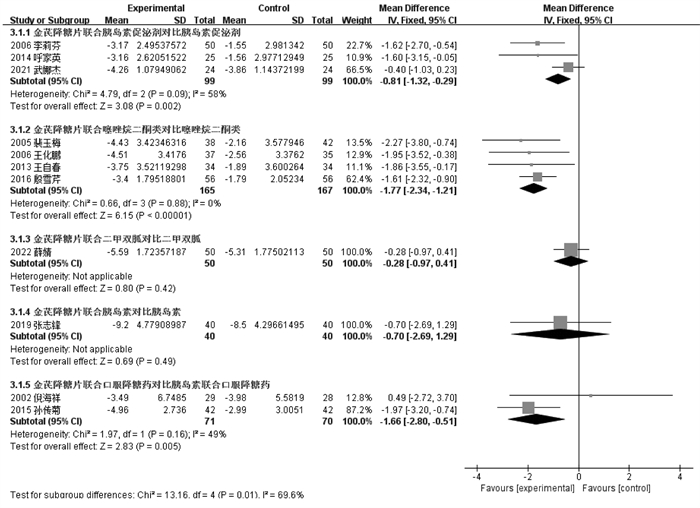
11个RCT[16-19, 21-23, 26-29]报告了2 h PG,根据不同对照方案分亚组进行数据分析。金芪降糖片联合胰岛素促泌剂优于胰岛素促泌剂单用,差异有统计学意义[MD=-0.81,95%CI(-1.32,-0.29)]。金芪降糖片联合TZDs优于TZDs单用,差异有统计学意义[MD=-1.77,95%CI(-2.34,-1.21)]。金芪降糖片联合二甲双胍与单用二甲双胍比较,差异无统计学意义[MD=-0.28,95%CI(-0.97,0.41)]。金芪降糖联合胰岛素与胰岛素单用比较,差异无统计学意义[MD=-0.70,95%CI(-2.69,1.29)]。金芪降糖片联合口服降糖药疗效优于胰岛素联合口服降糖药,组间比较有统计学意义[MD=-1.66,95%CI(-2.80,-0.51)]。见图 7。
|
| 图 7 金芪降糖片治疗2型糖尿病2hPG变化的Meta分析森林图 |
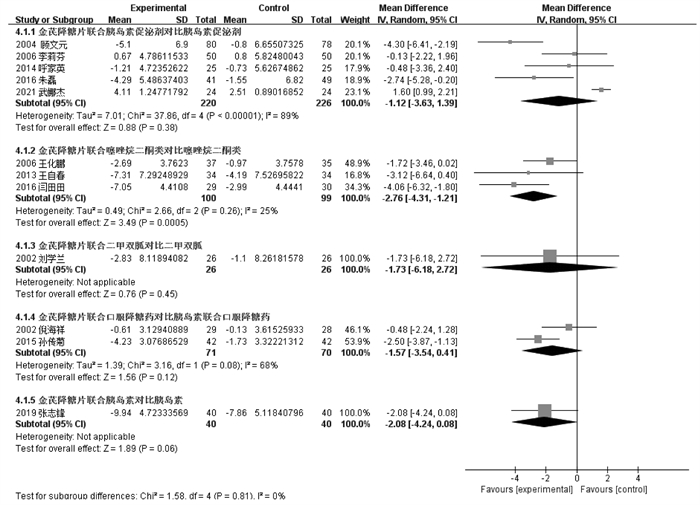
12个RCT报告FINS[14-16, 18, 20-24, 26-28],根据不同对照方案分亚组进行数据分析。金芪降糖片联合胰岛素促泌剂与胰岛素促泌剂单用比较,组间差异无统计学意义[MD=-1.12,95%CI(-3.63,1.39)]。金芪降糖片联合TZDs优于TZDs单用,组间差异有统计学意义[MD=-2.76,95%CI(-4.31,-1.21)]。金芪降糖片联合二甲双胍与二甲双胍单用比较,组间差异无统计学意义[MD=-1.73,95%CI(-6.18,2.72)]。金芪降糖片联合口服降糖药与胰岛素联合口服降糖药比较,组间差异无统计学意义[MD=-1.57,95%CI(-3.54,0.41)]。金芪降糖联合胰岛素与胰岛素单用比较,差异无统计学意义[MD=-2.08,95%CI(-4.24,0.08)]。见图 8。
|
| 图 8 金芪降糖片治疗2型糖尿病FINS变化的Meta分析森林图 |
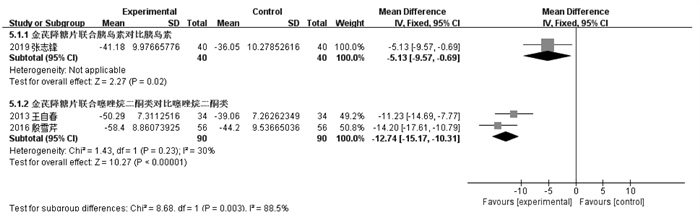
3个RCT报告了2 h INS[18-19, 27],根据不同对照方案分亚组进行数据分析。金芪降糖联合胰岛素疗效优于胰岛素单用,组间比较有统计学意义[MD=-5.13,95%CI(-9.57,-0.69)]。金芪降糖片联合TZDs疗效优于TZDs单用,组间比较有统计学意义[MD=-12.74,95%CI(-15.17,-10.31)]。见图 9。
|
| 图 9 金芪降糖片治疗2型糖尿病2 h INS变化的Meta分析森林图 |
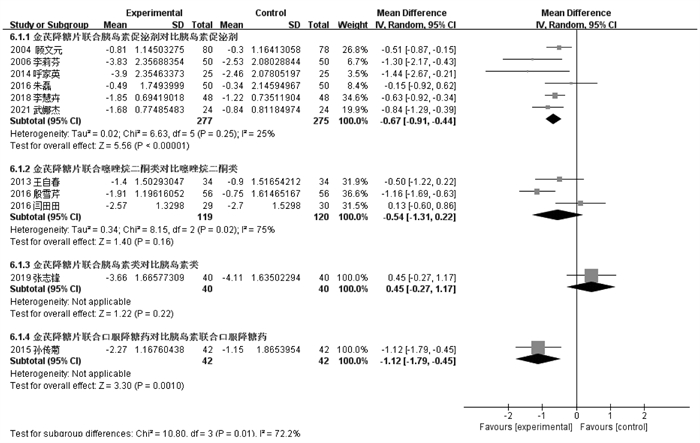
11个RCT报告了HbA1C[15-16, 18-20, 23-28],根据不同对照方案分亚组进行数据分析。金芪降糖片联用胰岛素促泌剂与单用胰岛素促泌剂比较,差异有统计学意义[MD=-0.67,95%CI(-0.91,-0.44)]。金芪降糖片联合TZDs与TZDs单用,组间比较差异无统计学意义[MD=-0.54,95%CI(-1.31,0.22)]。金芪降糖联合胰岛素对比胰岛素单用,组间差异无统计学意义[MD=0.45,95%CI(-0.27,1.17)]。金芪降糖片联合口服降糖药优于胰岛素联合口服降糖药,组间差异有统计学意义[MD=-1.12,95%CI(-1.79,-0.45)]。见图 10。
|
| 图 10 金芪降糖片治疗2型糖尿病HbA1C变化的Meta分析森林图 |
4个RCT报告了不良反应,金芪降糖片联合口服降糖药组(试验组)不良反应4例(4/653),不良反应包括轻度低血糖2例、胃肠道症状1例、皮疹1例。降糖西药组(对照组)报告不良反应23例(23/653),其中13例表现为低血糖,干预措施为口服降糖药或口服降糖药联合胰岛素;3例表现为胃肠道症状,干预措施为那格列奈片;3例表现为皮疹,干预措施为那格列奈片;2例不良反应表现为乏力,干预措施为那格列奈片;2例不良反应表现为轻度水肿,干预措施为吡格列酮片。未见单用金芪降糖片的不良反应报告,金芪降糖片与降糖西药联用,不增加低血糖不良反应的发生。
3 讨论 3.1 有效性安全性结果本研究结果显示,金芪降糖片联合胰岛素促泌剂与单用胰岛素促泌剂比较可改善HOMA-IR、增加胰岛素敏感性、降低FPG、2 h PG、HbA1C;金芪降糖片联合其他类降糖药,以TZDs为例,金芪降糖片联合TZDs与单用TZDs比较,可改善HOMA-IR、HOMA-IS,降低FPG、2 h PG、FINS、2 h INS。安全性方面,金芪降糖片组报告的不良反应较对照组少,为轻度低血糖、胃肠道症状、皮疹,且用药均为金芪降糖片联合降糖西药,金芪降糖片组未见对照组不良反应之外的不良反应表现。
糖尿病在中医属“消渴”范畴,其临床特点为阴虚为本,燥热为标,因此“消渴”的中医治疗多以滋阴补虚、清热益气,生津止渴为主[30]。金芪降糖片作为中成药制剂,其组方在清热同时重视补虚,益气同时生津止渴[31]。组方中的黄芪、黄连已通过基础研究表明具有改善胰岛素抵抗的作用[32],且黄连的主要成分小檗碱能促进诸如肝细胞、脂肪细胞等外周细胞对葡萄糖的摄取[33]。近年也有研究表明,金芪降糖片可促进胰岛素分泌,改善2糖尿病大鼠糖耐量异常,调节血脂功能,通过调控PPAR-α/FGF21信号通路增加胰岛素敏感性[34]。本研究的结果也从临床疗效上证实了金芪降糖片与口服降糖药联用在改善糖尿病患者的胰岛素抵抗、增加胰岛敏感、降血糖方面均可发挥协同作用。
3.2 本研究的局限性本研究的局限性如下:1)纳入研究存在偏倚风险,部分研究随机方法使用错误和未明确提出所使用的随机方法,未明确提出使用分配隐藏,存在选择性偏倚、实施偏倚的可能性。2)纳入研究诊断标准不一,存在采用诊断标准过于陈旧更新不及时的问题。3)研究随访时间短,未报告远期结局。
3.3 对未来研究的建议中医药治疗2型糖尿病改善胰岛功能具有较好的疗效和安全,但是尚需开展高质量的临床研究予以验证。进一步的临床研究应当注意:1)研究者应更加注重临床研究方法学学习和应用,规范临床研究方案设计,重视方案的提前注册,注重过程的质量控制,控制偏移风险。2)建议开展和实施设计严谨的多中心、大样本随机对照试验,为临床决策提供高质量研究证据。3)根据2型糖尿病疾病的特点,注重长疗程的随访,以便观察中药对2型糖尿病的长期疗效和安全性。
综上,金芪降糖片与降糖西药联用可治疗2型糖尿病改善胰岛功能且不增加不良反应。由于纳入文献的方法学质量低,样本量少,研究结果受多种偏倚影响,后续需要进一步开展严谨设计的多中心、大样本的高质量临床试验。
| [1] |
中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020年版)(上)[J]. 中国实用内科杂志, 2021, 41(8): 668-695. |
| [2] |
SUN H, SAEEDI P, KARURANGA S, et al. IDF Diabetes Atlas: Global, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045[J]. Diabetes Research and Clinical Practice, 2022, 183: 109119. DOI:10.1016/j.diabres.2021.109119 |
| [3] |
TANG Q, LI X Q, SONG P P, et al. Optimal cut-off values for the homeostasis model assessment of insulin resistance (HOMA-IR) and pre-diabetes screening: Developments in research and prospects for the future[J]. Drug Discoveries & Therapeutics, 2015, 9(6): 380-385. |
| [4] |
GARBER A J, ABRAHAMSON M J, BARZILAY J I, et al. Consensus statement by the American association of clinical endocrinologists and American college of endocrinology on the comprehensive type 2 diabetes management algorithm: 2016 executive summary[J]. Endocrine Practice, 2016, 22(1): 84-113. DOI:10.4158/EP151126.CS |
| [5] |
NATHAN D M, BUSE J B, DAVIDSON M B, et al. Medical management of hyperglycemia in type 2 diabetes: A consensus algorithm for the initiation and adjustment of therapy: A consensus statement of the American Diabetes Association and the European Association for the Study of Diabetes[J]. Diabetes Care, 2009, 32(1): 193-203. DOI:10.2337/dc08-9025 |
| [6] |
申竹芳. 金芪降糖片抗糖尿病的药理作用基础[J]. 国外医学内分泌学分册, 2004, 24(3): 215-216. |
| [7] |
陈家伦. 浅谈治疗糖尿病中药的研究与开发[J]. 国外医学内分泌学分册, 2004, 24(3): 150. |
| [8] |
VRAY M, ATTALI J R. Randomized study of glibenclamide versus traditional Chinese treatment in type 2 diabetic patients. Chinese-French Scientific Committee for the Study of Diabetes[J]. Diabete & Metabolisme, 1995, 21(6): 433-439. |
| [9] |
CAO H B, REN M, GUO L P, et al. JinQi-Jiangtang tablet, a Chinese patent medicine, for pre-diabetes: A randomized controlled trial[J]. Trials, 2010, 11: 27. DOI:10.1186/1745-6215-11-27 |
| [10] |
Xiao S, Guo L, Shang H, et al. The cost-effectiveness analysis of JinQi Jiangtang tablets for the treatment on prediabetes: a randomized, double-blind, placebo-controlled, multicenter design[J]. Trials, 2015, 16(1): 496. DOI:10.1186/s13063-015-0990-9 |
| [11] |
GAO L H, LIU Q, LIU S N, et al. A refined-JinQi-JiangTang tablet ameliorates prediabetes by reducing insulin resistance and improving beta cell function in mice[J]. Journal of Ethnopharmacology, 2014, 151(1): 675-685. DOI:10.1016/j.jep.2013.11.024 |
| [12] |
CHANG Y X, GE A H, YU X A, et al. Simultaneous determination of four phenolic acids and seven alkaloids in rat plasma after oral administration of traditional Chinese medicinal preparation Jinqi Jiangtang Tablet by LC-ESI-MS/MS[J]. Journal of Pharmaceutical and Biomedical Analysis, 2016, 117: 1-10. DOI:10.1016/j.jpba.2015.08.030 |
| [13] |
CHANG Y X, GE A H, DONNAPEE S, et al. The multi-targets integrated fingerprinting for screening anti-diabetic compounds from a Chinese medicine Jinqi Jiangtang Tablet[J]. Journal of Ethnopharmacology, 2015, 164: 210-222. DOI:10.1016/j.jep.2015.02.018 |
| [14] |
刘学兰, 刘红英. 金芪降糖片合二甲双胍对2型糖尿病胰岛素敏感性的影响[J]. 中医药学刊, 2002, 20(11): 142. |
| [15] |
顾文元. 金芪降糖片与格列齐特联合治疗2型糖尿病的临床观察[J]. 天津医科大学学报, 2004, 10(1): 87-89. |
| [16] |
李莉芬, 吴玉红. 金芪降糖片治疗2型糖尿病胰岛素抵抗患者的观察[J]. 天津医药, 2006, 34(9): 654-656. DOI:10.3969/j.issn.0253-9896.2006.09.027 |
| [17] |
裴玉梅, 田金莉, 张雅中, 等. 金芪降糖片对初发2型糖尿病胰岛功能的影响[J]. 天津医药, 2005, 33(5): 294-296. |
| [18] |
王自春, 王征. 金芪降糖片联合吡格列酮片治疗2型糖尿病高胰岛素血症的疗效观察[J]. 天津医药, 2013, 41(11): 1122-1123. |
| [19] |
殷雪芹. 金芪降糖片联合吡格列酮片治疗2型糖尿病高胰岛素血症的临床疗效[J]. 海峡药学, 2016, 28(2): 107-108. |
| [20] |
闫田田, 汤云昭, 李晨光, 等. 金芪降糖片联合吡格列酮对2型糖尿病胰岛素抵抗的研究[J]. 中国慢性病预防与控制, 2016, 24(8): 589-592. |
| [21] |
王化鹏. 金芪降糖片对初发轻中度2型糖尿病患者胰岛功能的影响[J]. 中国中西医结合杂志, 2006, 26(8): 709. DOI:10.3321/j.issn:1003-5370.2006.08.027 |
| [22] |
倪海祥, 罗苏生, 杨雪辉, 等. 金芪片对磺脲类降糖药物继发性失效的2型糖尿病疗效研究[J]. 中药新药与临床药理, 2002, 13(4): 208-209, 268. DOI:10.3321/j.issn:1003-9783.2002.04.004 |
| [23] |
孙传菊, 赵懿清, 曹宏. 金芪降糖片联合预混胰岛素治疗继发性磺脲类失效的2型糖尿病的疗效观察[J]. 中药材, 2015, 38(11): 2453-2455. |
| [24] |
朱磊. 金芪降糖片在2型糖尿病患者临床治疗中的意义[J]. 中国处方药, 2016, 14(11): 87-88. |
| [25] |
李慧卉. 金芪降糖片联合那格列奈治疗2型糖尿病的临床研究[J]. 现代药物与临床, 2018, 33(8): 2001-2004. |
| [26] |
武娜杰. 金芪降糖片联合沙格列汀片对老年2型糖尿病患者糖脂代谢及胰岛素抵抗的影响[J]. 黑龙江医学, 2021, 45(19): 2083-2084. DOI:10.3969/j.issn.1004-5775.2021.19.027 |
| [27] |
张志锋. 金芪降糖片联合预混胰岛素治疗继发性磺脲类失效的2型糖尿病的疗效观察[J]. 北方药学, 2019, 16(11): 17-19. |
| [28] |
呼家英, 汤建芬. 金芪降糖片治疗2型糖尿病胰岛素抵抗患者临床分析[J]. 大家健康(学术版), 2014, 8(4): 183. |
| [29] |
薛婧. 金芪降糖片治疗老年2型糖尿病患者的疗效[J]. 中国城乡企业卫生, 2022, 37(10): 131-133. |
| [30] |
张润云, 陈世波, 李云楚, 等. 2型糖尿病中医临床路径的医疗质量控制[J]. 北京中医药, 2018, 37(5): 398-400. |
| [31] |
丁美林, 董宏利, 江国荣, 等. 黄芩-黄连配伍治疗2型糖尿病的研究概述[J]. 中国药房, 2019, 30(17): 2440-2444. |
| [32] |
YEE Hong-yun, 杨晶晶, 万毅刚, 等. 胰岛素抵抗的分子机制及中药的干预作用[J]. 中国中药杂志, 2019, 44(7): 1289-1294. |
| [33] |
卢方晋, 丁丽琴, 曹世杰, 等. 调节糖脂代谢的苦味中药的化学及生物学研究[J]. 中国中药杂志, 2018, 43(19): 3834-3840. |
| [34] |
尹清晟, 范姗姗, 陈瑞, 等. 金芪降糖片联合胰岛素激活PPAR-α/FGF21信号改善2型糖尿病大鼠胰岛素抵抗[J]. 药物评价研究, 2018, 41(8): 1425-1429. |
 2024, Vol. 43
2024, Vol. 43