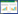文章信息
- 张怡博, 吴世豪, 李非凡, 等.
- ZHANG Yibo, WU Shihao, LI Feifan, et al.
- 基于豚鼠主动全身过敏实验和大鼠脑缺血再灌注炎症反应比较灯盏花素注射液和合成灯盏乙素注射液的安全性和有效性
- Comparison the safety and efficacy of Breviscapine Injection and Synthetic Scutellarin Injection based on active systemic anaphylaxis in Hartley guinea pigs and inflammatory response in cerebral ischemia-reperfusion rats
- 天津中医药, 2024, 41(11): 1423-1430
- Tianjin Journal of Traditional Chinese Medicine, 2024, 41(11): 1423-1430
- http://dx.doi.org/10.11656/j.issn.1672-1519.2024.11.12
-
文章历史
- 收稿日期: 2024-07-10
灯盏花素是从灯盏细辛Erigeron Breviscapus(vant.) Hand.-Mass.中提取的黄酮类化合物的混合物[1]。灯盏花素注射液是以灯盏花素为原料,应用现代制剂技术制成的注射用浓溶液[2]。其主要活性成分灯盏乙素含量达到98%[3],《中国药典》中也以灯盏乙素作为其质控指标[4]。
灯盏花素注射液(BI)用于治疗脑卒中具有疗效显著的优点[5]。药理研究表明[6-9],灯盏花素可改变大鼠脑中炎症细胞因子的含量,从而减少脑缺血的损伤,发挥脑保护作用。而灯盏花素注射液作为中药注射剂在临床用药中的不良反应也一直备受关注[10-12]。
近年来,由于过度开采使得灯盏细辛野生资源严重匮乏[13],阻碍灯盏乙素种源的筛选[14]。本实验通过考察BI和合成灯盏乙素注射液(SSI)主动全身过敏反应和对脑缺血再灌注损伤炎症因子的影响,比较两者的安全性和抗炎疗效,旨在通过合成灯盏乙素的方式缓解药材资源不足的问题,为临床用药提供依据。
1 材料与方法 1.1 实验动物SPF级健康雄性Hartley豚鼠,体质量(300±10) g,由北京维通利华实验动物技术有限公司提供,生产许可证号为SCXK(京)2021-0011;SPF级健康雄性SD大鼠,体质量(280±20) g,由斯贝福(北京)生物技术有限公司提供,生产许可证号为SCXK(京)2019-0010,均饲养于天津中医药大学实验动物中心。
1.2 实验药物灯盏花素注射液(石药银湖制药有限公司,规格5 mL: 20 mg,批号10121070711);合成灯盏乙素(中国科学院天津工业生物技术研究所提供,纯度:99%);尼莫地平注射液(辰欣药业股份有限公司,规格50 mL: 10 mg,国药准字H20059048);氯化钠注射液(石家庄四药有限公司,规格500 mL: 4.5 g,国药准字H13023200)。
1.3 主要试剂及仪器三溴乙醇(Sigma公司,批号T48402),异氟烷(深圳市瑞沃德生命科技公司,批号21120401),大鼠肿瘤坏死因子-α(TNF-α)、细胞间黏附分子-1(ICAM-1)、白细胞介素-6(IL-6)、白细胞介素-1β(IL-1β)和白细胞介素-10(IL-10)酶联免疫吸附测定(ELISA)试剂盒(泉州市睿信生物科技有限公司,批号RX302058R、RX302262R、RX302856R、RX302869R、RX302880R),A5线栓(北京西浓科技有限公司),异氟烷麻醉机(深圳市瑞沃德生命科技公司),Spark多功能酶标仪(瑞士Tecan公司),低速台式离心机(湖南湘仪实验室仪器开发有限公司),电子天平(余姚市金诺天平仪器有限公司)。
2 方法 2.1 豚鼠主动全身过敏实验 2.1.1 给药剂量换算及药物配制灯盏花素注射液成人每日最大注射剂量为20 mg/kg,按体表面积和人与动物临床剂量倍数直接换算,豚鼠的给药剂量约为1 mg/kg。本实验选取豚鼠等效剂量的5倍和20倍作为致敏阶段的低、高剂量组,即5 mg/kg、20 mg/kg。激发剂量均为致敏剂量的2倍,即10 mg/kg、40 mg/kg。阳性对照组致敏阶段给予牛血清白蛋白5 mg/kg,激发阶段给予10 mg/kg。
合成灯盏乙素注射液经天津中医药大学制剂中心按照灯盏花素注射液制备工艺配制(5 mL: 20 mg)。
2.1.2 动物分组及给药将36只健康雄性豚鼠随机分为6组,分别为阴性对照组(氯化钠注射液)、阳性对照组(牛血清白蛋白)、BI低剂量(BI-L)组、BI高剂量(BI-H)组、SSI低剂量(SSI-L)组、SSI高剂量(SSI-H)组,每组6只。
致敏阶段,对各组别腹腔注射相应剂量的药物,隔日1次,共3次。阴性对照组和阳性对照组给药方法和给药体积同受试药物组。激发阶段,末次给药后第12天静脉注射激发1次,激发剂量分别为致敏剂量的2倍。
2.1.3 观察指标和结果判定致敏期间,每日观察豚鼠症状。初次、末次致敏和激发前称体质量。激发后按表 1观察每只动物反应症状,症状出现及消失时间。一般观察3 h。之后判断过敏反应发生程度并计算过敏反应发生率。根据过敏反应发生率和发生程度进行综合判断。
灯盏花素注射液成人最大注射剂量为20 mg/(kg·d),参照《药理实验方法学》[15]人和动物的体表面积计算法换算,大鼠给药剂量为2.1 mg/(kg·d);高剂量组以成人剂量的2倍进行递增,即4.2 mg(kg·d)。尼莫地平注射液成人最大注射剂量为10 mg/(kg·d),换算后大鼠给药剂量为1 mg/(kg·d)。
2.2.2 动物分组及给药将144只健康雄性SD大鼠随机分成假手术组、模型组、尼莫地平组[1 mg/(kg·d)]、BI-L组[2.1 mg/(kg·d)]、BI-H组[4.2 mg/(kg·d)]、SSI-L组[2.1 mg/(kg·d)]、SSI-H组[4.2 mg/(kg·d)],共7组,每组24只。各给药组腹腔注射相应药物,假手术组和模型组腹腔注射等量的生理盐水,分别连续给药1、3、7和14 d,每日1次。
2.2.3 大鼠大脑中动脉(MCAO)闭塞的脑缺血再灌注模型制备采用改良longa-Zea氏线栓法[16]制备大脑中动脉脑缺血再灌注大鼠模型。操作如下:造模前禁食禁水12 h,通过异氟烷气体麻醉大鼠,将颈部正中备皮去毛,消毒后行纵向切口,眼科镊钝性分离皮下筋膜及颈前带状肌肉,充分暴露右侧颈总动脉并用玻璃分针分开附着的迷走神经,沿动脉继续向颅内方向探查颈内动脉和颈外动脉,将颈总动脉近心端结扎并用止血钳牵拉固定,继续于颈内动脉、颈外动脉分叉处系活结并牵拉固定,眼科角膜剪于牵拉起的颈总动脉作约0.2 mm开口,夹住线栓尾端向前推约18~22 mm经颈内动脉、颈外动脉分叉处沿颈内动脉入颅,后结扎线栓与分叉底部,行连续缝合。1.5 h后拔出线栓,行间断缝合。缺血1.5 h后,拔出线栓再灌注。假手术组只分离、暴露血管,不插入栓线,其余步骤同模型组。
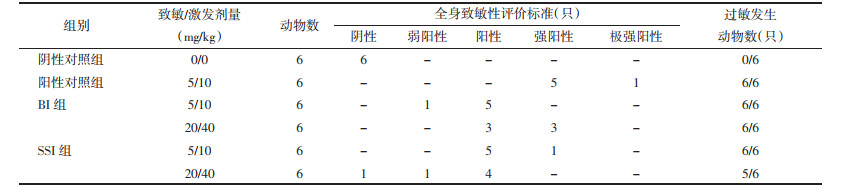
2.2.4 神经功能评分大鼠造模苏醒后2 h及给药1、3、7、14 d后参照Longa评分法[16],按照表 2标准对大鼠进行神经功能评分。
在给药1、3、7、14 d后各组随机取3只大鼠,给予3%三溴乙醇(7.5 mL/kg)麻醉,经腹主动脉取血后,用0.9%氯化钠溶液进行心脏灌注,灌注后血流干净便迅速取出大鼠全脑,放入培养皿置于-80 ℃冰箱快速冷冻,全脑冷冻质地便于切片后取出。刀片去除嗅球后,沿冠状面将其均匀切成5或6片,每片厚约2 mm。将切片置于盛有1 mL 2%TTC溶液的24孔板中,水平摇床37 ℃避光孵育10 min,回收TTC溶液,加入10%组织固定液孵育24 h后,排列整齐,使用相机采集图像,Image J软件分析大鼠脑部梗死面积,计算梗死面积百分比。梗死面积百分比(%)计算公式如下:[左侧半球面积-(右侧半球面积-梗死面积)]/全脑面积×100%。
2.2.6 血浆炎症因子测定将全血4 000 r/min离心20 min(离心半径17.0 cm),取上清,于-80 ℃保存备用。按照ELISA试剂盒说明书检测各组血清中TNF-α、ICAM-1、IL-6、IL-1β和IL-10含量。
2.3 统计学方法实验数据以均数±标准差(x±s)表示,应用SPSS 23.0统计软件分析。同一指标组间比较采用单因素方差分析,组间多重比较方差齐时采用LDS检验,方差不齐采用Dunnetts T3检验。P < 0.05表示具有统计学意义。
3 结果 3.1 豚鼠主动全身过敏实验阴性(生理盐水)对照组均未出现明显异常和过敏体征。阳性(牛血清白蛋白)对照组在激发后10 min内均出现了不同程度的过敏反应,其症状包括不安宁、搔鼻、喷嚏、咳嗽、排尿、排粪、呼吸困难、步态不稳、跳跃、喘息、痉挛、旋转、潮式呼吸和死亡。
BI低剂量组(5 mg/kg)豚鼠在激发后10 min内,1只出现不安宁症状,5只出现不同程度的不安宁、搔鼻、排尿、排粪症状。BI高剂量组(20 mg/kg)豚鼠在激发后10 min内,3只出现不安宁、搔鼻、排尿、排粪、哮鸣音,3只出现不安宁、搔鼻、喷嚏、排尿、排粪。
SSI低剂量组(5 mg/kg)豚鼠在激发后10 min内,5只出现不同程度的不安宁、搔鼻、喷嚏、排尿和排粪,1只出现不安宁、搔鼻、喷嚏、排粪和哮鸣音。SSI高剂量组(20 mg/kg)在激发后10 min内,4只出现搔鼻、排尿、排粪,1只出现搔鼻,1只未发生明显过敏反应症状。
除1只豚鼠死亡,其他豚鼠均在30~45 min内基本恢复过敏反应症状。过敏反应发生程度和过敏反应发生率如表 3所示。
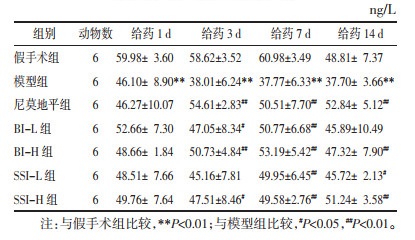
术后2 h,与假手术组比较,模型组评分均显著提高(P < 0.01),提示模型建立成功。给药1、3 d后,各给药组评分较模型组有所下降(P > 0.05);给药7、14 d后,各给药组评分较模型组均显著降低(P < 0.01)。见表 4。
比较灯盏花素注射液和合成灯盏乙素注射液对大鼠神经功能评分的影响,给药1 d,SSI-H组<SSI-L组=BI-H组<BI-L组;给药3 d,SSI-H组<SSI-L组<BI-H组=BI-L组;给药7 d,SSI-H组<BI-H组<SSI-L组=BI-L组;给药14 d,BI-H组=BI-L组=SSI-H组=SSI-L组。
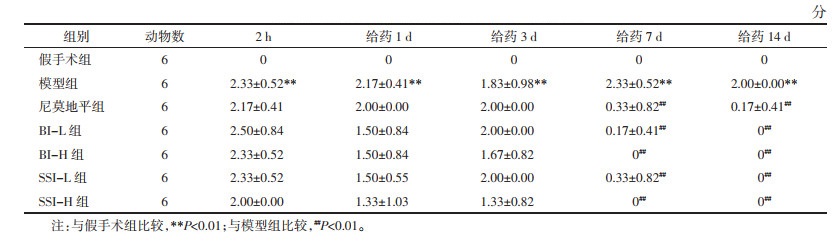
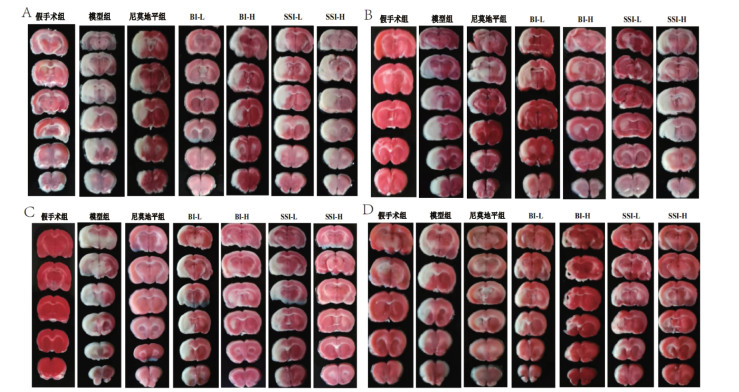
3.2.2 对各时间点大鼠脑梗死体积的影响与假手术组比较,给药1、3、7、14 d,模型组大鼠缺血侧脑梗死体积明显增加(P < 0.01);与模型组相比,给药1 d,BI-L组脑梗死体积显著减小(P<0.01);给药3 d,尼莫地平组脑梗死体积显著减小(P<0.01);给药7 d,SSI-L组和SSI-H组脑梗死体积显著减小(P<0.05或P<0.01);给药14 d,尼莫地平组、BI-L组和SSI-H组脑梗死体积显著减小(P<0.05或P<0.01)。见表 5,图 1。
|
| 注:A,给药1 d;B,给药3 d;C,给药7 d;D,给药14 d。 图 1 各时间点大鼠脑梗死体积情况 Fig. 1 Cerebral infarction of rats at different time points |
比较灯盏花素注射液和合成灯盏乙素注射液对大鼠脑梗死体积的影响,给药1 d,BI-L组<SSI-H组<SSI-L组<BI-H组;给药3 d,SSI-L组<BI-H组<BI-L组<SSI-H组;给药7 d,SSI-H组<SSI-L组<BI-L组<BI-H组;给药14 d,BI-L组<SSI-H组<SSI-L组<BI-H组。
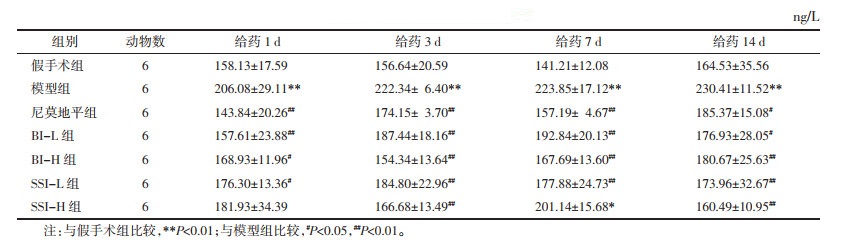
3.2.3 对各时间点大鼠血清TNF-α含量的影响与假手术组比较,给药1、3、7、14 d,模型组TNF-α含量均显著增加(P<0.01)。与模型组比较,给药1 d,SSI-H组TNF-α含量有所降低,其他各给药组TNF-α含量均显著降低(P<0.05或P<0.01);给药3、7、14 d,各给药组TNF-α含量均显著降低(P<0.05或P<0.01)。见表 6。
比较灯盏花素注射液和合成灯盏乙素注射液对TNF-α含量的影响,给药1 d,BI-L组<BI-H组<SSI-L组<SSI-H组;给药3 d,BI-H组<SSI-H组<SSI-L组<BI-L组;给药7 d,BI-H组<SSI-L组<BI-L组<SSI-H组;给药14 d,SSI-H组<SSI-L组<BI-L组<BI-H组。
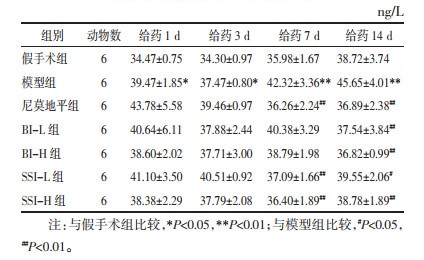
3.2.4 对各时间点大鼠血清ICAM-1含量的影响与假手术组比较,给药1、3、7、14 d,模型组ICAM-1含量均显著增加(P<0.05或P<0.01)。与模型组比较,给药1、3 d,各给药组ICAM-1含量均无显著性差异;给药7 d,尼莫地平组、SSI-L组和SSI-H组ICAM-1含量显著降低(P<0.01),BI-L组和BI-H组ICAM-1含量有所降低;给药14 d,各给药组ICAM-1含量均显著降低(P<0.05或P<0.01)。见表 7。
比较灯盏花素注射液和合成灯盏乙素注射液对ICAM-1含量的影响,给药1 d,SSI-H组<BI-H组<BI-L组<SSI-L组;给药3天,BI-H组<SSI-H组<BI-L组<SSI-L组;给药7 d,SSI-H组<SSI-L组<BI-H组<BI-L组;给药14 d,BI-H组<BI-L组<SSI-H组<SSI-L组。
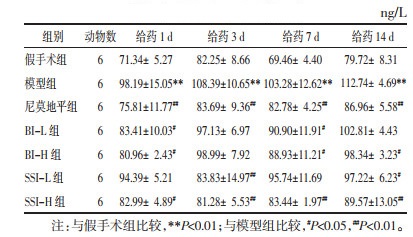
3.2.5 对各时间点大鼠血清IL-6含量的影响与假手术组比较,给药1、3、7、14 d,模型组IL-6含量均显著增加(P<0.01)。与模型组比较,给药1 d,除SSI-L组,其他各给药组IL-6含量均显著降低(P<0.05或P<0.01);给药3 d,尼莫地平组、SSI-L组和SSI-H组IL-6含量显著降低(P<0.01),BI-L组和BI-H组IL-6含量有所降低;给药7 d,除SSI-L组,其他各给药组IL-6含量均显著降低(P<0.05或P<0.01);给药14 d,除BI-L组,其他各给药组IL-6含量均显著降低(P<0.05或P<0.01)。见表 8。
比较灯盏花素注射液和合成灯盏乙素注射液对IL-6含量的影响,给药1 d,BI-H组<SSI-H组<BI-L组<SSI-L组;给药3 d,SSI-H组<SSI-L组<BI-L组<BI-H组;给药7 d,SSI-H组<BI-H组<BI-L组<SSI-L组;给药14 d,SSI-H组<SSI-L组<BI-H组<BI-L组。
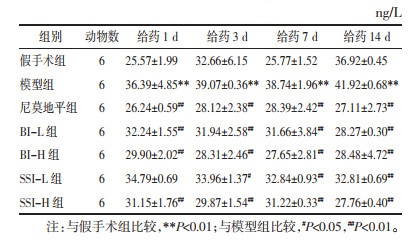
3.2.6 对各时间点大鼠血清IL-1β含量的影响与假手术组比较,给药1、3、7、14 d,模型组IL-1β含量均显著增加(P<0.01)。与模型组比较,给药1 d,除SSI-L组,其他各给药组IL-1β含量均显著降低(P<0.01);给药3、7、14 d,各给药组IL-1β含量均显著降低(P<0.05或P<0.01)。见表 9。
比较灯盏花素注射液和合成灯盏乙素注射液对IL-1β含量的影响,给药1、3、7 d,BI-H组<SSI-H组<BI-L组<SSI-L组;给药14 d,SSI-H组<BI-L组<BI-H组<SSI-L组。
3.2.7 对各时间点大鼠血清IL-10含量的影响与假手术组比较,给药1、3、7、14 d,模型组IL-10含量均显著降低(P<0.01)。与模型组比较,给药1 d,各给药组IL-10含量均无显著性差异;给药3 d,除SSI-L组,其他各给药组IL-10含量均显著增加(P<0.05或P<0.01);给药7 d,各给药组IL-10含量均显著增加(P<0.01);给药14 d,除BI-L组,其他各给药组IL-10含量均显著增加(P<0.05或P<0.01)。见表 10。
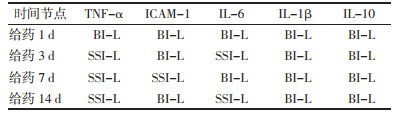
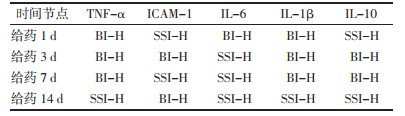
比较灯盏花素注射液和合成灯盏乙素注射液对IL-10含量的影响,给药1 d,BI-L组>SSI-H组>BI-H组>SSI-L组;给药3 d,BI-H组>SSI-H组>BI-L组>SSI-L组;给药7 d,BI-H组>BI-L组>SSI-L组>SSI-H组;给药14 d,SSI-H组>BI-H组>BI-L组>SSI-L组。见表 11、表 12。
|
|
临床常见的中药注射剂不良反应以过敏反应、过敏性休克、心悸、皮疹等为主[17]。《药物刺激性、过敏性和溶血性研究技术指导原则》[18]指出注射剂需要进行主动全身过敏试验。周莉等[19]研究发现《中药、天然药物免疫毒性(过敏性、光过敏反应)研究的技术指导原则》中收载的豚鼠主动全身过敏试验方法更加细致,故本研究采用此法开展实验;周莉等[19]指出,剂量如果太低,虽然在一定范围内,过敏反应发生率不变,但可能过敏反应轻微,而容易忽视观察豚鼠过敏症状,故本研究选取豚鼠等效剂量的5倍和20倍作为致敏阶段的低、高剂量。本研究发现,两种注射液过敏反应发生的严重程度随着致敏和激发剂量的增加而有所变化,BI高剂量组发生过敏反应的严重程度明显高于BI低剂量组,但SSI高剂量组却低于SSI低剂量组;BI过敏反应的发生率均为100%,SSI过敏反应的发生率随着剂量的增大而减小(从100%减小至83.33%)。由此可见,SSI高剂量组过敏反应发生率较低,其安全性更好。
炎症反应是脑缺血再灌注损伤复杂的级联反应中至关重要的一环[20-22]。再灌注再次暴露脑组织缺血、缺氧区域[23],导致免疫细胞激活和炎症损伤增加,从而使得促炎和抗炎细胞因子的表达。目前,已发现炎性细胞因子TNF-α、IL-1β、IL-6和IL-10是与脑缺血性疾病相关[24-25],其中促炎细胞因子TNF-α、IL-1β和IL-6表达升高,使缺血区白细胞被激活,发生局部炎性反应,同时通过刺激ICAM-1的合成,造成中性粒细胞浸润,进一步加重神经元损伤,导致缺血后炎症反应的发生。已有研究表明[3, 26-27],灯盏花素能够降低脑缺血再灌注模型大鼠脑中TNF-α、IL-1β、IL-6含量,并增加抗炎因子IL-10含量。而IL-10作为抗炎因子,可抑制IL-6、TNF-α和IL-1β等细胞因子的表达[28]。然而,不同剂量、给药时间不同,对于缺血再灌注损伤的炎症反应存在较大差别。本研究分别比较了两者低剂量组和高剂量组不同给药时间的抗炎疗效,结果表明,BI-L组比SSI-L组起效更快,SSI-H组比BI-H组持续效果更久。见表 10、11。
研究表明[29-30],BI在临床用于急性脑梗死患者具有较好的疗效,这与本研究的结果基本一致。本研究通过比较两种注射液不同剂量组过敏反应发生率,发现SSI安全性更高,提示BI中除灯盏乙素外的其他成分可能会促进过敏反应的发生,其安全性有待进一步探讨;通过抗炎作用比较,结果表明BI起效更快,适用于急性期,而SSI抗炎作用更加持久,较适用于后期恢复治疗,推测BI中其他成分可能与灯盏乙素发挥协同作用从而使BI起效更快,具体原因有待进一步探讨。
| [1] |
GAO J L, CHEN G, HE H Q, et al. Therapeutic effects of breviscapine in cardiovascular diseases: a review[J]. Frontiers in Pharmacology, 2017, 8: 289. DOI:10.3389/fphar.2017.00289 |
| [2] |
李响明, 孙胜斌, 姜国志. 灯盏花素注射剂质量控制研究进展[J]. 中国现代中药, 2020, 22(6): 971-978. |
| [3] |
曹小雨. 灯盏花素注射剂对大鼠脑缺血再灌注损伤的影响及microRNA和CYP介导的机制研究[D]. 南宁: 广西中医药大学, 2016.
|
| [4] |
国家药典委员会. 中华人民共和国药典-一部: 2020年版[M]. 北京: 中国医药科技出版社, 2020.
|
| [5] |
廖映迪, 倪小佳, 张昌林, 等. 灯盏花制剂防治缺血性脑卒中和短暂性脑缺血发作的临床研究进展[J]. 广东医学, 2020, 41(9): 963-967. |
| [6] |
廉全荣, 封臻. 灯盏花素对大鼠缺血再灌注后脑组织炎性细胞因子表达的影响[J]. 中国医学前沿杂志(电子版), 2015, 7(5): 112-115. |
| [7] |
戴新文, 张海宇, 王登科, 等. 灯盏花素注射液对脑出血后大鼠脑组织含水量及炎症介质ICAM-1的影响[J]. 神经解剖学杂志, 2011, 27(6): 665-669. |
| [8] |
魏静, 陈景瑞, 苗琳, 等. 灯盏乙素对LPS诱导的RAW264.7细胞炎症介质分泌的影响[J]. 天津中医药, 2016, 33(8): 487-490. |
| [9] |
WANG S, WANG H, GUO H, et al. Neuroprotection of scutellarin is mediated by inhibition of microglial inflammatory activation[J]. Neuroscience, 2011, 185: 150-160. |
| [10] |
仇锦林. 灯盏花素注射液常见不良反应[J]. 临床合理用药杂志, 2017, 10(23): 96-97. |
| [11] |
周其如, 鲁德林, 陈君, 等. 灯盏花素注射液致过敏反应分析[J]. 西部中医药, 2014, 27(3): 88-92. |
| [12] |
钟薇. 灯盏花素注射液常见不良反应临床分析[J]. 亚太传统医药, 2015, 11(15): 141-142. |
| [13] |
赵瑜君, 于一凡, 黄璐琦. 药用植物灯盏细辛组织培养分析[J]. 分子植物育种, 2023, 21(15): 5058-5065. |
| [14] |
闫亚哲, 闻豪, 杜江, 等. 灯盏花中灯盏乙素生物合成相关基因转录组分析[J]. 西南农业学报, 2022, 35(6): 1318-1324. |
| [15] |
魏伟, 吴希美, 李元建. 药理实验方法学[M]. 4版. 北京: 人民卫生出版社, 2010.
|
| [16] |
LONGA E Z, WEINSTEIN P R, CARLSON S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke, 1989, 20(1): 84-91. |
| [17] |
武晓红. 中药注射剂不良反应与安全性评价研究[J]. 山西中医学院学报, 2019, 20(1): 76-77, 79. |
| [18] |
国家食品药品监督管理局. 药物刺激性、过敏性和溶血性研究技术指导原则[S]. 北京: 国家食品药品监督管理局, 2014.
|
| [19] |
周莉, 王永, 杨春雷, 等. 注射用灯盏花素豚鼠全身主动过敏性试验评价方法的比较[J]. 中国药理学与毒理学杂志, 2015, 29(2): 265-271. |
| [20] |
LIU H Q, WEI X B, KONG L J, et al. NOD2 is involved in the inflammatory response after cerebral ischemia-reperfusion injury and triggers NADPH oxidase 2-derived reactive oxygen species[J]. International Journal of Biological Sciences, 2015, 11(5): 525-535. |
| [21] |
LYU S T, YANG H Y, JING P C, et al. α-tocopherol pretreatment alleviates cerebral ischemia-reperfusion injury in rats[J]. CNS Neuroscience & Therapeutics, 2022, 28(6): 964-970. |
| [22] |
ZHOU K C, CHEN J, WU J Y, et al. Atractylenolide Ⅲ ameliorates cerebral ischemic injury and neuroinflammation associated with inhibiting JAK2/STAT3/Drp1-dependent mitochondrial fission in microglia[J]. Phytomedicine, 2019, 59: 152922. |
| [23] |
DELONG J H, OHASHI S N, O'CONNOR K C, et al. Inflammatory responses after ischemic stroke[J]. Seminars in Immunopathology, 2022, 44(5): 625-648. |
| [24] |
WONG C H, CRACK P J. Modulation of neuro-inflammation and vascular response by oxidative stress following cerebral ischemia-reperfusion injury[J]. Current Medicinal Chemistry, 2008, 15(1): 1-14. |
| [25] |
NAKAJIMA M, NITO C, SOWA K, et al. Mesenchymal stem cells overexpressing interleukin-10 promote neuroprotection in experimental acute ischemic stroke[J]. Molecular Therapy Methods & Clinical Development, 2017, 6: 102-111. |
| [26] |
CHEN Z P, WANG C, LIU Y J, et al. Protective effects of medicinal plant breviscapine on postcerebral hemorrhage in rats[J]. Journal of Integrative Neuroscience, 2020, 19(1): 101-109. |
| [27] |
JIANG L, HU Y, HE X, et al. Breviscapine reduces neuronal injury caused by traumatic brain injury insult: partly associated with suppression of interleukin-6 expression[J]. Neural Regeneration Research, 2017, 12(1): 90-95. |
| [28] |
HWANG C J, YUN H M, JUNG Y Y, et al. Reducing effect of IL-32α in the development of stroke through blocking of NF-κB, but enhancement of STAT3 pathways[J]. Molecular Neurobiology, 2015, 51(2): 648-660. |
| [29] |
李辰, 谭燕萍, 毛振林, 等. 灯盏花素注射液联合依达拉奉注射液对未溶栓急性脑梗死患者神经功能、脑血流动力学和血清炎症细胞因子的影响[J]. 现代生物医学进展, 2022, 22(24): 4691-4694, 4685. |
| [30] |
卢烈梅, 刘政委, 刘志标, 等. 灯盏花素治疗急性脑梗死的临床疗效观察[J]. 中西医结合心脑血管病杂志, 2017, 15(17): 2192-2195. |
 2024, Vol. 41
2024, Vol. 41